(Vaccini mRNA-Immagine Credit Public Domain).
Le nanoparticelle lipidiche (LNP) sono i veicoli di trasporto che proteggono le molecole di RNA messaggero (mRNA) dalla degradazione e aiutano il rilascio intracellulare e la fuga endosomiale nelle piattaforme vaccinali mRNA-LNP modificate con nucleosidi attualmente utilizzate da Pfizer / BioNTech e Moderna, contro la sindrome respiratoria acuta grave coronavirus 2 (SARS-CoV-2).
Questi due vaccini superano gli altri con il loro supporto efficace per le cellule T helper follicolari (Tfh) e le risposte umorali protettive osservate negli studi preclinici.
Sebbene sia stabilito il ruolo vitale degli LNP nell’azione di questi vaccini, la natura potenzialmente infiammatoria di questi LNP non viene valutata. Inoltre, negli studi sull’uomo dei vaccini Pfizer / BioNTech e Moderna, è stato riportato che gli effetti collaterali spesso legati all’infiammazione, come dolore, gonfiore, febbre e sonnolenza, sono comuni.
Poiché si presumeva che il vaccino non fosse infiammatorio, si è ritenuto che questi effetti collaterali fossero generati dalla potente risposta immunitaria al vaccino. Pertanto, è necessario un approccio sistemico per analizzare le proprietà infiammatorie degli LNP e comprenderne il ruolo nel processo di vaccinazione.
In un recente documento di ricerca pubblicato in preprint bioRxiv *, Botond Z. Igyártó e colleghi della Thomas Jefferson University hanno dimostrato la natura infiammatoria delle nanoparticelle lipidiche (LNP). Dopo somministrazione intradermica nei topi, i ricercatori hanno osservato una massiccia infiltrazione di neutrofili, l’attivazione di diverse vie infiammatorie e la produzione di varie citochine e chemochine infiammatorie. Hanno osservato reazioni simili a quelle derivate degli LNP somministrati per via intranasale.
Vedi anche:Vaccino Pfizer Biontech: da Israele nuovi dati sulla risposta immunitaria
In particolare, l’inoculazione intranasale con la stessa dose (10 μg) di LNP (come nella consegna intradermica) ha causato un alto tasso di mortalità nei topi: circa l’80% dei topi trattati è morto in meno di 24 ore. I ricercatori hanno scoperto che le proprietà infiammatorie degli LNP non sono specifiche del sito. Hanno osservato una rapida diffusione, dispersione e velocità di distribuzione nei tessuti, al momento del rilascio interno. “Pertanto, l’ambiente infiammatorio indotto dagli LNP potrebbe essere parzialmente responsabile degli effetti collaterali segnalati dei vaccini SARS-CoV-2 basati su mRNA-LNP negli esseri umani e potrebbero contribuire alla loro elevata potenza segnalata per suscitare l’immunità protettiva”.
Gli LNP sono costituiti da una miscela di fosfolipidi, colesterolo, lipidi PEGilati e lipidi cationici o ionizzabili. Questi migliorano la struttura, la stabilità e supportano la circolazione prolungata. I lipidi cationici / ionizzabili, complessi con le molecole di mRNA caricate negativamente, consentono l’uscita dell’mRNA dall’endosoma al citosol per la traduzione.
È stato riferito che alcuni LNP contenenti lipidi ionizzabili / cationici sono altamente infiammatori e possibilmente citotossici. Uno studio preclinico ha mostrato l’attività adiuvante dell’mRNA complessato con LNP. Per evitare l’attivazione di vie infiammatorie innate, nel vaccino, l’mRNA è modificato dai nucleosidi.
In questo studio, i ricercatori hanno notato che la natura infiammatoria degli LNP potrebbe spiegare la loro potente attività adiuvante e la loro superiorità, rispetto ad altri adiuvanti, nel supportare l’induzione di risposte immunitarie adattative.
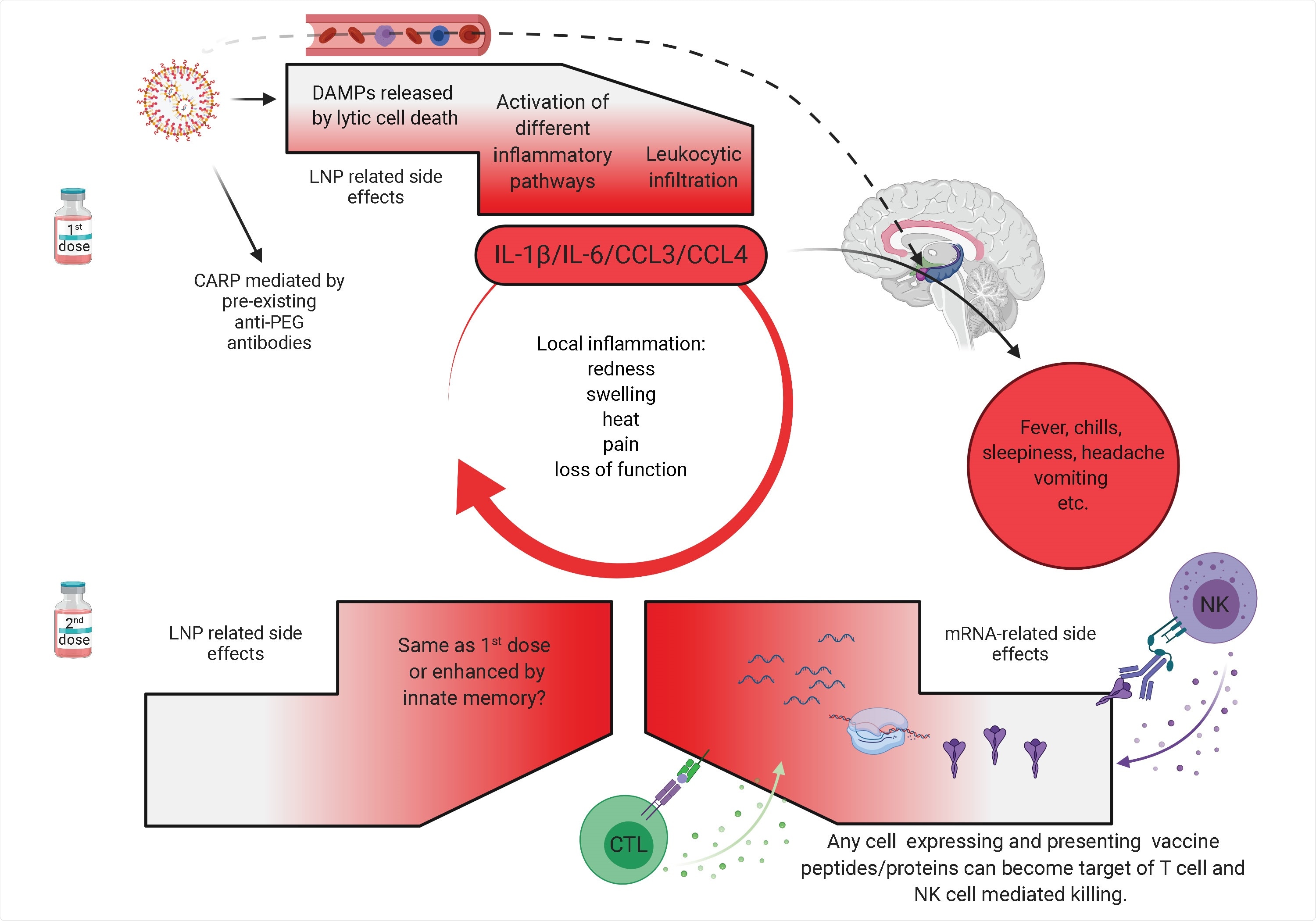
Potenziale meccanismo di effetti collaterali. Gli effetti collaterali osservati con la prima dose del vaccino SARS-CoV-2 sono probabilmente associati alle proprietà infiammatorie degli LNP. Gli LNP attivano diverse vie infiammatorie che porteranno alla produzione di citochine infiammatorie, come IL-1β e IL-6, che possono avviare e sostenere infiammazioni locali e sistemiche ed effetti collaterali. Gli LNP possono anche diffondersi dalla periferia e raggiungere qualsiasi organo del corpo, compreso il SNC (ipotalamo) dove potrebbero indurre direttamente effetti collaterali (linea tratteggiata). Il PEG è ampiamente usato come additivo alimentare e medicinale e molti di noi sviluppano anticorpi contro il PEG. Pertanto, i lipidi PEGilati degli LNP possono indurre CARP negli esseri umani con anticorpi PEG specifici preesistenti. Gli esseri umani spesso sperimentano effetti collaterali più gravi con la seconda dose. Qui ipotizziamo che potrebbe essere dovuto a molteplici ragioni. In primo luogo, la memoria immunitaria innata contro gli LNP potrebbe formarsi dopo la prima vaccinazione e ciò potrebbe portare a risposte infiammatorie ancora più robuste alla seconda vaccinazione. In secondo luogo, dopo la prima vaccinazione si formano risposte immunitarie adattative che prendono di mira la proteina virale codificata dall’mRNA. Pertanto, le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. la memoria immunitaria innata contro gli LNP potrebbe formarsi dopo la prima vaccinazione e ciò potrebbe portare a risposte infiammatorie ancora più robuste alla seconda vaccinazione. In secondo luogo, dopo la prima vaccinazione si formano risposte immunitarie adattative che prendono di mira la proteina virale codificata dall’mRNA. Pertanto, le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. la memoria immunitaria innata contro gli LNP potrebbe formarsi dopo la prima vaccinazione e ciò potrebbe portare a risposte infiammatorie ancora più robuste alla seconda vaccinazione. In secondo luogo, dopo la prima vaccinazione si formano risposte immunitarie adattative che prendono di mira la proteina virale codificata dall’mRNA. Pertanto, le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. e ciò potrebbe portare a risposte infiammatorie ancora più robuste alla seconda vaccinazione. In secondo luogo, dopo la prima vaccinazione si formano risposte immunitarie adattative che prendono di mira la proteina virale codificata dall’mRNA. Pertanto, le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. e ciò potrebbe portare a risposte infiammatorie ancora più robuste alla seconda vaccinazione. In secondo luogo, dopo la prima vaccinazione si formano risposte immunitarie adattative che prendono di mira la proteina virale codificata dall’mRNA. Pertanto, le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata. le cellule (mostrate come forma rossa) che esprimono i peptidi derivati dalla proteina virale o la proteina stessa possono diventare il bersaglio dell’uccisione mediata da cellule CD8 + T o NK (ADCC), rispettivamente. Poiché gli LNP potrebbero diffondersi in tutto il corpo e trasfettare qualsiasi cellula nel loro percorso con l’mRNA, e l’mRNA potrebbe anche essere ulteriormente distribuito attraverso vescicole extracellulari (Maugeri et al., 2019), la popolazione target potrebbe essere potenzialmente vasta e diversificata.
Come previsto con gli effetti collaterali osservati nell’uomo dopo la vaccinazione intramuscolare con i vaccini Pfizer / BioNTech o Moderna, l’inoculazione intradermica di LNP nei topi ha portato alla secrezione dei pirogeni – IL-1β / IL-6 e della proteina infiammatoria dei macrofagi-α (CCL3 ) e la proteina-β infiammatoria dei macrofagi (CCL4). “Nel complesso, il robusto ambiente infiammatorio indotto dagli LNP, combinato con la presentazione dei peptidi / proteine derivati dal vaccino al di fuori delle cellule che presentano l’ antigene, potrebbe causare danni ai tessuti ed esacerbare gli effetti collaterali”.
I ricercatori hanno espresso la preoccupazione che gli LNP, come particelle lipidiche che possono diffondersi rapidamente, potrebbero potenzialmente accedere al sistema nervoso centrale (SNC) attraverso il bulbo olfattivo o il sangue. Tuttavia, questo deve essere determinato con ulteriori studi. Inoltre, deve essere studiato il ruolo delle risposte innate della memoria agli LNP.
In conclusione, l’inoculazione intradermica con LNP ha indotto una forte infiammazione nei topi. Utilizzando diverse tecniche, i ricercatori hanno dimostrato che gli LNP, da soli o complessati con l’mRNA della policitosina non codificante di controllo, sono altamente infiammatori nei topi, probabilmente attraverso l’impegno e l’attivazione di varie vie infiammatorie distinte e convergenti.
È importante sottolineare che questo studio ha dimostrato che il rilascio intradermico o intranasale nei topi di LNP utilizzati negli studi preclinici innesca l’infiammazione caratterizzata da infiltrazione leucocitaria, attivazione di diverse vie infiammatorie e secrezione di un pool diversificato di citochine infiammatorie e chemochine.
“Tuttavia, saranno necessari ulteriori studi per determinare l’esatta natura delle risposte infiammatorie innescate dai vaccini mRNA-LNP negli esseri umani e quanta sovrapposizione potrebbe esserci con le firme infiammatorie qui documentate per i topi”, scrivono i ricercatori.“Tuttavia, sarà necessario trovare un equilibrio tra proprietà adiuvanti positive e infiammatorie negative man mano che i vaccini associati a LNP vanno avanti”.
*Avviso IMPORTANTE
bioRxiv pubblica rapporti scientifici preliminari che non sono sottoposti a revisione paritaria e, pertanto, non devono essere considerati conclusivi.
Fonte:bioRxiv