“Il recupero è senza precedenti”, dice l’autore Jerry Silver.”Ciascuno dei 21 animali ha qualcosa di nuovo in termini di funzione”.
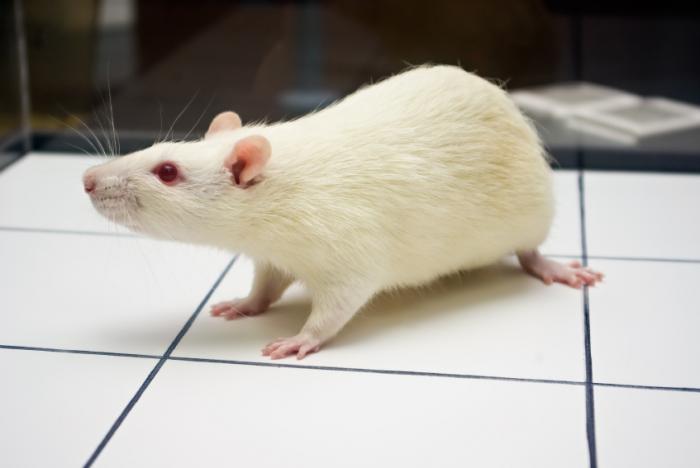
Un team internazionale di scienziati sono stati coinvolti nella ricerca che ha dimostrato che 21 dei 26 animali con lesioni del midollo spinale hanno riacquistato la capacità di urinare o spostarsi, o entrambi, dopo il trattamento con intracellulare peptide sigma (ISP).
Lyn Jakeman, PhD, direttore del National Institute of Neurological Disorders and Stroke in Bethesda, MD, spiega che non esistono attualmente terapie farmacologiche “che migliorano il molto limitato recupero da lesioni del midollo spinale”.
Il nuovo trattamento è “un grande passo verso l’identificazione di un nuovo agente per il trattamento dei pazienti con lesioni del midollo spinale”.
I risultati dello studio sono stati pubblicati sulla rivista Nature .
Il leader dello studio, Jerry Silver, PhD, Case Western Reserve University School of Medicine professor of Neurosciences, spiega i risultati:
“Questo recupero è senza precedenti. Tutti i 21 animali hanno acquisito qualcosa di nuovo in termini di funzione. Per tutti i pazienti con lesioni al midollo spinale, oggi, sarebbe considerato straordinario poter riconquistare anche una di queste funzioni, in particolare la funzione della vescica. ISP ha inoltre potenziale per il trattamento di altre condizioni in cui il corpo produce cicatrici distruttive quali l’infarto, lesioni del nervo periferico e la sclerosi multipla(SM)”.
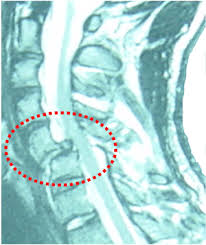
I proteoglicani, molecole chiave che mantengono la struttura del sistema nervoso centrale (CNS), diventano sovrabbondanti nel tessuto cicatriziale, intorno alle sinapsi e midollo spinale.
Da questa sovrabbondanza risultano ostacoli appiccicosi che impediscono agli impulsi elettrici di essere trasmessi alle cellule nervose.
Il peptide ISP è stato progettato per spegnere i recettori proteoglicani nei neuroni. Inoltre i ricercatori hanno anche sviluppato un trans-attivatore della trascrizione, chiamato TAT, che permette ad ISP di viaggiare attraverso le membrane e in tutto il sistema nervoso centrale.
Questa capacità di attraversare le membrane significa che ISP può passare facilmente attraverso il tessuto cicatriziale dei siti di lesioni. Essa consente inoltre al composto la consegna sistematica anziché attraverso un’iniezione diretta nel midollo spinale.
Il composto è stato sperimentato su 26 ratti con gravi lesioni del midollo spinale, i quali sono stati valutati per le loro capacità di camminare, per l’ equilibrio e la capacità di urinare. Sebbene alcuni ratti abbiano riacquistato tutte queste funzioni, alcuni di loro ne hanno riguadagnato solo una o due. Complessivamente, 21 dei 26 topi hanno recuperato parte – se non tutto – delle funzioni.
I ricercatori non sanno perché alcuni dei topi hanno recuperato completamente e altri no – “Questa è una delle grandi questioni rimanenti”, dice Silver, ” pensiamo che un indizio può essere trovato nelle vie nervose del midollo spinale dei ratti”.
Ogni topo aveva danni diversi nei tratti del midollo spinale. Tuttavia, un tratto del midollo spinale in particolare – che contiene fibre serotoninergiche che rilasciano la serotonina nel midollo spinale, – ha dimostrato di rispondere con forza a ISP.
Il team continuerà ad indagare. “Il nostro obiettivo è quello di progredire in questo trattamento per l’uso terapeutico delle lesioni del midollo spinale”, conclude Silver.
Fonte
Modulation of the proteoglycan receptor PTPs promotes recovery after spinal cord injury, Jerry Silver, et al., Nature, doi:10.1038/nature13974, published online 3 December 2014.
Case Western Reserve University news release, accessed 4 December 2014 via Newswise.