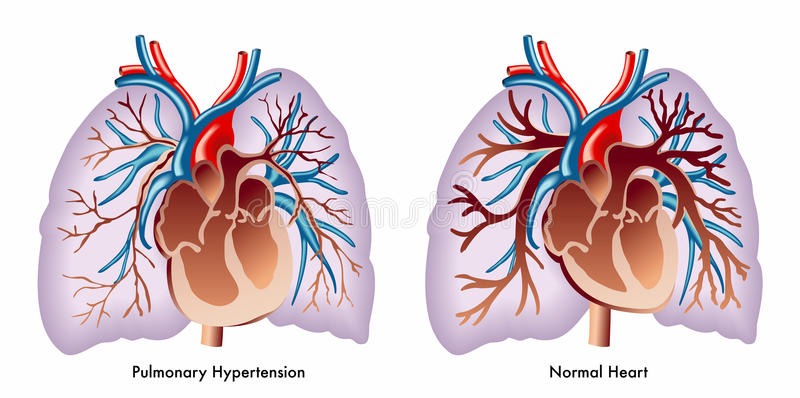
Lavorando con le cellule che rivestono lo strato più interno dei vasi sanguigni, i ricercatori della Johns Hopkins affermano di aver fatto un passo avanti nella comprensione della biologia sottostante l’ipertensione polmonare, un tipo pericoloso di ipertensione nei polmoni che alla fine porta allo scompenso cardiaco destro e alla morte .
Conducendo esperimenti su cellule endoteliali, i ricercatori hanno scoperto che una proteina chiamata KLF15 (fattore 15 di tipo Kruppel) protegge queste cellule dai danni in caso di condizioni gravi come la privazione dell’ossigeno che può portare all’ipertensione polmonare. I ricercatori hanno dimostrato che KLF15 è probabilmente un regolatore chiave di geni importanti per il mantenimento della corretta funzione dei vasi sanguigni polmonari. È interessante notare che KLF15 può proteggere il sistema cardiovascolare da condizioni simili a quelle che gli animali sperimentano durante il letargo.
Durante uno stato di ossigeno ridotto, i livelli di KLF15 possono precipitare causando una serie di reazioni a catena che probabilmente contribuiscono al danno dei vasi sanguigni e alla progressione dell’ipertensione polmonare.
I ricercatori affermano di poter alterare geneticamente le cellule cresciute in una Piastra di Petri in modo tale da indurre un aumento dell’espressione di KLF15 e invertire il danno, ripristinando il normale funzionamento delle cellule nonostante l’esposizione a bassi livelli di ossigeno. Una descrizione degli esperimenti e dei risultati che è stata pubblicata online il 22 febbraio 2018 nella rivista Arteriosclerosis, Thrombosis e Vascular Biology, suggerisce nuovi obiettivi per lo sviluppo di farmaci per l’ipertensione polmonare.
“I nostri esperimenti fanno avanzare la nostra comprensione del modo in cui i bassi livelli di ossigeno fanno ammalare i vasi sanguigni”, dice Lewis Romer, coautore senior dello studio e Professore di anestesia e medicina, biologia cellulare, ingegneria biomedica e pediatria presso la Johns Hopkins University School of Medicine. Romer conduce anche ricerche sull’ipertensione polmonare al Johns Hopkins Children’s Center. “I risultati avanzano potenzialmente anche la ricerca di farmaci che non solo controllano l’ipertensione polmonare, ma possono anche invertire la malattia o curarla”.
( Vedi anche:Scoperto un nuovo tipo di cellule alla base dell’ ipertensione polmonare).
“Negli Stati Uniti, l’ipertensione polmonare è considerata una malattia rara, che colpisce circa 109 persone per milione, sotto i 65 anni e 451 persone per milione oltre i 65 anni”, dice Romer. La condizione può essere gestita attraverso farmaci che massimizzano il flusso di sangue attraverso i polmoni o, in casi gravi, un trapianto di cuore o cuore-polmone. Se non trattata, metà delle persone con la condizione può morire entro due o cinque anni dalla diagnosi, “quindi è molto importante per la comunità medica avere una migliore comprensione di ciò che accadendo con la malattia di base” dice il ricercatore.
Le proteine della famiglia KLF sono note per essere importanti regolatori della funzione evolutiva e biologica dei vasi sanguigni. KLF15 ha dimostrato di recente di svolgere un ruolo protettivo in alcune condizioni cardiache come l’insufficienza cardiaca e la formazione di aneurismi aortici, ma il suo ruolo nell’alterazione della funzione delle cellule endoteliali che rivestono i vasi sanguigni del polmone era sconosciuto.
Pertanto, per il presente studio, il gruppo di ricerca si è proposto di determinare il ruolo di KLF15 nel controllo dei geni critici per la funzione delle cellule endoteliali in uno stato di ipertensione polmonare.
Tra i risultati, i ricercatori hanno mostrato quanto segue: KLF15 è normalmente abbondante nelle cellule endoteliali e regola altri enzimi fondamentali per la funzione endoteliale, compresa la repressione di Arg2 (arginase-2); in uno stato di basso livello di ossigeno, i livelli di KLF15 diminuiscono e aumenta Arg2 e sovraesprimere KLF15 potrebbe completamente invertire il danno causato dall’esposizione a uno stato di basso ossigeno, consentendo ancora una volta la produzione di ossido nitrico – una sostanza naturale che dilata i vasi sanguigni per aumentare il flusso sanguigno e previene rimodellamento e infiammazione anomala dei vasi sanguigni.
“Quando le cellule vengono esposte a bassi livelli di ossigeno, producono grandi quantità di specie reattive dell’ossigeno che sono dannose e anche una minore quantità di ossido nitrico, che è protettivo.Questo porta le cellule a uno stato di” stress ossidativo “, dice Deepesh Pandey, assistente Professore di anestesiologia e medicina di terapia intensiva presso la Johns Hopkins University School of Medicine e membro principale del gruppo di ricerca. “Quando aumentiamo l’espressione di KLF15 in queste cellule, la produzione di specie reattive dell’ossigeno e l’ossido di azoto è ripristinata alla normalità”.
Aggiunge Dan Berkowitz, MBBCh., Professore di anestesiologia e medicina e vicepresidente per la ricerca in anestesia e medicina di terapia intensiva presso Johns Hopkins, “Stiamo essenzialmente reclutando un meccanismo di protezione naturale che viene utilizzato da animali in letargo per lo sviluppo di una potenziale terapia nel contesto di uno stimolo stressante, che in questo caso è la carenza di ossigeno o privazione.Il meccanismo è chiamato SUMOilazione ( La sumoilazione è un meccanismo regolatorio della funzione e della localizzazione di numerose proteine, rappresenta una modificazione proteica post-traduzionale e consiste nell’aggiunta, covalente e reversibile, di piccole proteine simili all’ubiquitina, le SUMOs (Small Ubiquitin-like Modifier) a specifici bersagli) e gli agenti che promuovono questo processo potrebbero diventare nuove terapie per l’ipertensione polmonare”.
Fonte: Johns Hopkins Medicine