Infiammazione-Immagine Credit Public Domain-
Una nuova serie di studi riportati sull’American Journal of Pathology indica che mediatori lipidici specializzati prorisolutivi possono migliorare o potenziare il trattamento per il declino degli organi legato all’età.
La risoluzione dell’infiammazione è un processo attivo governato da numerosi fattori, come i mediatori lipidici prorisolutivi specializzati (SPM). Studi recenti suggeriscono che l’infiammazione può persistere a causa di un’alterazione dei programmi di risoluzione dell’infiammazione e che il trattamento con SPM, come le resolvine, attenua l’eccessiva infiammazione e la disfunzione tissutale legata all’età.
I ricercatori co-responsabili dello studio Gabrielle Fredman, PhD, Dipartimento di fisiologia molecolare e cellulare, Albany Medical College e Katherine C. MacNamara, PhD, Dipartimento di immunologia e malattie microbiche, Albany Medical College, hanno spiegato: “Ci siamo resi conto fin dall’inizio della nostra collaborazione che i meccanismi associati alla risoluzione dell’infiammazione nell’invecchiamento erano ampiamente sottoesplorati. Pertanto, abbiamo unito le nostre competenze collettive per colmare alcune lacune in questo ambito”.
Per esplorare i meccanismi avviati da SPM che limitano le caratteristiche dell’infiammazione, i ricercatori hanno condotto una nuova serie di studi utilizzando il ligando o messaggero chimico, Resolvin D2 (RvD2). RvD2 agisce tramite uno specifico recettore accoppiato alla proteina G chiamato GPR18 che i ricercatori hanno scoperto essere associato al mantenimento dell’omeostasi dei tessuti durante l’invecchiamento.
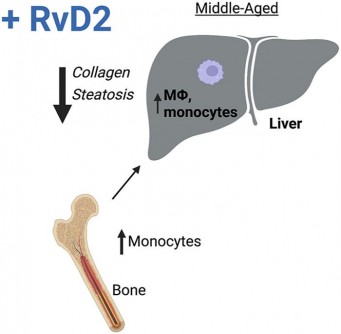
Utilizzando i topi per modellare un invecchiamento normale e sano, i ricercatori hanno identificato i principali cambiamenti patologici nel fegato che si verificano nella mezza età, tra cui la steatosi (malattia del fegato grasso) e la deposizione di collagene. Hanno osservato che questi cambiamenti erano correlati a una riduzione dei macrofagi proriparativi (protettivi). Poiché l’analisi trascrizionale ha mostrato che Gpr18 era aumentato nei macrofagi anziani rispetto a quelli giovani, hanno studiato il suo ruolo nell’invecchiamento generando un topo knockout condizionale in cui solo le cellule mieloidi mancano di GPR18 e attraverso il trattamento dei topi con il ligando di GPR18, RvD2.
Insieme, i loro studi hanno dimostrato che il GPR18 mieloide-specifico limitava la steatosi e l’accumulo di collagene nel fegato. Inoltre, l’aggiunta di RvD2 da una fonte esterna per attivare GPR18 ha migliorato l’istopatologia del fegato. I ricercatori hanno anche scoperto che il trattamento con RvD2 ha aumentato i monociti del midollo osseo e del sangue, nonché i loro precursori. Per esaminare come la funzione del midollo osseo contribuisse alla patologia epatica, hanno eseguito trapianti di midollo osseo in cui hanno ricostituito topi giovani con il midollo di animali giovani o anziani, con o senza trattamento con RvD2.
Il Dottor MacNamara ha osservato: “Questi studi hanno rivelato che il midollo donato da animali anziani era sufficiente per indurre l’accumulo di collagene nel fegato, dimostrando che l’invecchiamento del midollo osseo contribuisce alla patologia epatica. È importante sottolineare, tuttavia, che questo potrebbe essere migliorato con il trattamento RvD2”.
Il Dr. Fredman ha commentato: “ Insieme, questi studi dimostrano che la segnalazione RvD2-GPR18 controlla la steatosi e la fibrosi e fornisce una terapia basata su meccanismi per promuovere la riparazione del fegato durante l’invecchiamento”.
I ricercatori sono rimasti sorpresi dalla specificità delle azioni di RvD2 sul midollo osseo e dall’osservazione che RvD2, quando aggiunto ex vivo, agiva direttamente sul midollo osseo per indurre un aumento specifico dei progenitori monociti/macrofagi.
Il Dottor MacNamara ha spiegato: “Questo studio è stato entusiasmante perché mentre molto è stato studiato riguardo al modo in cui i mediatori lipidici specializzati nella prorisoluzione influiscono sulla funzione dei macrofagi, si sa molto meno riguardo al loro impatto sulla produzione di cellule del sangue. Poiché i monociti e i macrofagi sono importanti per l’omeostasi dei tessuti in tutto il corpo, essenzialmente in tutti gli organi, riteniamo che la capacità di RvD2 di aumentare la produzione di monociti sarà rilevante per molte malattie o contesti di invecchiamento in cui la riparazione dei tessuti è ostacolata”.
Il Dottor Fredman ha aggiunto: “Forse la sorpresa più grande è stata che anche un trattamento molto breve con RvD2 sul midollo osseo più vecchio nei topi riceventi ha avuto una risposta così profonda e duratura. Abbiamo utilizzagto i trapianti di midollo osseo per una sola settimana e abbiamo scoperto che anche questo trattamento transitorio con RvD2 poteva migliorare la patologia epatica quattro mesi dopo. Questi risultati suggeriscono che RvD2 può partecipare ad alcune programmazioni a lungo termine del midollo osseo, delle cellule immunitarie o persino del fegato”.
I ricercatori hanno concluso che questi studi forniscono una prova del fatto che RvD2 può alleviare le cicatrici epatiche o la fibrosi, per le quali attualmente non esiste alcun trattamento e che la sua azione potrebbe essere in parte dovuta alla regolazione del midollo osseo.
Leggi anche:Infiammazione e vitamina B12: svelare la connessione nascosta
Secondo il Dottor MacNamara, “questi studi rivelano una potenziale terapia che può migliorare le patologie legate all’invecchiamento migliorando il processo di produzione delle cellule del sangue. L’idea che la produzione di midollo osseo possa essere modulata per generare cellule che forniscono funzioni riparative può essere ampiamente rilevante nell’invecchiamento. I nostri studi non solo evidenziano la notevole durata del trattamento, anche transitorio, con RvD2, ma dimostrano l’importante ruolo del midollo osseo e la sua funzione nella generazione delle cellule del sangue come aspetto chiave nel trattamento della malattia. Riteniamo che esista un’enorme promessa di mediatori lipidici specializzati prorisolutivi, come RvD2, come terapie che possono migliorare o potenziare i trattamenti attuali”.