Immagine:
Gli scienziati dell’Università della California, Berkeley, hanno progettato un nuovo modo di fornire la tecnologia di modifica del gene CRISPR-Cas9 all’interno delle cellule e hanno dimostrato nei topi che la tecnologia può riparare la mutazione che causa la distrofia muscolare di Duchenne, grave malattia da perdita di muscoli.
Un nuovo studio dimostra che una singola iniezione di CRISPR-Gold, come il nuovo sistema di somministrazione è chiamato, nei topi con distrofia muscolare di Duchenne ha portato ad un tasso di correzione di 18 volte superiore e un aumento di due volte della resistenza in un test di agilità.
Dal 2012, Jennifer Doudna, Professore di biologia molecolare e cellulare e di chimica presso la UC Berkeley e la collega Emmanuelle Charpentier, dell’Istituto Max Planck per la biologia delle infezioni, hanno cercato di creare un prodotto economico e preciso, utilizzando CRISPR/Cas9. i ricercatori sperano che le terapie basate su CRISPR-Cas9 possano un giorno rivoluzionare il trattamento delle malattie genetiche. Tuttavia, i trattamenti in via di sviluppo per le malattie genetiche rimangono una grande sfida della medicina. Questo perché la maggior parte delle malattie genetiche possono essere curate solo se la mutazione genetica causata dalla malattia viene corretta alla normale sequenza e questo è impossibile con le terapie convenzionali.
CRISPR / Cas9, tuttavia, può correggere le mutazioni del gene tagliando il DNA mutato e provocando una riparazione del DNA rivolta all’omologia. Tuttavia, devono essere sviluppate strategie per garantire in modo sicuro le componenti necessarie (Cas9, RNA guida che indirizza Cas9 ad un gene specifico e DNA donatore) nelle cellule prima che sia possibile realizzare potenziali trattamenti terapeutici basati su CRISPR-Cas9. Una tecnica comune per trasportare CRISPR-Cas9 nelle cellule impiega un virus, ma questa tecnica presenta numerose complicazioni. CRISPR-Gold, la nuova strategia, non necessita di virus.
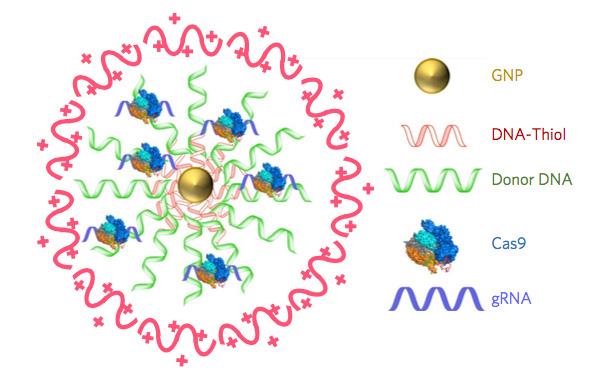
Nel nuovo studio, la ricerca condotta dai laboratori dei professori di bioengineering di Berkeley Niren Murthy e Irina Conboy, ha dimostrato che il nuovo approccio, denominato CRISPR-Gold perché le nanoparticelle d’oro sono una componente chiave, può fornire Cas9 – la proteina che lega e taglia il DNA con RNA guida e DNA donatore nelle cellule di un organismo vivente per fissare una mutazione del gene.
“CRISPR-Gold è il primo esempio di un veicolo di consegna che può fornire tutti i componenti CRISPR necessari per correggere le mutazioni del gene, senza l’uso di virus”, ha detto Murthy.
Lo studio è stato pubblicato il 2 ottobre nella rivista Nature Biomedical Engineering .
CRISPR-Gold ripara le mutazioni del DNA attraverso un processo chiamato riparazione diretta da omologia. Gli scienziati hanno lottato per sviluppare terapie a base di riparazione rivolta all’omologia, perché richiedono attività nello stesso luogo e tempo di Cas9, un RNA guida che riconosce la mutazione e il DNA donatore per correggere la mutazione.
Per superare queste sfide, gli scienziati di Berkeley hanno inventato un tipo di vaso di consegna che lega tutti questi componenti insieme e li rilascia quando il vaso si trova all’interno di un’ampia varietà di tipi di cellule, innescando la riparazione diretta da omologia. Le nanoparticelle d’oro di CRISPR-Gold rivestono il DNA del donatore e legano anche Cas9. Quando vengono iniettati nei topi, le loro cellule riconoscono un marcatore in CRISPR-Gold e quindi importano il vaso di consegna. Poi, attraverso una serie di meccanismi cellulari, CRISPR-Gold viene rilasciato nel citoplasma delle cellule e si rompe, rilasciando rapidamente Cas9 e il donatore DNA.
Una singola iniezione di CRISPR-Gold nei tessuti muscolari di topi modello della distrofia muscolare di Duchenne, ha ripristinato il 5,4 per cento del gene della distrofina, che causa la malattia. Tale tasso di correzione è stato circa 18 volte superiore a quello dei topi trattati con Cas9 e il DNA donatore da soli, che hanno registrato solo una percentuale di correzione dello 0,3%.
Importante, gli autori dello studio fanno notare che CRISPR-Gold ha ripristinato fedelmente la normale sequenza della distrofina, miglioramento significativo rispetto agli approcci precedentemente pubblicati che hanno rimosso solo la parte difettosa del gene, rendendolo più corto e convertendo una malattia in un’altra malattia più lieve.
CRISPR-Gold è stato anche in grado di ridurre la fibrosi tissutale – il segno distintivo delle malattie in cui i muscoli non funzionano correttamente – e ripristinare una maggiore forza e agilità nei topi con la distrofia muscolare di Duchenne.
“Questi esperimenti suggeriscono che sarà possibile sviluppare terapie CRISPR non virali che potranno correttamente correggere le mutazioni del gene, attraverso il processo di riparazione diretta da omologia, semplicemente sviluppando nanoparticelle che possono contemporaneamente incapsulare tutti i componenti CRISPR”, ha spiegato Murthy.
Lo studio ha riscontrato che l’approccio CRISPR-Gold per la consegna di proteine Cas9 è più sicuro della consegna virale di CRISPR che, oltre alla tossicità, amplifica gli effetti collaterali di Cas9 attraverso l’espressione continua di questo enzima di taglio del DNA. Quando il team di ricerca ha testato la capacità di modificare il gene di CRISPR-Gold nei topi, ha scoperto che CRISPR-Gold ha correttamente corretto la mutazione del DNA che causa la distrofia muscolare di Duchenne, con un minimo di danno collaterale al DNA.
I ricercatori hanno quantificato il danno del DNA off-target di CRISPR-Gold e hanno trovato livelli di danno simili a quelli di un tipico errore di sequenza del DNA in una cellula tipica non esposta a CRISPR (0,005-0,2%). Per testare l’eventuale immunogenicità, i profili di citochine dei topi sono stati analizzati 24 ore e due settimane dopo l’iniezione di CRISPR-Gold.
Sarà necessaria una sperimentazione clinica per sapere se CRISPR-Gold è un trattamento efficace per le malattie genetiche negli esseri umani. I coautori dello studio Kunwoo Lee e Hyo Min Park hanno formato una società di start-up, GenEdit (Murthy ha una quota di proprietà in GenEdit), che è incentrata sulla traduzione della tecnologia CRISPR-Gold negli esseri umani. I laboratori di Murthy e Conboy stanno lavorando anche sulla prossima generazione di particelle che possono trasportare CRISPR nei tessuti del flusso sanguigno.
“Le malattie genetiche causano livelli devastanti di mortalità e morbilità e sono necessarie nuove strategie per il loro trattamento”, ha detto Murthy. “CRISPR-Gold è stato in grado di correggere le mutazioni del gene causanti malattie in vivo, attraverso la consegna non virale di proteine Cas9, RNA e DNA donatore, e quindi ha il potenziale di svilupparsi in un terapeutico trattamento delle malattie genetiche”.
Fonte: Nature