Rezatapopt-immagine credit public domain
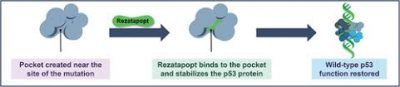
Ricercatori e collaboratori del Memorial Sloan Kettering Cancer Center hanno testato Rezatapopt, un attivatore orale di p53 progettato per i tumori con TP53 Y220C e hanno osservato un’attività antitumorale su diversi tipi di tumori solidi in uno studio di fase 1. Il Rezatapopt si lega specificamente al p53 mutato Y220C, stabilizza il p53 in una conformazione wild-type e ripristina la funzionalità di p53.
Tutti noi abbiamo cellule che si svilupperebbero in tumori clinicamente cancerosi se non fosse per alcune proteine piuttosto utili che ne sopprimono la crescita iniziale. Tra gli oltre 30 trilioni di cellule del corpo umano, si stima che diverse diventino cancerose in un giorno normale, ed è raro che qualcuna di queste sfugga al sistema immunitario e ai meccanismi di riparazione del DNA abbastanza a lungo da formare un tumore.
TP53 codifica p53, una proteina oncosoppressore che regola un’ampia varietà di funzioni cellulari. La proteina p53 attiva trascrizionalmente geni che codificano soppressori della crescita tumorale e proteine proapoptotiche che contribuiscono alla difesa cellulare contro il cancro, essenzialmente impedendo alle cellule con DNA danneggiato di dividersi.
Il problema p53
Alterazioni del gene TP53 sono presenti in oltre il 50% dei tumori maligni. Il carcinoma ovarico sieroso di alto grado può raggiungere il 95%. Le mutazioni di TP53 sono associate a una prognosi sfavorevole in molti tumori e si verificano con elevata frequenza nei tipi di tumore più aggressivi e invasivi.
Attualmente non sono disponibili terapie mirate specifiche per TP53, sebbene recenti scoperte scientifiche abbiano trasformato p53 da “non farmacologico” a bersaglio terapeutico valido. I ricercatori stanno attivamente cercando modi per supportare la potente capacità di p53 dell’organismo di combattere il cancro.
Le alterazioni Y220C di TP53 si verificano in circa l’1% di tutti i tumori solidi e rappresentano la nona mutazione più frequente di TP53 tra i tumori umani. Y220C riduce la temperatura di fusione di p53, producendo p53 termodinamicamente instabile con perdita della funzione di oncosoppressore.
Y220C crea anche una tasca in p53 che può ospitare il legame di piccole molecole. Rezatapopt è stato progettato per adattarsi a questa tasca attraverso legami a idrogeno non covalenti che migliorano le interazioni idrofobiche e di van der Waals, stabilizzando p53 con mutazione Y220C.
Nello studio “Phase 1 Study of Rezatapopt, a p53 Reactivator, in TP53 Y220C–Mutated Tumors”, pubblicato sul New England Journal of Medicine, i ricercatori hanno assegnato pazienti pesantemente pretrattati a ricevere Rezatapopt per determinare la dose massima tollerata e il dosaggio raccomandato per la fase 2, caratterizzando al contempo la sicurezza, l’efficacia preliminare e le caratteristiche farmacocinetiche.
PYNNACLE è stato condotto come studio clinico multicentrico di fase 1-2, a gruppo singolo. La fase 1 includeva l’aumento della dose, l’ottimizzazione della dose e la valutazione del profilo di sicurezza. Settantasette pazienti hanno ricevuto Rezatapopt con otto livelli di dose crescenti, da 150 mg una volta al giorno a 2.500 mg una volta al giorno, con un’ulteriore coorte che ha ricevuto 1.500 mg due volte al giorno.
L’idoneità richiedeva un tumore solido localmente avanzato o metastatico che ospitasse TP53 Y220C e una malattia progressiva dopo almeno una precedente terapia antitumorale sistemica.
Selezione della dose
La somministrazione di Rezatapopt è avvenuta per via orale in cicli di trattamento continui di 21 giorni. La fase 1 è iniziata con un disegno di aggiustamento accelerato della dose, per poi passare a un approccio basato su un intervallo di probabilità di tossicità modificato dopo la comparsa di un primo evento avverso, correlato al trattamento di grado 2 o superiore.
Non sono stati osservati effetti tossici dose-limitanti nell’aumento della dose da 150 mg a 2.500 mg. Effetti tossici dose-limitanti si sono verificati in due dei 10 pazienti trattati con 1.500 mg due volte al giorno, tra cui un aumento di grado 3 dei livelli di alanina e aspartato aminotransferasi in un paziente e un danno renale acuto di grado 3 in un altro paziente. La dose massima tollerata è stata fissata a 1.500 mg due volte al giorno.
Tumori e risposta p53
Un totale di 71 pazienti presentava una malattia misurabile al basale e almeno una valutazione post-basale. La risposta complessiva è stata del 20% secondo la valutazione dello sperimentatore. Risposte confermate si sono verificate nel carcinoma ovarico, nel carcinoma mammario, nel carcinoma endometriale, nel carcinoma testa-collo, nel carcinoma prostatico e nel carcinoma polmonare a piccole cellule.
Anche la risposta complessiva, valutata da una revisione centrale indipendente in cieco, è stata del 20% e ha incluso due risposte complete. La risposta completa è stata definita come scomparsa di tutte le lesioni target e non target senza sviluppo di nuove lesioni.
Una risposta completa si è verificata in una paziente con carcinoma polmonare a piccole cellule che ha ricevuto 1.150 mg una volta al giorno. Un’altra risposta completa si è verificata in una paziente con carcinoma ovarico che ha ricevuto 1.500 mg due volte al giorno.
Il tempo mediano alla risposta è stato di 1,4 mesi. La durata mediana della risposta è stata di 7 mesi. La sopravvivenza libera da progressione è stata di 4,3 mesi. La sopravvivenza globale è stata di 11,4 mesi.
Tutti i 14 pazienti con una risposta valutata dallo sperimentatore presentavano tumori che presentavano la variante TP53 Y220C e KRAS wild-type. La risposta complessiva è stata del 30% tra i pazienti valutabili per l’efficacia con TP53 Y220C e KRAS wild-type. Non si sono verificate risposte confermate tra i pazienti i cui tumori presentavano una variante a singolo nucleotide di KRAS, un risultato che potrebbe avere implicazioni per il target futuro.
I dati sul DNA tumorale circolante erano disponibili per 41 pazienti. Una riduzione rispetto al basale della frequenza dell’allele variante Y220C di TP53 all’inizio del ciclo di trattamento 2 o 3 si è verificata in 39 pazienti su 41, pari al 95%. Una riduzione del 50% o superiore si è verificata in 32 pazienti, pari al 78%. Una riduzione del 95% o superiore si è verificata in 16 pazienti, pari al 39%. Una riduzione rispetto al basale si è verificata in tutti i 14 pazienti con una risposta parziale. Questi risultati suggeriscono un’attività farmacologica mirata.
Leggi anche:Il ruolo architettonico di p53 nello sviluppo del cancro
Sicurezza
Eventi avversi (di ogni tipo) si sono verificati in 76 pazienti su 77, ovvero nel 99%. Gli eventi avversi più comuni includevano nausea nel 58% dei casi, vomito nel 44%, aumento del livello di creatinina nel sangue nel 39%, affaticamento nel 39% e anemia nel 36%. L’anemia ha rappresentato l’evento avverso di grado 3 o superiore più comune durante il periodo di trattamento, con una percentuale del 16%.
Si sono verificati eventi avversi correlati al trattamento in 67 pazienti, ovvero l’87%. Eventi avversi correlati al trattamento di grado 1 o 2 si sono verificati in 48 pazienti, ovvero il 62%. L’interruzione dovuta a un evento avverso correlato al trattamento si è verificata in due pazienti, ovvero il 3%, tra cui un aumento del livello di creatinina nel sangue di grado 2 in un paziente e una trombocitopenia immune di grado 4 in un paziente.
Meglio con il cibo
Il cibo ha influenzato l’esposizione e la tollerabilità gastrointestinale. La concentrazione plasmatica è risultata circa il 30% più elevata a 2.000 mg con il cibo rispetto all’assenza di cibo, e l’area media sotto la curva concentrazione-tempo durante il ciclo di trattamento è risultata circa il 40% più elevata con il cibo rispetto all’assenza di cibo.
Anche gli eventi avversi gastrointestinali sono stati segnalati come meno frequenti quando il Rezatapopt veniva assunto con il cibo e la maggior parte degli eventi avversi gastrointestinali si è risolta con il trattamento dei sintomi o con l’interruzione del trattamento.
L’attività antitumorale su diversi tipi di tumore ha fornito la prova di fattibilità per la riattivazione farmacologica diretta di p53 nei tumori solidi con TP53 Y220C. Sebbene la variante Y220C presa di mira nello studio implichi che i risultati siano specifici per TP53 con una particolare alterazione, i risultati dimostrano che p53 mutante può essere riattivato nei pazienti, risvegliando il “Guardiano del Genoma” dell’organismo.
Fonte: New England Journal of Medicine