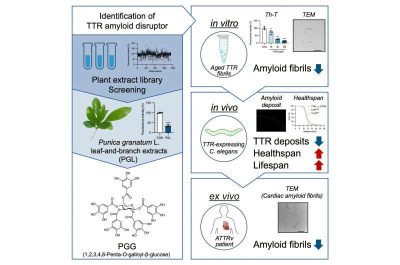
Amiloidosi da transtiretina-immagine: ricercatori hanno identificato un composto bioattivo chiamato PGG (1,2,3,4,6-penta-O-galloil-β-D-glucosio) da estratti di foglie e rami di melograno (Punica granatum) attraverso lo screening di una libreria vegetale. Crediti: Kagami A. et al., “Glycosidic scaffold bearing multiple galloyl moieties from pomegranate disrupts transthyretin amyloids”, iScience (2026). Concesso in licenza con licenza CC BY 4.0.
L’amiloidosi da transtiretina (ATTR) è una malattia rara, progressiva e talvolta fatale, causata dall’accumulo di depositi di amiloide (proteina transtiretina mal ripiegata) in organi come cuore e nervi. Può essere ereditaria (hATTR) o di tipo wild-type (wtATTR), spesso causando scompenso cardiaco, neuropatia periferica e sindrome del tunnel carpale.
Un team di ricerca dell’Università di Kumamoto ha scoperto che un composto naturale presente nelle foglie e nei rami del melograno può scomporre direttamente gli aggregati proteici dannosi legati all’amiloidosi da transtiretina (TTR), una malattia progressiva e potenzialmente letale che colpisce i nervi e il cuore.
Lo studio, pubblicato su iScience, identifica l’1,2,3,4,6-penta-O-galloil-β-D-glucosio (PGG) come un potente “disgregatore dell’amiloide”. L’amiloidosi da TTR si verifica quando la proteina di trasporto transtiretina si ripiega in modo anomalo e si accumula sotto forma di fibrille amiloidi insolubili negli organi. I trattamenti esistenti agiscono principalmente stabilizzando la proteina normale o riducendone la produzione, ma sono meno efficaci una volta che i depositi di amiloide si sono già formati.
Per rispondere a questa esigenza insoddisfatta, i ricercatori hanno analizzato 1.509 estratti vegetali da una banca dati di prodotti naturali. Gli estratti derivati da foglie e rami di melograno (Punica granatum) hanno mostrato un’attività particolarmente efficace nel distruggere le fibrille amiloidi TTR preformate. Ulteriori analisi chimiche hanno individuato il PGG come componente attivo.
Esperimenti di laboratorio hanno dimostrato che il PGG ha efficacemente disassemblato le fibrille amiloidi formate sia dalla TTR mutante che da quella selvatica. È importante notare che, nelle stesse condizioni, ha preso di mira selettivamente gli aggregati di TTR senza distruggere le fibrille beta-amiloidi associate al morbo di Alzheimer, suggerendo un certo grado di specificità molecolare.
Il team ha anche testato il PGG in un modello di nematode (C. elegans) che esprime frammenti di TTR umana. Il trattamento ha ridotto i depositi proteici e prolungato significativamente sia la durata della vita che quella della salute. Inoltre, il PGG ha distrutto con successo le fibrille amiloidi isolate dal tessuto cardiaco di un paziente con amiloidosi ereditaria da TTR, evidenziandone la potenziale rilevanza clinica.
Leggi anche:Amiloidosi da transtiretina: biopsia cutanea può rilevare la rara malattia neurodegenerativa
Analisi strutturali hanno inoltre rivelato che molteplici gruppi galloile legati a un nucleo di glucosio sono essenziali per l’attività, fornendo informazioni su come il composto interagisce con le fibrille amiloidi a livello molecolare.
Sebbene siano necessari ulteriori studi per valutare la sicurezza e l’efficacia negli esseri umani, i risultati suggeriscono che le molecole derivate dalle piante come il PGG potrebbero fungere da promettenti composti guida per le terapie di nuova generazione che rimuovono attivamente i depositi di amiloide patogeni, rispondendo a un’importante esigenza insoddisfatta nel trattamento dell’amiloidosi TTR.
Fonte: iScience