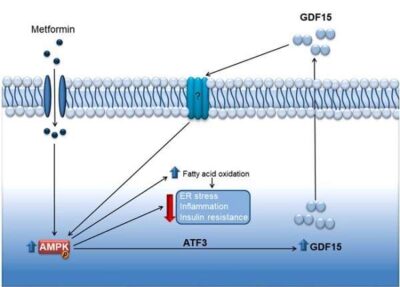
Metformina-Immagine:lo studio identifica la citochina GDF15, una proteina la cui espressione aumenta in risposta allo stress cellulare, come un fattore chiave affinché il farmaco metformina mostri effetti antidiabetici. Credito: Phsrmacological Research.
La metformina, il farmaco più prescritto per il trattamento del diabete mellito, noto come diabete di tipo 2, richiede la presenza del fattore di differenziazione della crescita 15 (GDF15), una proteina la cui espressione aumenta in risposta allo stress cellulare, per ottenere i suoi effetti antidiabetici.
Questa scoperta è merito di uno studio condotto dal gruppo di ricerca del Diabetes and Associated Metabolic Diseases Networking Biomedical Research Center (CIBERDEM) dell’Università di Barcellona (UB) e dell’Istituto di ricerca Sant Joan de Déu (IRSJD), che ha incluso la partecipazione di un team dell’Istituto di ricerca biomedica Alberto Sols (CSIC/UAM).
Lo studio, pubblicato sulla rivista Pharmacological Research, rivela un nuovo meccanismo attraverso il quale la regolazione positiva della citochina GDF15 coinvolta nella risposta allo stress cellulare, attiva un sensore metabolico (AMPK) che è fondamentale nel bilancio energetico. Lo studio mostra anche che l’azione di GDF15 è indipendente dall’attivazione dei suoi recettori situati nel sistema nervoso centrale, gli unici finora conosciuti, il che suggerisce l’esistenza di nuove azioni di questa citochina mediate dai recettori periferici da determinare.
Il diabete di tipo 2 è un disturbo metabolico complesso caratterizzato principalmente da una quantità eccessiva di glucosio nel sangue dovuta all’incapacità dell’organismo di rispondere adeguatamente all’azione dell’insulina, un processo noto come insulino-resistenza o di produrre questo ormone. Durante lo sviluppo di questa patologia si verifica uno stress cellulare, che provoca un aumento della secrezione di citochine in risposta a questo processo – come GDF15 – che attivano meccanismi per contrastare processi come l’infiammazione o l’insulino-resistenza.
Sebbene la metformina sia il farmaco più utilizzato nel trattamento del diabete di tipo 2, i meccanismi responsabili degli effetti antidiabetici non sono completamente compresi. Per questo motivo, questo studio mira a determinare se l’azione della metformina dipende dalla proteina di risposta allo stress GDF15, secondo il Professor Manuel Vázquez-Carrera, capo del gruppo CIBERDEM presso la Facoltà di Farmacia e Scienze dell’Alimentazione e l’UB Institute of Biomedicine (IBUB) e coordinatore dello studio.
“GDF15 è una citochina di risposta allo stress cellulare, con livelli aumentati in molte malattie, come insufficienza cardiaca, cancro, fegato grasso e diabete, che è stata presentata come un potenziale biomarcatore di molte malattie e in questo studio specifico, abbiamo studiato la sua partecipazione all’attivazione di AMPK da parte della metformina“, osserva il ricercatore.
Ángela M. Valverde, capo del gruppo CIBERDEM presso l’Istituto di ricerca biomedica Alberto Sols (CSIC/UAM) e coautore dello studio, afferma che “i nostri risultati suggeriscono che l’attivazione di AMPK da parte della metformina aumenta i livelli di GDF15 e, allo stesso tempo, questa citochina contribuisce a mantenere l’attività dell’AMPK.”
Uno studio su topi selvatici con e senza la citochina GDF15
Per raggiungere queste conclusioni, i ricercatori hanno utilizzato topi selvatici che esprimono GDF15 e altri topi senza questa citochina. Dopo aver causato obesità e diabete di tipo 2 in questi topi alimentandoli con una dieta ricca di grassi, hanno osservato che l‘effetto antidiabetico causato dalla metformina nei topi selvatici scompariva nei topi senza GDF15.
Inoltre, l’attivazione dell’AMPK causata dalla metformina nel fegato e nei muscoli dei topi selvatici era assente anche nei topi che non esprimevano GDF15.
Spiegano gli autori:
“La metformina è il farmaco più prescritto per il trattamento del diabete mellito di tipo 2, a causa del suo effetto ipoglicemizzante, che si verifica principalmente attraverso l’inibizione della produzione epatica di glucosio. Tuttavia, il suo preciso meccanismo d’azione rimane solo parzialmente noto. La metformina non viene metabolizzata e, di conseguenza, i suoi tessuti bersaglio sono identificati dall’assorbimento cellulare e dall’accumulo del farmaco. Nei topi a cui sono state somministrate dosi terapeutiche di metformina per via orale (100-300 mg/kg/giorno), il farmaco viene assorbito e trasportato dalla vena porta al fegato, dove si accumula, raggiungendo concentrazioni fino a 1 mM. Nel fegato, la metformina attenua la produzione epatica di glucosio inibendo la glicerolo-3-fosfato deidrogenasi mitocondriale e attivando la proteina chinasi attivata da AMP (AMPK), che inibisce l’espressione dei geni gluconeogenici. Mentre le concentrazioni farmacologiche di metformina attivano direttamente l’AMPK nel fegato promuovendo la formazione del complesso eterotrimerico di questa chinasi e attraverso la fosforilazione. Sebbene il fegato sia considerato l’organo bersaglio primario per gli effetti ipoglicemizzanti della metformina, gli effetti benefici di questo farmaco antidiabetico sono stati estesi ad altri organi, inclusi intestino, reni e muscoli. Anche il muscolo scheletrico, che rappresenta la maggior parte dell’uso di glucosio stimolato dall’insulina, assorbe e accumula metformina. Ciò è coerente con l’attivazione segnalata di AMPK da parte della metformina nel muscolo scheletrico di pazienti con diabete di tipo 2.
Nel 2017, uno studio clinico ha rivelato che la metformina ha aumentato i livelli sierici del fattore di differenziazione della crescita 15 (GDF15), un membro divergente della superfamiglia del fattore di crescita trasformante β (TGFβ), in modo dose-dipendente, rendendolo un biomarcatore adatto per la risposta a questo farmaco. Più recentemente, due studi hanno riportato che l’aumento dei livelli di GDF15 causato dalla metformina è stato mediato dalla sovraregolazione della proteina omologa C/EBP (CHOP), fornendo un nuovo meccanismo mediante il quale la metformina riduce il peso corporeo. Infatti, GDF15 è una citochina di risposta allo stress che regola l’appetito e il metabolismo, influenzando così l’obesità, il diabete e la steatosi epatica non alcolica (NAFLD). Inizialmente, è stato proposto che i recettori TGFβ mediassero gli effetti GDF15, ma è stata poi documentata la mancanza di legame di questa citochina a questi recettori, il che ha portato a esplorare altri recettori. La presenza di contaminazione da TGFβ nei primi lotti purificati di GDF15 da colture di cellule di mammifero potrebbe aver influenzato l’interpretazione di alcuni studi in vitro. Studi più recenti hanno dimostrato che GDF15 segnala attraverso il recettore α-simile (GFRAL) della famiglia del fattore neurotrofico derivato dalla linea cellulare gliale (GDNF) nel rombencefalo. L’aumento di GDF15 indotto dalla metformina sopprime l’appetito e promuove la perdita di peso attraverso GFRAL. Tuttavia, alcuni studi recenti indicano che l’effetto anoressizzante del GDF15 esogeno somministrato tramite GFRAL si verifica solo a dosi farmacologiche elevate, mentre gli aumenti fisiologici (2-3 volte) dei livelli di GDF15 endogeni (valori basali di ~ 50 pg/mL nei topi) non non sopprimere l’assunzione acuta di cibo. Infatti, una dose di GDF15 di 20 µg/kg ha portato a livelli sierici di questa citochina di ~1500 pg/mL che hanno ridotto l’assunzione di cibo, mentre una dose inferiore di GDF15 di 2 µg/kg non ha avuto alcun effetto sull’assunzione di cibo in nessuno dei punti temporali studiati. Inoltre, abbiamo recentemente riportato che GDF15 attiva AMPK in miotubi in coltura e muscolo scheletrico isolato che non esprimono GFRAL, suggerendo così la segnalazione GDF15 indipendente da GFRAL nelle cellule muscolari. In questo lavoro, abbiamo esaminato se l’aumento di GDF15 causato dalla metformina contribuisce all’attivazione di AMPK indipendentemente da GFRAL”.
Per escludere il coinvolgimento dei recettori centrali di GDF15 nei cambiamenti causati da GDF15, i ricercatori hanno utilizzato colture cellulari di epatociti e cellule muscolari in quelle su cui la riduzione del GDF15 ha attenuato l’aumento dell’attività dell’AMPK causato dalla metformina, il che ha suggerito che gli effetti della metformina su AMPK erano indipendenti dal sistema nervoso centrale.
Fonte:Pharmacological Research