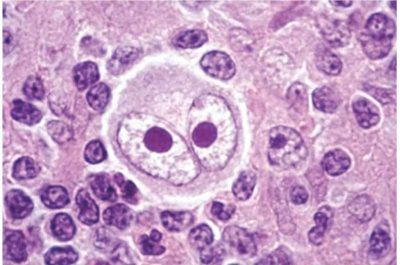
Linfoma di Hodgkin-immagine: le cellule di Reed-Sternberg, spesso descritte come aventi un aspetto a “occhi di gufo” con due nuclei, sono un segno distintivo del linfoma di Hodgkin. Queste cellule maligne si trovano nei linfonodi delle persone affette da questo tumore. Fonte: National Cancer Institute
Per la prima volta, i ricercatori del Weill Cornell Medicine hanno dimostrato che le cellule tumorali del linfoma di Hodgkin prelevate da campioni di pazienti sono cellule immunitarie bloccate in una “crisi d’identità”. Normalmente, una cellula B matura in una plasmacellula che produce anticorpi per combattere le infezioni, ma in questo caso le cellule rimangono intrappolate a metà della transizione. Disattivano le caratteristiche chiave delle cellule B, ma non maturano mai completamente in plasmacellule funzionali, sopravvivendo invece come cellule maligne del linfoma di Hodgkin, chiamate anche cellule di Reed-Sternberg.
Il linfoma di Hodgkin è il tumore più comune negli adolescenti di età compresa tra i 15 e i 19 anni e colpisce anche persone di età superiore ai 55 anni. Tipicamente causa un ingrossamento dei linfonodi del collo, del torace, delle ascelle o dell’inguine, e richiede chemioterapia e radioterapia nei casi avanzati.
I risultati, pubblicati il 22 aprile sul Blood Cancer Journal, ridefiniscono il linfoma di Hodgkin come un tumore derivante da un’anomala crescita cellulare, piuttosto che da una semplice crescita incontrollata, e suggeriscono nuovi biomarcatori diagnostici per distinguerlo da altri linfomi non-Hodgkin correlati.
“Si riteneva che le cellule del linfoma di Hodgkin avessero origine da cellule B che, nel centro germinativo, stavano sviluppando la capacità di produrre immunoglobuline”, ha affermato la Dr.ssa Ethel Cesarman, Prof.ssa di patologia e medicina di laboratorio e membro del Sandra and Edward Meyer Cancer Center del Weill Cornell, che ha co-diretto questa ricerca. “In questo studio, ora vediamo che queste cellule erano sulla via della differenziazione in plasmacellule, ma questo processo è stato interrotto perché non sono in grado di produrre immunoglobuline, come fanno le normali plasmacellule“.
La Dr.ssa Lisa Giulino-Roth, direttrice della Divisione di Ematologia-Oncologia Pediatrica presso la New York University Langonne, precedentemente in servizio presso il Weill Cornell, ha co-diretto la ricerca. Il Dottor Mikhail Roshal, patologo presso il Memorial Sloan Kettering Cancer Center, e la dottoressa Isabella Kong, ricercatrice post-dottorato in Pediatria presso il Weill Cornell, sono i primi autori dell’articolo.
Eludere il sistema immunitario
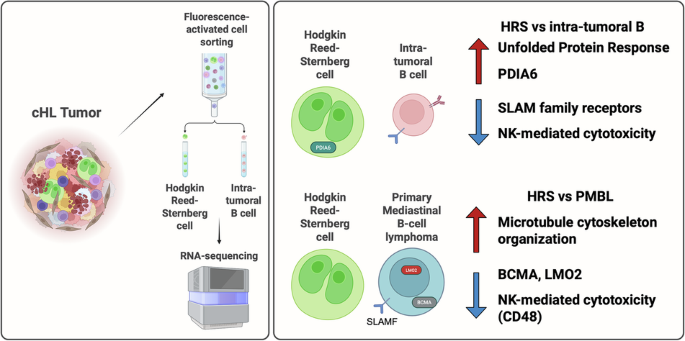
Per comprendere le origini delle cellule del linfoma di Hodgkin, il team ha analizzato i profili di espressione genica di 18 tumori primari e quattro linee cellulari. I ricercatori hanno confrontato i dati del linfoma di Hodgkin con quelli di un raro linfoma chiamato linfoma primario mediastinico a cellule B (PMBL), che ha una connessione con le cellule B e si sviluppa nella stessa sede del corpo. Il team ha notato che i due linfomi esprimono set di geni diversi, con le cellule del linfoma di Hodgkin che assomigliano maggiormente al mieloma multiplo, un tumore delle plasmacellule, rispetto ad altri linfomi.
“Le cellule del linfoma di Hodgkin riducono l’espressione di alcune proteine, quindi non sono più simili alle cellule B“, ha affermato il Dottor Kong. “Inoltre, aumentano l’espressione di altre proteine per assomigliare maggiormente alle plasmacellule, pur non svolgendo completamente la loro funzione”. Ad esempio, il team ha scoperto che i geni del pathway della risposta alle proteine mal ripiegate (UPR) erano insolitamente attivi nelle cellule del linfoma di Hodgkin.
La risposta UPR aiuta le plasmacellule a gestire lo stress derivante dalla produzione di grandi quantità di immunoglobuline per combattere le infezioni. Poiché le cellule del linfoma di Hodgkin non sono in grado di produrre questi anticorpi, sono sottoposte a una costante tensione interna e potrebbero utilizzare questa risposta allo stress come meccanismo di sopravvivenza.
Lo studio ha anche mostrato un nuovo meccanismo con cui le cellule del linfoma di Hodgkin eludono il riconoscimento da parte del sistema immunitario. Normalmente, le cellule natural killer (NK), parte del sistema immunitario innato, sono sentinelle a risposta rapida che scansionano le cellule alla ricerca di specifici “marcatori” di superficie che segnalano loro di attaccare. Le cellule del linfoma di Hodgkin riducono l’espressione di una serie di marcatori chiamati ligandi della famiglia SLAM, tra cui il CD48, in modo che le cellule NK non riconoscano il tumore come una minaccia e non sferrino un attacco efficace. I ricercatori hanno anche scoperto che il tumore stesso presentava un numero inferiore di cellule NK, suggerendo che le cellule cancerose potrebbero attivamente escluderle o respingerle dal sito tumorale.
Leggi anche:Linfoma di Hodgkin: prognosi monitorata con DNA tumorale circolante
Queste cellule tumorali eludono anche i linfociti T, parte della risposta immunitaria adattativa, attraverso altri meccanismi, in modo che il tumore possa sfuggire a entrambi i principali rami della sorveglianza immunitaria.
Questi risultati potrebbero portare all’identificazione di nuovi marcatori diagnostici che aiuterebbero i medici a distinguere il linfoma di Hodgkin da altri tumori con sintomi simili. Ad esempio, la presenza della proteina PDIA6 potrebbe indicare un linfoma di Hodgkin poiché è coinvolta nella risposta UPR ed è specificamente sovraregolata in queste cellule.
Astratto
“Il linfoma di Hodgkin classico (cHL) condivide mutazioni con il linfoma primario a cellule B mediastinico (PMBL), ma se ne differenzia per istologia, comportamento clinico e fenotipo. Per definire i programmi trascrizionali alla base di queste differenze, abbiamo eseguito un’analisi di citometria a flusso e un sequenziamento dell’RNA a basso input di cellule di Hodgkin e Reed-Sternberg (HRS) provenienti da diciotto tumori primari, cellule B intratumorali appaiate e quattro linee cellulari di cHL, confrontandole con i dati di sequenziamento dell’RNA di 40 casi di PMBL. La profilazione trascrittomica ha rivelato che le cellule HRS subiscono una differenziazione abortiva in plasmacellule con una robusta attivazione della risposta alle proteine mal ripiegate (UPR), una caratteristica condivisa con il mieloma multiplo ma assente nel linfoma diffuso a grandi cellule B e nel PMBL. Le cellule HRS hanno anche dimostrato una profonda evasione immunitaria, inclusa la soppressione dei geni dell’identità delle cellule B e la perdita del riconoscimento da parte delle cellule natural killer attraverso la down-regolazione dei ligandi della famiglia SLAM come CD48. L’analisi comparativa con PMBL ha evidenziato programmi oncogenici condivisi e distinzioni chiave: le cellule HRS hanno mostrato una maggiore perdita di identità delle cellule B, assenza di marcatori delle cellule GCB e delle plasmacellule e una singolare sovraregolazione delle vie citoscheletriche e mitotiche coerente con la loro morfologia multinucleata. Questi risultati identificano le cellule HRS come cellule GCB differenziate in modo aberrante con caratteristiche plasmacellulari parziali, attivazione della risposta UPR e distinte strategie di evasione immunitaria”.
“In definitiva, abbiamo bisogno di trattamenti più mirati rispetto alla chemioterapia, che ha effetti collaterali a lungo termine”, ha affermato il Dottor Cesarman, che è anche patologo presso il NewYork-Presbyterian/Weill Cornell Medical Center. “Potrebbero esserci modi per colpire selettivamente la UPR e aiutare i pazienti“.
Fonte: Blood Cancer Journal