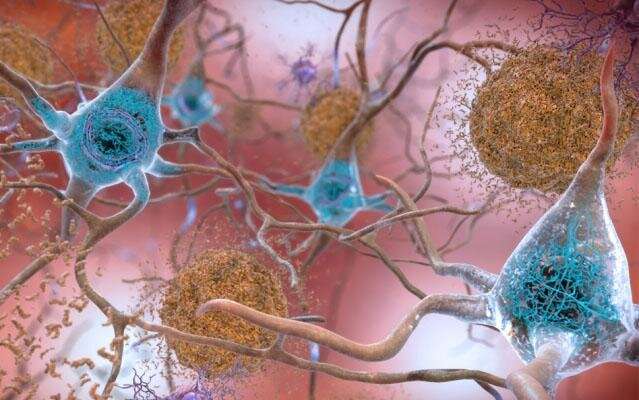
Immagini, nei cervelli affetti dalla malattia di Alzheimer, livelli anomali della proteina beta-amiloide si aggregano per formare placche ( in marrone) che si accumulano tra i neuroni e interrompono la funzione cellulare. Accumuli anormali della proteina tau formano grovigli (visti in blu) all’interno dei neuroni, danneggiando la comunicazione sinaptica tra le cellule nervose. Credito: National Institute on Aging, NIH.
Tra le sfide della diagnosi e del trattamento della malattia di Alzheimer (AD) c’è il fatto che i pazienti con versioni asintomatiche e sintomatiche della condizione degenerativa possono condividere oneri neuropatologici simili, ma sperimentare tassi significativamente diversi di declino cognitivo.
In un nuovo studio, pubblicato il 23 luglio 2019 su Cell Reports, un team guidato da ricercatori della School of Medicine dell’Università di California di San Diego ha utilizzato il trascrittoma, la somma di tutte le molecole di RNA messaggero (mRNA) espresse dai geni, per confrontare 414 studi su partecipanti con AD diagnosticato clinicamente e neuropatologicamente confermato con un gruppo di controllo.
Vedi anche, Il ruolo della barriera emato-encefalica nella prevenzione dell’ Alzheimer.
I loro risultati suggeriscono che l’integrazione delle interazioni proteiche con le perturbazioni geniche può generare un quadro completo per la caratterizzazione delle alterazioni nella rete molecolare correlata all’AD.
Mentre l’AD familiare ha un forte fattore genetico, le cause dell’AD sporadico (la forma più comune) sono molteplici e non completamente note. I fattori di rischio primari comprendono l’età, il genere e la storia familiare, ma includono anche una varietà di fattori biologici, psicologici e sociali.
Molte ricerche si sono concentrate su due elementi chiave della patologia dell’AD: l’accumulo di placche proteiche amiloidi e grovigli anomali di proteine neurofibrillari tau nel cervello, che si pensa causino disfunzione e morte dei neuroni. Ma gli scienziati riconoscono sempre più la rilevanza e l’importanza di altri fattori, come l’infiammazione, i problemi di circolazione sanguigna e l’atrofia cerebrale, tutti “correlati con i sintomi clinici del declino cognitivo e che hanno portato a cambiamenti nei criteri diagnostici durante l’ultimo decennio”, hanno scritto il autori.
“Il nuovo studio ha combinato analisi di perturbazioni geniche e interazioni proteiche”, ha affermato l’autore senior Robert Rissman, Professore di neuroscienze presso la UC San Diego School of Medicine, Direttore del Biomarker Core per l’Alzheimer’s Disease Cooperative Study (ADCS) e Direttore di Neuropathology / Brain Bank e Biomarker Core per l’UC San Diego Shiley-Marcos Alzheimer Disease Research Center, che alla fine ha identificato gruppi compositi di geni funzionalmente distinti rivelando ampi cambiamenti nei livelli di espressione in AD. Questi cluster corrispondevano ampiamente alla trasmissione sinaptica, al metabolismo, al ciclo cellulare, alla sopravvivenza cellulare e alla risposta immunitaria, tutti gli aspetti critici coinvolti nella patologia dell’AD.
“Uno dei maggiori problemi nella ricerca sull’AD è l’identificazione dei pazienti a rischio al momento giusto”, ha affermato Rissman. “Comprendere le reti geniche che possono cambiare in specifici gruppi di pazienti può aiutare a semplificare gli sforzi di reclutamento delle sperimentazioni cliniche e ridurre i costi e il tempo per arruolare pazienti alle sperimentazioni. Con il campo che si sposta sempre più verso la malattia pre-sintomatica, abbiamo bisogno di espandere la nostra comprensione dei meccanismi molecolari alla base dell’intero spettro della malattia “.
Fonte, Cell Reports