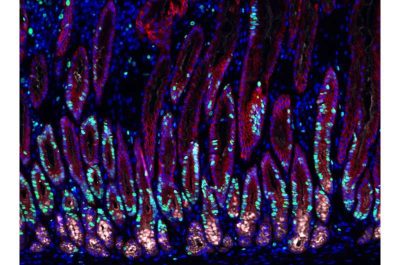
(Helicobacter pylori/ Cancro allo stomaco-Immagine:tessuto dello stomaco infetto da batteri Helicobacter. Le cellule in divisione sono rappresentate in verde, i nuclei cellulari in blu. Credito: Charité | Michele Sigillo).
Quando il batterio Helicobacter pylori infetta lo stomaco, provoca infiammazione gastrica e aumenta il rischio di cancro allo stomaco. Un team di ricercatori della Charité—Universitätsmedizin Berlin e del Max Delbrück Center for Molecular Medicine (MDC) è stato in grado di chiarire i cambiamenti caratteristici che si verificano all’interno delle ghiandole gastriche durante un’infezione da H. pylori.
I ricercatori hanno scoperto un nuovo meccanismo che, limitando la divisione cellulare nel tessuto sano dello stomaco, protegge lo stomaco dai cambiamenti cancerosi. Un’infiammazione dello stomaco, tuttavia, disattiva questo meccanismo, consentendo alle cellule di crescere in modo incontrollato. I risultati dei ricercatori, che sono stati pubblicati su Nature Communications, potrebbero offrire un nuovo obiettivo per il trattamento del cancro allo stomaco.
Colpendo circa la metà della popolazione mondiale, l’Helicobacter pylori è una delle cause più comuni di infezioni batteriche croniche nell’uomo.H. pylori può portare a un’infiammazione dello stomaco (gastrite) e aumentare il rischio di sviluppare un cancro allo stomaco. Poiché il rivestimento protettivo all’interno dello stomaco è costantemente esposto all’acido dello stomaco, deve rigenerarsi completamente ogni poche settimane, pur mantenendo la sua struttura e composizione nonostante l’elevato turnover cellulare.
“Fino ad ora, i ricercatori avevano ipotizzato che un’infezione da Helicobacter causasse danni diretti alle cellule della ghiandola gastrica nel rivestimento dello stomaco e che la patologia gastrica dopo l’infezione fosse semplicemente il risultato di questo processo”, spiega l’ultimo autore dello studio, il Prof. Dr. Michael Sigal . Continua: “In effetti, il nostro team ha ora scoperto che l’infezione interrompe le complesse interazioni tra diversi tipi di cellule e segnali che sono responsabili della stabilità dei tessuti“. Il Prof. Sigal è Professore di oncologia gastrointestinale traslazionale e dirige un gruppo di ricerca indipendente presso il Dipartimento di epatologia e gastroenterologia della Charité e dell’Istituto di biologia dei sistemi medici (BIMSB) di Berlino, che fa parte dell’MDC.
Guidato dal Prof. Sigal e in collaborazione con i colleghi del Max Planck Institute for Infection Biology, il team di ricercatori ha utilizzato modelli murini complessi per osservare i cambiamenti che si verificano all’interno delle ghiandole gastriche. Utilizzando tecnologie di imaging e sequenziamento unicellulari all’avanguardia, i ricercatori sono stati in grado di visualizzare e isolare specifiche cellule della ghiandola gastrica, che hanno poi esaminato in dettaglio. Per ridurre al minimo la necessità di modelli animali, hanno anche sviluppato speciali microstrutture tissutali simili a organi note come organoidi. I ricercatori hanno utilizzato questi stomaci microscopici per ricreare molte delle caratteristiche delle ghiandole gastriche. Questa strategia ha permesso loro di studiare gli effetti di vari segnali sulle cellule staminali che si trovano all’interno delle ghiandole gastriche (e che sono in grado di differenziarsi in molti diversi tipi cellulari).
“Abbiamo scoperto che le ‘cellule stromali’, un tipo di cellula che circonda le ghiandole gastriche, non sono solo responsabili della stabilità meccanica delle ghiandole, come si pensava in precedenza. Al contrario, producono varie molecole di segnalazione che influenzano in modo significativo il comportamento delle cellule della ghiandola“, spiega il Prof. Sigal. Queste sostanze includono le “proteine morfogenetiche ossee” (BMP), che svolgono un ruolo importante nello sviluppo dei tessuti.
I ricercatori sono stati in grado di dimostrare che le cellule stromali che circondano la base della ghiandola inibiscono continuamente la via di segnalazione BMP, stimolando così la proliferazione delle cellule staminali vicine. Al contrario, le cellule stromali sulla superficie della ghiandola sono state trovate per attivare la via di segnalazione, sopprimendo così la proliferazione cellulare. Insieme, questo forma un gradiente di segnalazione che guida il ricambio e la differenziazione delle cellule staminali e funge da base per la stabilità strutturale della ghiandola. L’infezione da Helicobacter provoca il rilascio di sostanze pro-infiammatorie come l’interferone gamma (IFN-γ). Questa citochina infiammatoria interferisce con l’asse di segnalazione BMP, determinando una minore attività di segnalazione BMP e stimolando la proliferazione delle cellule staminali della ghiandola. Ciò si traduce in iperplasia, una lesione precancerosa caratterizzata da ingrossamento dei tessuti.
Vedi anche:Helicobacter pylori: una nanoparticella che contiene acido linoleico uccide i batteri
“I nostri risultati mostrano che una risposta infiammatoria guidata dall’infezione ha effetti molto più pronunciati di quanto si pensasse in precedenza. Oltre ai loro effetti antimicrobici ben caratterizzati, le sostanze pro-infiammatorie come l’IFN-γ influenzano sia la proliferazione cellulare che il comportamento delle cellule staminali dei tessuti e quindi hanno un impatto diretto sull’omeostasi tissutale. In caso di danno tissutale, può essere utile un aumento della proliferazione cellulare, in quanto favorisce una rapida guarigione. In caso di infiammazione cronica associata a un’infezione da Helicobacter, invece, potrebbe favorire lo sviluppo di lesioni precancerose ”, riassume il Prof. Sigal.
Le vie di segnalazione che regolano le interazioni tra il sistema immunitario e le cellule staminali nello stomaco potrebbero rivelarsi significative anche in altri organi. In quanto tali, rappresentano un nuovo obiettivo terapeutico, sia nella prevenzione del cancro che nella medicina rigenerativa.
Fonte:Nature