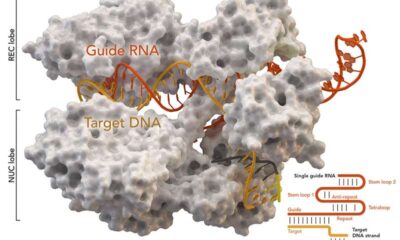
Immagine, proteina associata a CRISPR Cas9 (bianco) dello Staphylococcus aureus basata su Database ID 5AXW. Credit: Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0).
Negli studi preclinici, gli scienziati della Stanford University e i loro collaboratori hanno sfruttato il sistema di modifica genica CRISPR-Cas9 per sostituire il gene mutato alla base di una devastante malattia immunitaria.
Molto raramente, un bambino nasce con una mutazione che rende il suo sistema immunitario sterile, privo di tutte le cellule immunitarie. La malattia, l’immunodeficienza combinata grave legata all’X, o SCID-X1, viene spesso indicata come la malattia del ragazzo bolla, “bubble boy”. Colpisce solo i maschi ed è letale se non trattata, nel primo anno di vita.
Ora, gli scienziati della School of Medicine e i loro collaboratori hanno utilizzato il sistema di modifica genica CRISPR-Cas9 per ideare un nuovo trattamento delle cellule immunitarie nei modelli murini di SCID-X1. Gli scienziati ritengono che il trattamento possa potenzialmente funzionare anche nell’uomo.
SCID-X1 colpisce circa 1 su 50.000 parti di neonati maschi. I bambini con questa malattia soffrono di una mutazione debilitante in un singolo gene , IL2R gamma. Quando questo gene è difettoso, il sistema immunitario non si sviluppa.
Il trattamento standard per i pazienti con SCID-X1 è un trapianto di midollo osseo che fornisce loro cellule staminali che daranno origine a un sistema immunitario funzionante. Ma il processo di trasferimento è complicato e non è garantito il funzionamento. Così, Matthew Porteus, Professore di pediatria, ha avuto una nuova idea: correggere i geni nelle cellule dei pazienti stessi.
Vedi anche, Una nuova ricerca potrebbe perfezionare le forbici genetiche CRISPR.
Attraverso CRISPR-Cas9, Porteus e il suo team hanno fatto proprio questo. Usando campioni di cellule provenienti da persone con SCID-X1, i ricercatori hanno modificato geneticamente la classe delle cellule staminali che danno origine a sangue e cellule immunitarie. Il loro approccio ha indotto il funzionamento del gene.
Ogni topo che ha ricevuto le cellule modificate ha iniziato a generare nuove cellule immunitarie e non ha mostrato effetti collaterali avversi rilevabili.
“A nostra conoscenza, è la prima volta che le cellule umane SCID-X1 modificate con CRISPR-Cas9 sono state utilizzate con successo per produrre le cellule immunitarie umane in un modello animale“, ha detto la studiosa post-dottorato Mara Pavel-Dinu.
Un documento che descrive il lavoro è stato pubblicato online il 9 aprile su Nature Communications. Porteus è l’autore senior e Pavel-Dinu è il primo autore.
Modifica in una soluzione
La terapia basata sul gene per SCID non è nuova. Negli anni ’90, gli scienziati hanno cominciato a dilettarsi in terapie geniche che utilizzavano un virus per fornire un nuovo gene gamma IL2R funzionale. “E’ stato un trattamento molto efficace, ma circa il 25% dei pazienti ha sviluppato una leucemia perché il virus si è integrato in un gene errato“, ha detto Porteus.
L’approccio di Porteus utilizza CRISPR-Cas9 per creare una rottura a doppio filamento nel DNA per inserire una copia sana del gene gamma IL2R nelle cellule staminali che creano le cellule immunitarie.
Usando il sistema di modifica genetica, gli scienziati hanno ottimizzato le cellule di sei persone con SCID-X1 e poi hanno trapiantato quelle cellule in modelli murini di SCID-X1. Quei topi non erano quindi in grado solo di fabbricare le proprie cellule immunitarie, ma molte delle cellule modificate conservavano qualcosa chiamata “stelo”, nel senso che mantenevano la loro capacità di creare continuamente nuove cellule .
“L’idea è che queste cellule staminali modificate daranno origine al sistema sanguigno e al sistema immunitario per l’intera vita del paziente, che speriamo sia di 90 o più anni”, ha detto Porteus. “E abbiamo prove di questo nel nostro studio”.
“Abbiamo dimostrato che questa è una strategia innovativa ed efficace per trattare potenzialmente questa malattia, ma l’altra cosa importante qui è la sicurezza“, ha detto Porteus. “Non vediamo alcuna anomalia nei topi che ricevono il trattamento. In più specificamente, abbiamo anche eseguito un’analisi genetica per vedere se il sistema CRISPR-Cas9 ha creato delle rotture del DNA in luoghi dove non dovrebbe e non abbiamo alcuna prova di ciò. Questo è cruciale”, ha detto Porteus,”perché garantisce che altri geni sani non vengano erroneamente manomessi”.
“La traduzione di queste ricerche di laboratorio in una popolazione di pazienti richiede tempo”, ha detto Porteus che è ottimista sul fatto che se studi più grandi avranno successo, la terapia genica CRISPR-Cas9 potrebbe essere pilotata in pazienti umani nel prossimo anno o due, attraverso il Centro per il Definitivo e Curativo di Stanford Medicina.
Fonte, Nature Communications (2019)