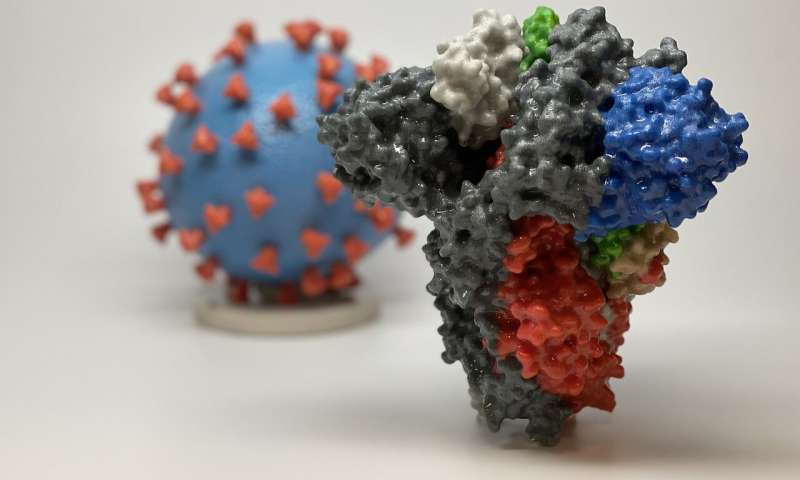
Immagine: stampa 3D di una proteina spike di SARS-CoV-2, il virus che causa COVID-19 – di fronte a una stampa 3D di una particella di virus SARS-CoV-2. La proteina spike (primo piano) consente al virus di entrare e infettare le cellule umane. Sul modello del virus, la superficie del virus (blu) è coperta da proteine spike (rosse) che consentono al virus di entrare e infettare le cellule umane. Credito: NIH.
Cosa rende SARS-CoV-2, il virus che sta dietro COVID-19, una tale minaccia?
Un nuovo studio, guidato da Jose Ordovas-Montanes, Ph.D. al Boston Children’s Hospital e Alex K. Shalek, Ph.D. al MIT, individua i probabili tipi di cellule infettati dal virus. Inaspettatamente, mostra anche che una delle principali difese dell’organismo contro le infezioni virali può effettivamente aiutare il virus a infettare quelle stesse cellule.
I risultati dello studio sono stati pubblicati il 21 aprile dalla rivista Cell.
“Lo studio peer-review, pubblicato come prestampa, aiuterà a focalizzare gli sforzi per capire cosa fa SARS-COV-2 nel corpo, perché alcune persone sono più sensibili e come cercare i trattamenti migliori“, dicono i ricercatori.
Modelli multipli di ricerca
Quando arrivarono le notizie su un nuovo coronavirus in Cina, Ordovas-Montanes e Shalek avevano già studiato diversi tipi di cellule da tutto il sistema respiratorio umano e intestino. Avevano anche raccolto dati da primati e topi. A febbraio hanno iniziato a immergersi in questi dati. “Abbiamo iniziato a esaminare le cellule di tessuti come il rivestimento della cavità nasale, i polmoni e l’intestino, in base ai sintomi riportati e in cui è stato rilevato il virus”, afferma Ordovas-Montanes. “Volevamo fornire le migliori informazioni possibili su tutto il nostro spettro di modelli di ricerca”.
Cellule sensibili a COVID-19
Ricerche recenti hanno scoperto che SARS-CoV-2, come la SARS-CoV strettamente correlata che ha causato la pandemia di SARS, utilizza un recettore chiamato ACE2 per ottenere l’ingresso nelle cellule umane, aiutato da un enzima chiamato TMPRSS2. Ciò ha portato Ordovas-Montanes, Shalek e colleghi a porsi una semplice domanda: quali cellule del tessuto respiratorio e intestinale esprimono sia ACE2 che TMPRSS2?
Per rispondere a questa domanda, il team si è rivolto al sequenziamento dell’RNA a singola cellula, che identifica quali di circa 20.000 geni sono “attivi” nelle singole cellule. Hanno scoperto che solo una piccola percentuale di cellule respiratorie e intestinali umane, spesso ben al di sotto del 10%, produce sia ACE2 che TMPRSS2. Queste cellule si dividono in tre tipi: cellule caliciformi nel naso che secernono muco; cellule polmonari note come pneumociti di tipo II che aiutano a mantenere l’integrità degli alveoli (le sacche in cui viene assorbito l’ossigeno); e un tipo di cosiddetti enterociti che rivestono l’intestino tenue e sono coinvolti nell’assorbimento dei nutrienti.
Vedi anche: Grandi incognite sul virus SARS-CoV-2 complicano il ritorno alla normalità
Il campionamento da primati non umani ha mostrato un modello simile di cellule sensibili.“Molte linee cellulari respiratorie esistenti potrebbero non contenere l’intero mix di tipi di cellule e potrebbero mancare i tipi rilevanti”, osserva Ordovas-Montanes. “Una volta capito quali cellule sono infette, puoi iniziare a chiederti: ‘Come funzionano queste cellule?’ “C’è qualcosa all’interno di queste cellule che è fondamentale per il ciclo di vita del virus?” Con modelli cellulari più raffinati, siamo in grado di eseguire schermate migliori per trovare quali farmaci esistenti colpiscono quella biologia, fornendo un trampolino di lancio per entrare nei topi o nei primati non umani”.
Ma è stata la seconda scoperta dello studio a incuriosire maggiormente gli scienziati. Hanno scoperto che il gene ACE2, che codifica per il recettore utilizzato da SARS-CoV-2 per entrare nelle cellule umane, è stimolato dall’interferone, una delle principali difese dell’organismo quando rileva un virus. L’interferone ha effettivamente attivato il gene ACE2 a livelli più alti, potenzialmente dando al virus nuovi portali per entrare.
“ACE2 è anche fondamentale per proteggere le persone durante vari tipi di lesioni polmonari”, osserva Ordovas-Montanes. “Quando arriva ACE2, di solito è una risposta produttiva. Ma poiché il virus utilizza ACE2 come target, ipotizziamo che potrebbe sfruttare quella normale risposta protettiva. Gli interferoni, infatti, vengono testati come trattamento per COVID-19. Aiuterebbero o farebbero più male che bene? Questo non è ancora chiaro.
“Potrebbe essere che in alcuni pazienti, a causa dei tempi o della dose, l’interferone possa contenere il virus, mentre in altri l’interferone promuove una maggiore infezione”, afferma Ordovas-Montanes. “Vogliamo capire meglio dove si trova l’equilibrio e come possiamo mantenere una risposta antivirale produttiva senza produrre più cellule bersaglio da infettare per il virus”.
ACE-inibitori e tempeste di citochine
I risultati potrebbero anche sollevare nuove linee di indagine sugli ACE-inibitori. Questi farmaci sono comunemente usati per trattare l’ipertensione, che è stata collegata alla più grave malattia COVID-19. Gli ACE-inibitori stanno influenzando il rischio delle persone?
“ACE e ACE2 funzionano nello stesso percorso, ma in realtà hanno proprietà biochimiche diverse“, avverte Ordovas-Montanes. “È una biologia complessa, ma sarà importante comprendere l’impatto degli ACE-inibitori sulla risposta fisiologica delle persone al virus”.
È anche troppo presto per provare a mettere in relazione i risultati dello studio con la “tempesta di citochine”, una risposta infiammatoria in fuga che è stata riportata in pazienti COVID-19 molto malati. Le citochine sono una famiglia di sostanze chimiche che raccolgono le risposte immunitarie del corpo per combattere le infezioni e l’interferone fa parte della famiglia. “Potrebbe essere che stiamo assistendo a una tempesta di citochine a causa di un fallimento dell’interferone nel limitare il virus all’inizio, quindi i polmoni iniziano a chiedere più aiuto. Questo è esattamente ciò che stiamo cercando di capire in questo momento”.
Fonte: Cell