Steatosi epatica-Immagine:astratto grafico Credito: Cell Metabolism (2025).
Uno studio pionieristico pubblicato oggi su Cell Metabolism, illustra in dettaglio come l’ormone FGF21 (fattore di crescita dei fibroblasti 21) possa invertire gli effetti della steatosi epatica nei topi. L’ormone agisce principalmente segnalando al cervello di migliorare la funzionalità epatica.
Il ricercatore Matthew Potthoff, Ph.D., dell’Università dell’Oklahoma è l’autore principale dello studio, che fornisce preziose informazioni sul meccanismo d’azione dell’ormone, bersaglio di una nuova classe di farmaci molto attesi, attualmente in fase 3 di sperimentazione clinica.
La steatosi epatica o MASLD (malattia epatica steatosica associata a disfunzione metabolica), è un accumulo di grasso nel fegato. Può progredire in MASH (steatoepatite associata a disfunzione metabolica), durante la quale può insorgere fibrosi e, in ultima analisi, cirrosi. La MASLD sta diventando un problema molto diffuso negli Stati Uniti, colpendo il 40% della popolazione mondiale, e attualmente esiste un solo trattamento approvato dalla Food and Drug Administration per il trattamento della MASH.
“Una nuova classe di farmaci, basata sulla segnalazione FGF21, sta mostrando buoni benefici terapeutici nelle sperimentazioni cliniche, ma finora il meccanismo del loro funzionamento non era chiaro“, ha affermato Potthoff, Professore di biochimica e fisiologia presso la Facoltà di Medicina dell’Università dell’Oklahoma e viceDirettore dell’OU Health Harold Hamm Diabetes Center.
I risultati dello studio hanno dimostrato che FGF21 è stato efficace nel causare una segnalazione nella specie modello, che ha modificato il metabolismo del fegato. In questo modo, il grasso epatico è stato ridotto e la fibrosi è stata invertita. L’ormone ha anche inviato un segnale separato direttamente al fegato, specificamente per abbassare il colesterolo.
“Si tratta di un ciclo di feedback in cui l’ormone invia un segnale al cervello, e il cervello modifica l’attività nervosa verso il fegato per proteggerlo“, ha affermato Potthoff. “La maggior parte dell’effetto deriva dal segnale al cervello, anziché da una segnalazione diretta al fegato, ma insieme, i due segnali sono potenti nella loro capacità di regolare i diversi tipi di lipidi nel fegato“.
Simile alla famiglia di farmaci dimagranti noti come GLP-1 (peptide 1 simile al glucagone), che contribuiscono a regolare i livelli di zucchero nel sangue e l’appetito, l’FGF21 agisce sul cervello regolando il metabolismo. Inoltre, entrambi sono ormoni prodotti dai tessuti periferici – il GLP-1 dall’intestino e l’FGF21 dal fegato – ed entrambi agiscono inviando un segnale al cervello.
Spiegano gli autori:
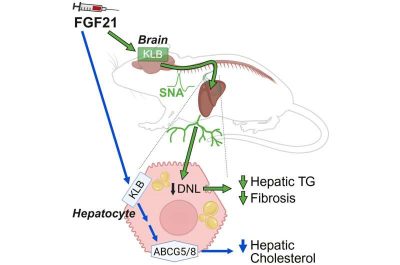
“Il fattore di crescita dei fibroblasti 21 (FGF21) è un’epatochina secreta in risposta a sfide nutrizionali e metaboliche epatiche e regola il metabolismo e l’assunzione di macronutrienti per ripristinare l’omeostasi. I segnali FGF21 sono espressi attraverso un complesso recettoriale costituito da un recettore FGF tradizionale, principalmente FGFR1c e dal co-recettore β-klotho (KLB). L’espressione di KLB è necessaria affinché un tessuto risponda a FGF21 e conferisce specificità per l’azione di FGF21. La somministrazione farmacologica di FGF21 nei roditori ha diversi effetti metabolici. Dopo somministrazione acuta, FGF21 agisce direttamente sui tessuti adiposi per aumentare la sensibilità all’insulina e stimolare l’assorbimento del glucosio. Quando somministrato cronicamente, FGF21 segnala ai neuroni glutammatergici (Vglut2 + ) nel sistema nervoso centrale (SNC) di aumentare il dispendio energetico, ridurre il peso corporeo e, secondariamente, migliorare la sensibilità all’insulina. I livelli di FGF21 sono elevati nel plasma dei roditori e degli esseri umani con MASLD/MASH e i livelli di FGF21 sono correlati alla gravità della fibrosi. I roditori privi di FGF21 endogeno mostrano fenotipi MASH peggiorati, indicando un ruolo protettivo di FGF21 in questo contesto. Inoltre, la somministrazione farmacologica di FGF21 riduce il contenuto di lipidi epatici e inverte il danno agli epatociti nei modelli di MASLD/MASH nei roditori indotti da genetica, tossine e dieta. I risultati preclinici di FGF21 hanno portato allo sviluppo di diversi analoghi di FGF21 a lunga durata che hanno mostrato grande efficacia nel ridurre il contenuto di lipidi epatici e lo stadio di fibrosi negli studi clinici per MASLD e MASH umani. Ad esempio, la somministrazione una volta alla settimana di Efruxifermina, una proteina di fusione bivalente FGF21-Fc, o di pegozafermina, un analogo glicopegilato di FGF21, ha migliorato lo stadio di fibrosi epatica nei pazienti con MASH confermato da biopsia. Tuttavia, i tessuti bersaglio e i meccanismi metabolici alla base di questi effetti rimangono poco chiari. In questo studio, utilizziamo modelli di MASH indotto dalla dieta nei roditori per indagare a fondo l’effetto del trattamento con FGF21 su MASH lieve e avanzato. Utilizzando molteplici modelli genetici, dimostriamo che l’espressione di KLB nei neuroni Vglut2 + è necessaria affinché FGF21 riduca il contenuto di trigliceridi epatici, ma è superflua per le riduzioni dei livelli di colesterolo mediate da FGF21. Al contrario, la segnalazione diretta di FGF21 agli epatociti è responsabile della sua capacità di ridurre i livelli di colesterolo epatico nel MASH indotto dalla dieta. Inoltre, dimostriamo che FGF21 comunica con il fegato attraverso il sistema nervoso centrale per ridurre i livelli di trigliceridi epatici aumentando l’attività del nervo simpatico (SNA) verso il fegato e riducendo la lipogenesi de novo epatica . Insieme, questi risultati chiariscono un asse cervello-fegato che è regolato da FGF21 per ridurre i trigliceridi epatici e invertire MASH“.
Leggi anche: Steatosi epatica non alcolica: scoperto il gene legato allo sviluppo
“È interessante notare che questo ormone/farmaco metabolico agisce principalmente inviando segnali al cervello invece che direttamente al fegato, in questo caso“, ha affermato. “L’FGF21 è piuttosto potente perché non solo ha portato a una riduzione del grasso, ma ha anche mediato l’inversione della fibrosi, che è la parte patologica della malattia e lo ha fatto mentre i topi stavano ancora seguendo una dieta che avrebbe causato la malattia. Ora non solo comprendiamo come funziona l’ormone, ma questa conoscenza potrebbe guidarci nella creazione di terapie ancora più mirate in futuro”.
Fonte: Cell Metabolism