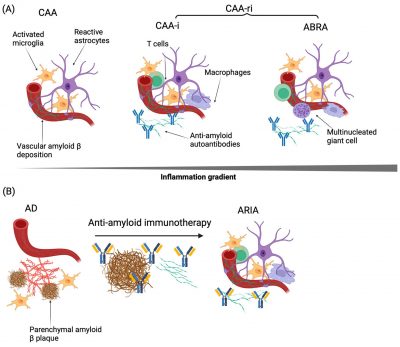
Immunoterapie anti-amiloide-immagine credit mdpi.
Le immunoterapie anti-amiloide sono i primi trattamenti in grado di modificare il decorso della malattia di Alzheimer (AD). Attualmente, due farmaci di questa classe sono approvati dalla Food and Drug Administration (FDA) statunitense: Aducanumab e Lecanemab. Inoltre, il Donanemab ha recentemente dimostrato risultati positivi in uno studio clinico di fase 3. Il meccanismo d’azione di questi farmaci consiste nella rimozione dell’amiloide-β (Aβ) dal cervello mediante anticorpi. In ampi studi clinici, i pazienti trattati con Aducanumab, Lecanemab e Donanemab hanno mostrato una significativa riduzione dell’Aβ e un rallentamento del declino cognitivo. È importante notare che altre immunoterapie anti-amiloide discusse in questa revisione hanno mostrato una riduzione dell’Aβ o una riduzione inferiore alle aspettative e gli studi su questi anticorpi non sono riusciti a dimostrare un beneficio clinico.
Questi risultati suggeriscono che la rimozione dell’Aβ fibrillare dal cervello è un aspetto chiave del meccanismo d’azione degli anticorpi monoclonali anti-amiloide, poiché una significativa riduzione dell’Aβ fibrillare, rilevata tramite tomografia a emissione di positroni (PET) per l’amiloide, si osserva solo con quei farmaci che hanno raggiunto i loro endpoint primari negli studi clinici.
Le immunoterapie anti-amiloide sono state associate ad anomalie di imaging correlate all’amiloide (ARIA), che si presentano in due forme, ARIA-E (edema) e ARIA-H (emorragia), entrambe discusse in dettaglio in questa revisione. Dato che molti pazienti con diagnosi di malattia di Alzheimer presentano fattori di rischio vascolare e patologie cerebrovascolari concomitanti, è fondamentale stabilire se l’uso di antitrombotici e trombolitici sia sicuro nei pazienti sottoposti a immunoterapie anti-amiloide. Sebbene i rischi e i benefici per ogni singolo paziente debbano essere attentamente valutati, questa revisione fornisce una discussione completa dei meccanismi noti delle ARIA, nonché dei dati attualmente disponibili sulla sicurezza di questi farmaci.
Circa il 50% dei pazienti con AD presenta angiopatia amiloide cerebrale (CAA) da moderata a grave [ 12 ], un importante fattore di rischio per ARIA. La CAA, una delle principali cause di emorragia intracerebrale lobare negli anziani, è una malattia dei piccoli vasi cerebrali in cui l’Aβ si deposita all’interno delle pareti dei vasi sanguigni leptomeningei e corticali. È stato ipotizzato che vi sia una significativa sovrapposizione meccanicistica tra ARIA e infiammazione correlata alla CAA (CAA-ri), una condizione in cui i pazienti sviluppano autoanticorpi contro l’Aβ che causano infiammazione cerebrale clinicamente significativa ed eventi emorragici. Inoltre, le immunoterapie anti-amiloide possono esacerbare la deposizione vascolare di Aβ. Le preoccupazioni sulla sicurezza e l’efficacia nei pazienti con una diagnosi clinica di CAA hanno spinto gli esperti del settore a rilasciare una dichiarazione in cui sconsigliavano l’uso off-label di Aducanumab (all’epoca l’unica immunoterapia anti-amiloide approvata dalla FDA) per il trattamento della CAA. Questa revisione discute la sovrapopsizione tra ARIA e CAA, comprese le implicazioni per la prevenzione secondaria dell’ictus ischemico nei pazienti a rischio di ARIA.
2. Definizione delle anomalie di imaging correlate all’amiloide: spunti dagli studi clinici
Le anomalie di imaging sono state costantemente riconosciute come un potenziale effetto avverso dell’immunoterapia anti-amiloide. Il primo riconoscimento di questi eventi avversi è avvenuto durante uno studio di fase 1 sull’immunizzazione attiva con Aβ42 pre-aggregato più adiuvante (AN1792) che ha portato a 18 casi di meningoencefalite. Questi casi presentavano una varietà di anomalie di risonanza magnetica (RM), tra cui iperintensità FLAIR (fluid-attenuated inversion recovery) e potenziamento leptomeningeo.
Le tecniche di RM utilizzate in questo studio potrebbero non essere state sufficientemente sensibili per rilevare le microemorragie, ma tre partecipanti hanno manifestato emorragie cerebrali durante lo studio. Anche le strategie di immunizzazione passiva per l’immunoterapia anti-amiloide sono state associate ad anomalie di imaging. Nello studio di fase 1 sul Bapineuzumab, tre partecipanti che hanno ricevuto la dose più alta hanno sviluppato evidenza di edema vasogenico nella sequenza FLAIR. Uno di questi partecipanti ha anche sviluppato una nuova lesione puntiforme di suscettibilità magnetica sulla sequenza di eco di gradiente (GRE) che si sospettava rappresentasse una microemorragia. Lo sviluppo di edema vasogenico alla risonanza magnetica è stato anche associato al trattamento con Bapineuzumab in uno studio di fase 2.
In risposta a questi eventi avversi, è stata sviluppata una nomenclatura per descriverli. Queste alterazioni della risonanza magnetica associate all’immunoterapia anti-amiloide sono state definite anomalie di imaging correlate all’amiloide (ARIA) e sono suddivise in due fenomeni distinti: ARIA-E (edema), in cui si osservano iperintensità FLAIR nel parenchima cerebrale o nelle leptomeningi, e ARIA-H (emorragia), in cui si osservano depositi di emosiderina sotto forma di microemorragie o siderosi superficiale corticale (cSS) su GRE o imaging pesato per la suscettibilità (SWI).
Nei successivi studi clinici, compresi gli studi di fase 3, l’ARIA è stata osservata costantemente come effetto avverso di diverse immunoterapie anti-amiloide. Sebbene spesso asintomatica, la sindrome ARIA-E può presentare sintomi clinici quali cefalea, confusione, alterazioni della vista, disturbi dell’andatura, deficit neurologici focali e persino la morte. La sindrome ARIA-H è tipicamente asintomatica, ma occasionalmente è associata a emorragia intracerebrale sintomatica; esempi specifici di questi eventi in studi recenti sono discussi più avanti. Nella Tabella 1 è presentato un quadro di riferimento per la classificazione della gravità radiologica della sindrome ARIA. In definitiva, la sindrome ARIA è emersa come un fattore importante da considerare sia nella progettazione degli studi clinici che nella gestione clinica con l’immunoterapia anti-amiloide.

Tabella 1. Classificazione radiografica della gravità ARIA.
Il gruppo di lavoro che ha definito ARIA ha anche proposto raccomandazioni per gli studi clinici, tra cui standard minimi del protocollo MRI, monitoraggio MRI per lo sviluppo di ARIA, lettura e refertazione MRI e risultati di esclusione. Per l’arruolamento dei partecipanti in uno studio di immunoterapia anti-amiloide, è stato raccomandato un cut-off di quattro microemorragie sulla MRI basale per l’esclusione al fine di ridurre il rischio di ARIA-H. È stato raccomandato il monitoraggio di ARIA con MRI regolari, comprese sequenze T2-FLAIR e sensibili all’emosiderina, e l’interruzione della terapia con ARIA-H incidente è stata raccomandata per i partecipanti con sintomi clinici significativi o evidenza di un declino clinico precipitoso. Oltre a queste scansioni di sorveglianza, la risonanza magnetica è raccomandata per i pazienti con sintomi clinici suggestivi di ARIA-E. Affinché i due anticorpi anti-amiloide ricevessero l’approvazione accelerata o completa da parte della Food and Drug Administration (FDA) degli Stati Uniti, Aducanumab e Lecanemab, gli studi clinici di fase 3 escludevano i pazienti con più di quattro microemorragie e/o un riscontro di cSS alla risonanza magnetica.
Sebbene le prove accumulate dagli studi clinici sull’immunoterapia anti-amiloide indichino una relazione causale tra queste terapie e l’ARIA, gli studi condotti su coorti più ampie (in particolare gli studi di fase 3) hanno mostrato evidenze sia di ARIA-E che di ARIA-H nel gruppo placebo, ma generalmente a un tasso inferiore rispetto al gruppo di trattamento.
Fonte: Rivista di Medicina Clinica