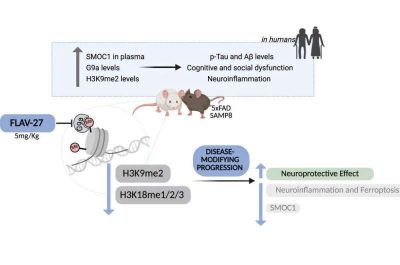
Alzheimer-immagine: abstract grafico. Crediti: Molecular Therapy
Un team dell’Università di Barcellona ha progettato e validato su modelli animali un composto innovativo con un meccanismo d’azione pionieristico per il trattamento della malattia di Alzheimer. A differenza dei farmaci attualmente in uso, che si limitano a rimuovere le placche di beta-amiloide che si accumulano nel cervello, questo nuovo farmaco sperimentale riprogramma l’epigenoma neuronale correggendo le alterazioni nell’espressione genica che contribuiscono alla progressione della malattia.
I risultati di questo studio, pubblicati sulla rivista Molecular Therapy, aprono la strada a una strategia terapeutica basata sull’epigenetica per combattere il morbo di Alzheimer.
“Il composto FLAV-27 rappresenta un approccio innovativo e promettente alla malattia di Alzheimer, con il potenziale di modificarne il decorso, poiché agisce non solo sui sintomi o su un singolo biomarcatore patologico, ma direttamente sui meccanismi molecolari sottostanti“, afferma Aina Bellver, ricercatrice presso l’Istituto di Neuroscienze dell’Università di Buffalo (UBneuro) e prima autrice dell’articolo.
Lo studio è stato condotto dal Professor Christian Griñán e dalla Prof.ssa Mercè Pallàs, della Facoltà di Farmacia e Scienze Alimentari, con la partecipazione di ricercatori di UBneuro e dell’Area CIBER per le Malattie Neurodegenerative (CIBERNED), nonché dell’Istituto di Biomedicina dell’Università di Barcellona (IBUB), dell’Istituto di Nutrizione e Sicurezza Alimentare (INSA-UB), dell’Istituto di Ricerca Biomedica August Pi i Sunyer (IDIBAPS) e di altre istituzioni nazionali e internazionali.
Oltre la proteina beta-amiloide: un nuovo bersaglio epigenetico
I farmaci attualmente approvati per il trattamento dell’Alzheimer, come Lecanemab e Donanemab, sono anticorpi monoclonali che agiscono rimuovendo le placche della proteina beta-amiloide dal cervello.
“Sebbene rappresentino una svolta, la loro efficacia è limitata, in quanto rallentano il declino cognitivo solo del 27-35%, presentano diversi effetti collaterali e agiscono unicamente sulla parte della patologia causata dall’accumulo di beta-amiloide“, spiegano i ricercatori.
Al contrario, FLAV-27 agisce in modo completamente diverso: è il primo inibitore della sua classe ad agire sull’enzima G9a, essenziale nella regolazione epigenetica del cervello, poiché contribuisce a silenziare i geni fondamentali per lo sviluppo neuronale, la plasticità sinaptica e il consolidamento della memoria.
“Inibendo la G9a, il nuovo farmaco impedisce l’accesso della molecola naturale S-adenosilmetionina (SAM), necessaria all’enzima per modificare il DNA. In questo modo, rallenta la disregolazione epigenetica, caratteristica della malattia di Alzheimer, e permette ai neuroni di recuperare la loro normale funzionalità”, affermano gli autori.
Recupero cognitivo funzionale in modelli animali
“Lo studio dimostra che l’inibizione di G9a con FLAV-27 non solo riduce i classici marcatori patologici, come la proteina beta-amiloide e la proteina tau fosforilata, che si accumulano nel cervello delle persone affette da malattia di Alzheimer, ma ripristina anche la funzione cognitiva, il comportamento sociale e la struttura delle sinapsi neuronali in diversi modelli: da test in vitro, passando per il nematode C. elegans – nel quale migliora la mobilità, l’aspettativa di vita e la respirazione mitocondriale – fino a modelli murini di malattia di Alzheimer a esordio tardivo e precoce”.
“In questi modelli, si riscontra un miglioramento della memoria a breve e a lungo termine, della memoria spaziale e della socialità, il che dimostra non solo un effetto sui marcatori molecolari, ma anche un recupero cognitivo funzionale”, sottolineano i ricercatori.
Secondo gli autori, questi risultati confermano che la disregolazione epigenetica – ovvero le alterazioni dei meccanismi chimici che determinano quali geni vengono attivati o meno, senza modificare la sequenza del DNA – non è solo un effetto collaterale della malattia di Alzheimer, ma un meccanismo attivo e controllabile che collega le principali caratteristiche patologiche della malattia, come le proteine beta-amiloide e tau, la neuroinfiammazione e la disfunzione sinaptica, attraverso un asse epigenetico comune.
Questo apre la strada a una nuova categoria di terapie: i trattamenti epigenetici in grado di modificare il decorso della malattia, che potrebbero integrare o addirittura sostituire le strategie attuali, basate esclusivamente sull’eliminazione della proteina beta-amiloide.
Il nuovo composto sperimentale agisce attraverso un meccanismo epigenetico che interviene non solo sui sintomi della malattia, ma direttamente sui meccanismi molecolari che contribuiscono alla sua progressione.
Leggi anche:Alzheimer: esosomi arricchiti con miR-124-3p mostrano un potenziale terapeutico
Biomarcatori ematici per monitorare il trattamento
Un risultato fondamentale che accresce il valore traslazionale di questo trattamento è l‘identificazione di un biomarcatore misurabile sia nel cervello che nel plasma sanguigno dei pazienti.
Il team ha scoperto che il marcatore epigenetico H3K9me2, la proteina SMOC1 e la molecola p-tau181 sono significativamente elevati e che i loro livelli ematici sono direttamente correlati a sintomi quali l’accumulo della proteina tau, la neuroinfiammazione e il grado di deterioramento cognitivo.
Quando FLAV-27 viene somministrato a modelli animali, questi indicatori tornano a livelli normali, parallelamente al recupero cognitivo.
La disponibilità di questi bioindicatori periferici è uno degli aspetti chiave che distingue FLAV-27 dagli altri farmaci in fase di sviluppo.
“Questo studio ha importanti implicazioni per le future sperimentazioni cliniche, in quanto consentirà la selezione di pazienti idonei tramite un semplice esame del sangue, il monitoraggio del trattamento e la dimostrazione che il farmaco modifica effettivamente il suo bersaglio terapeutico“, sottolineano gli autori.
Verso la sperimentazione sull’uomo
Nonostante questi risultati promettenti, FLAV-27 deve ancora superare ulteriori fasi prima che possano iniziare le sperimentazioni cliniche sull’uomo.
Attualmente in fase preclinica avanzata, i prossimi passi includono studi tossicologici regolatori su almeno due specie animali, l’ottenimento della forma farmaceutica e la preparazione del dossier regolatorio per richiedere l’autorizzazione alla sperimentazione clinica alle agenzie competenti, un processo che richiederà anni.
Questa nuova fase sarà guidata da Flavii Therapeutics, una società spin-off dell’UB fondata nel 2025 e detentrice della licenza esclusiva per FLAV-27.
L’azienda si occuperà dello sviluppo preclinico e clinico del farmaco, nonché della gestione della proprietà intellettuale e della raccolta fondi, con l’obiettivo di convertire le conoscenze generate presso l’UB in nuove terapie per le malattie del sistema nervoso centrale come l’Alzheimer.
Fonte: Molecular Therapy