I ricercatori del Baylor College of Medicine hanno scoperto una potenziale nuova strategia per combattere l’Alzheimer e il Parkinson, patologie legate all’accumulo tossico di proteine Tau e alfa-sinucleina nel cervello. Il team riferisce su Nature Communications che la tubulina, l’elemento costitutivo dei microtubuli, i “binari ferroviari” interni della cellula, può impedire a Tau e alfa-sinucleina di formare aggregati tossici, indirizzandoli invece verso il loro normale e sano ruolo.
“Tau e alfa-sinucleina sono ben note per il loro ruolo nelle malattie neurodegenerative come l’Alzheimer e il Parkinson. In queste condizioni, queste proteine possono ripiegarsi in modo anomalo, attaccarsi tra loro e formare aggregati dannosi che danneggiano i neuroni e contribuiscono alla perdita di memoria, ai problemi di movimento e ad altri sintomi“, ha affermato il primo autore dello studio, il Dott. Lathan Lucas, ricercatore post-dottorato di biochimica e farmacologia molecolare nel laboratorio del Dott. Allan Ferreon. “Ma la tau e l’alfa-sinucleina svolgono anche funzioni essenziali nei neuroni sani: aiutano a mantenere la struttura cellulare e supportano la comunicazione interagendo con la tubulina e contribuendo all’assemblaggio e alla stabilizzazione dei microtubuli”.
Per svolgere le loro funzioni cellulari, dannose o salutari, la tau e l’alfa-sinucleina si concentrano in minuscole goccioline chiamate anche condensati. Sebbene prevenire la formazione di queste goccioline sia un potenziale approccio terapeutico per le malattie neurodegenerative, poiché svolgono anche funzioni salutari, la loro interruzione potrebbe alterare la normale funzione neuronale.
“Questo ci ha portato alla seguente idea: cosa succederebbe se invece di impedire la formazione di goccioline, creassimo le condizioni che spingerebbero la tau e l’alfa-sinucleina all’interno delle goccioline verso il loro percorso sano, scoraggiandole dall’intraprendere la strada della malattia?” ha affermato Ferreon, Professore associato di biochimica e farmacologia molecolare e coautore corrispondente del lavoro.
“Penso alla Tau e all’alfa-sinucleina come a dei bambini problematici a scuola. Puoi tenerli in classe senza fargli fare molto, se non recitare o tenerli impegnati con i compiti, lo sport o il teatro, in modo che non si mettano nei guai“, ha detto Lucas. “Abbiamo scoperto che la tubulina può guidare i problematici Tau e alfa-sinucleina verso un percorso sano”.
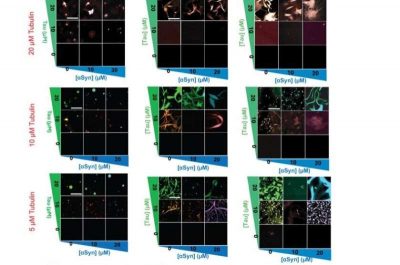
Il team ha lavorato con tecniche biochimiche e biofisiche, microscopia ad alta risoluzione e test neuronali per studiare il ruolo della tubulina nella modulazione e nella prevenzione della formazione di aggregati tossici nelle goccioline.
“Quando i livelli di tubulina sono bassi, come è stato riscontrato nel morbo di Alzheimer, i microtubuli sono meno abbondanti e Tau e alfa-sinucleina possono formare aggregati tossici. Ma quando la tubulina è presente, Tau e alfa-sinucleina si allontanano dagli aggregati dannosi e promuovono invece l’assemblaggio di microtubuli sani“, ha affermato Lucas. “La tubulina reindirizza l’attività di queste proteine, fornendo loro qualcosa di produttivo da fare”.
Leggi anche: Aggregati proteici e invecchiamento
“I nostri risultati modificano significativamente il ruolo della tubulina nella neurodegenerazione, da vittima passiva della malattia a protettore attivo contro l’aggregazione proteica tossica“, ha affermato Ferreon. “Aumentare il pool di tubulina, anziché bloccare la formazione di goccioline, può frenare l’aggregazione tossica preservando al contempo il ruolo benefico di Tau e alfa-sinucleina, offrendo una potenziale strategia terapeutica selettiva”.
Altri collaboratori di questo lavoro sono Phoebe S. Tsoi, co-autore principale, My Diem Quan, Kyoung-Jae Choi e la co-autrice corrispondente Josephine C. Ferreon, tutti del Baylor College of Medicine.
Fonte:Nature Communications