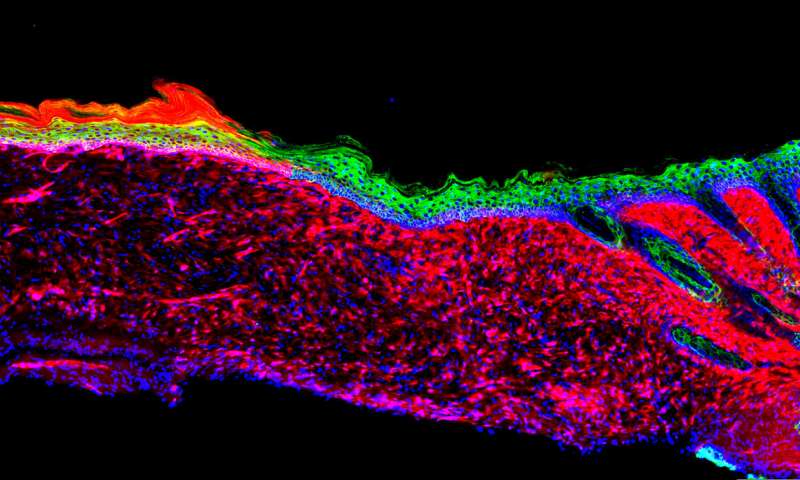
Immagine: l’immagine rappresenta la prima prova di principio per il successo della rigenerazione di un organo funzionale (la pelle) all’interno di un mammifero, mediante una tecnica nota come riprogrammazione in vivo basata su AAV.
La chirurgia plastica per il trattamento di grandi ulcere cutanee, comprese quelle osservate in persone con gravi ustioni, piaghe da decubito o malattie croniche come il diabete, potrebbe essere un ricordo del passato. Gli scienziati del Salk Institute hanno sviluppato una tecnica per convertire direttamente le cellule in una ferita aperta in nuove cellule della pelle. L’approccio si basa sulla riprogrammazione delle cellule a uno stato simile a cellule staminali e potrebbe essere utile per curare il danno alla pelle, contrastando gli effetti dell’invecchiamento e aiutandoci a capire meglio il cancro della pelle.
Le nostre osservazioni costituiscono una prima prova di principio per la rigenerazione in vivo di un intero tessuto tridimensionale come la pelle, non solo i singoli tipi di cellule come precedentemente mostrato”, dice il Professore del Salk, Juan Carlos Izpisua Belmonte, titolare della cattedra Roger Guillemin e autore senior del nuovo documento, pubblicato sulla rivista Nature il 5 settembre 2018. “Questa conoscenza potrebbe non solo essere utile per migliorare la riparazione della pelle, ma potrebbe anche servire a guidare le strategie rigenerative in vivo in altre situazioni patologiche umane, così come durante l’invecchiamento in cui la riparazione dei tessuti è compromessa”.
Le ulcere cutanee – ferite che possono estendersi attraverso più strati della pelle – sono tipicamente trattate chirurgicamente, trapiantando la pelle esistente per coprire la ferita. Tuttavia, quando l’ulcera è particolarmente grande, può essere difficile per i chirurghi innestare una quantità sufficiente di pelle. In questi casi, i ricercatori sono in grado di isolare le cellule staminali della pelle da un paziente, farle crescere in laboratorio e trapiantarle nuovamente nel paziente. Tuttavia, tale procedura richiede una notevole quantità di tempo, che può mettere a rischio la vita del paziente e talvolta non è efficace.
Izpisua Belmonte, in collaborazione con Masakazu Kurita del Salk Research, che ha una formazione in chirurgia plastica, sapeva che un passo fondamentale nel recupero delle ferite era la migrazione o il trapianto di cheratinociti basali nelle ferite. Queste cellule simili a cellule staminali agiscono come precursori dei diversi tipi di cellule della pelle. Ma le ferite grandi e gravi che hanno perso più strati di pelle non hanno più cheratinociti basali. E anche se queste ferite guariscono, le cellule che si moltiplicano nell’area sono principalmente coinvolte nella chiusura della ferita e nell’infiammazione, piuttosto che nella ricostruzione della pelle sana.
Izpisua Belmonte e Kurita volevano convertire direttamente queste altre cellule in cheratinociti basali, senza mai portarli fuori dal corpo. “Abbiamo deciso di creare una pelle dove non esisteva pelle da cui cominciare”, dice Kurita.
I ricercatori hanno prima confrontato i livelli di diverse proteine dei due tipi di cellule (infiammazione e cheratinociti) per avere un’idea di cosa dovevano cambiare per riprogrammare le identità delle cellule. Hanno individuato 55 “fattori di riprogrammazione” (proteine e molecole di RNA) che erano potenzialmente coinvolti nella definizione dell’identità distinta dei cheratinociti basali. Quindi, attraverso prove ed errori e ulteriori esperimenti su ciascun potenziale fattore di riprogrammazione, hanno ridotto l’elenco a quattro fattori che potevano mediare la conversione in cheratinociti basali.
Quando il team ha trattato topicamente le ulcere cutanee sui topi con i quattro fattori, le ulcere hanno sviluppato una pelle sana (nota come epiteli) entro 18 giorni. Nel corso del tempo, gli epiteli si sono espansi e collegati alla pelle circostante anche nelle grandi ulcere. A tre e sei mesi più tardi, le cellule generate si sono comportate come cellule della pelle sane in numerosi test molecolari, genetici e cellulari.
I ricercatori stanno pianificando ulteriori studi per ottimizzare la tecnica e iniziare a testarla in ulteriori modelli di ulcera.
“Prima della sperimentazione clinica, dobbiamo fare ulteriori studi sulla sicurezza a lungo termine del nostro approccio e migliorare l’efficienza il più possibile”, dice Kurita.
Fonte: Nature