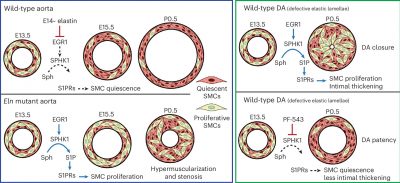
Sindrome di Williams-Beuren-immagine:rappresentazione schematica del modello operativo. Crediti: Nature Cardiovascular Research (2026).
La sindrome di Williams-Beuren è una rara malattia congenita in cui la morbilità e la mortalità principali derivano da ostruzioni, o stenosi, in arterie specifiche. Quando queste ostruzioni coinvolgono l’aorta, si parla di stenosi aortica sopravalvolare. Attualmente, non esistono farmaci per trattare questa condizione. Sebbene l’intervento chirurgico sia un’opzione per alcuni pazienti, non tutti i tipi di stenosi arteriosa possono essere facilmente corretti chirurgicamente. Se non trattata, questa condizione può causare gravi complicazioni cardiovascolari, tra cui l’insufficienza cardiaca congestizia.
Un nuovo studio condotto dalla Yale e pubblicato su Nature Cardiovascular Research, fornisce approfondimenti sullo sviluppo della stenosi aortica sopravalvolare e individua un possibile percorso per contrastare il disturbo.
“La stenosi aortica sopravalvolare è causata da una mutazione genetica che induce gli individui a produrre meno elastina, una proteina che permette ai vasi sanguigni di contrarsi come un elastico”, afferma il Dott. Daniel Greif, Professore di medicina (medicina cardiovascolare) e genetica e autore senior dello studio. “Questa carenza di elastina porta a un eccesso di cellule muscolari lisce e, infine, alla stenosi. Il nostro obiettivo con questo studio era comprendere meglio le cause della proliferazione accelerata delle cellule muscolari lisce, in modo che un giorno possano essere scoperti e utilizzati potenziali trattamenti per questo disturbo“.
In questo studio, i ricercatori del Greif Lab hanno scoperto che un enzima specifico, la sfingosina chinasi 1, causa la proliferazione di cellule muscolari lisce in eccesso. Sebbene precedenti ricerche di Greif e del suo team abbiano identificato altri percorsi alterati dalla carenza di elastina (tra cui il percorso NOTCH3 e il gene dell’integrina β3), i loro risultati più recenti indicano che la sfingosina chinasi 1 viene alterata nelle prime fasi del processo di sviluppo. Modifiche a NOTCH3 e all’integrina β3 si sono osservate in un secondo momento.
“In base alla nostra ricerca, riteniamo che la sfingosina chinasi 1 possa rappresentare un nodo che causa questi altri cambiamenti, rendendola un valido candidato per ulteriori ricerche e, in futuro, un possibile bersaglio terapeutico per aiutare le persone affette dalla sindrome di Williams-Beuren“, afferma Greif.
Leggi anche:Stenosi aortica: identificato potenziale bersaglio terapeutico
Ricerche recentemente pubblicate da altri laboratori hanno dimostrato che questo percorso potrebbe essere rilevante per l’ipertensione polmonare, un’altra condizione caratterizzata anch’essa da un eccesso di muscolatura liscia.
Abstract:
“La carenza di elastina (ELN), il principale componente delle fibre elastiche, porta a un eccesso di cellule muscolari lisce (SMC), che caratterizza le malattie arteriose (ad esempio, la stenosi aortica sopravalvolare (SVAS)) e la chiusura fisiologica del dotto arterioso (DA). Qui dimostriamo che la sfingosina chinasi 1 (SPHK1) è un nodo chiave in questi contesti. Sphk1 è il trascritto più sovraregolato nelle SMC aortiche Eln (−/−) al giorno embrionale 15,5, quando queste cellule sono inizialmente iperproliferative. Anche l’aorta di esseri umani con SVAS sovraregola SPHK1. La riduzione di ELN aumenta i livelli del fattore di trascrizione Early Growth Response 1, con conseguente aumento dei livelli di SPHK1. La delezione di Sphk1 specifica per le SMC o l’inibizione farmacologica di SPHK1 attenua la proliferazione delle SMC e mitiga la malattia aortica. Inoltre, il trattamento con un inibitore di SPHK1 riduce l’accumulo di cellule staminali mesenchimali DA, portando alla pervietà della DA nei topi wild-type. Questi risultati indicano che l’inibizione di SPHK1 può rappresentare una strategia terapeutica per la SVAS e per alcune cardiopatie congenite in cui la DA brevettata mantiene la circolazione“.
“La Williams-Beuren è una malattia rara, quindi non è un’area molto studiata da altri scienziati”, afferma Greif. “Sebbene siano necessarie ulteriori ricerche, riteniamo che questo percorso possa essere importante anche per trattare altri tipi di malattie cardiovascolari più comuni in cui si verifica un eccesso di muscolatura liscia, come l’aterosclerosi o la restenosi coronarica“.