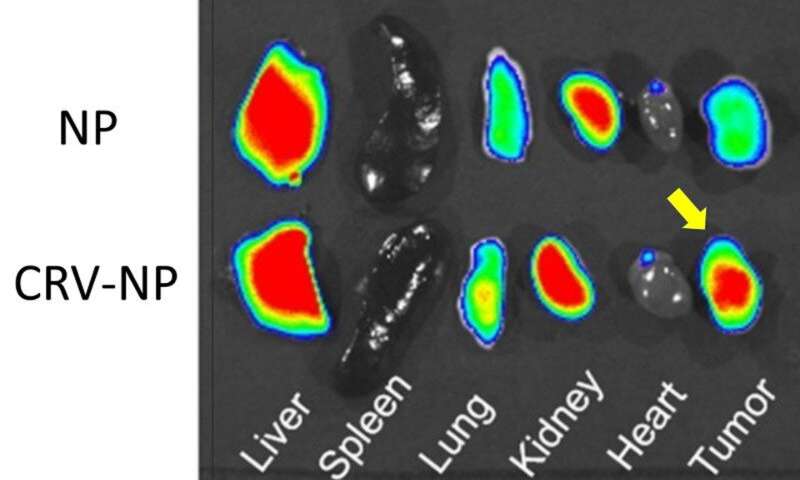
Immagine, una nanoparticella attaccata a CRV (CRV-NP) ospita specificamente i macrofagi nei tumori al seno nei topi (freccia gialla) e non nella milza, polmone o cuore. Le nanoparticelle senza CRV (NP) non si sono accumulate nei tumori. Le sole nanoparticelle attaccate al peptide CRV sono state trovate nel fegato e nei reni perché venivano eliminate dal sistema. Credito: Tang, et al., J Control Release, maggio 2019 / Elsevier.
I macrofagi sono globuli bianchi che si accumulano nei tumori e favoriscono la loro progressione. Ora gli scienziati hanno identificato una proteina di superficie sui macrofagi che risiedono nei tumori e che può essere un obiettivo per trattamenti di precisione.
La maggior parte dei tumori contiene macrofagi, un tipo di cellule immunitarie, che aiutano la crescita tumorale attraverso una serie di meccanismi. I macrofagi associati ai tumori (TAM) agiscono per stimolare la crescita di nuovi vasi sanguigni, rimodellare la matrice extracellulare per promuovere metastasi e migliorare la resistenza ai farmaci.
Nonostante il ruolo dei TAM nel favorire la crescita tumorale a causa della loro alta concentrazione nei tumori, i ricercatori hanno cercato dei modi per sfruttare queste cellule e favorire le terapie tumorali. Una grande barriera per raggiungere questo obiettivo, tuttavia, è come distinguere i TAM dai macrofagi negli organi normali.
Ora, Hongbo Pang, Professore associato del College of Pharmacy dell’Università del Minnesota e i suoi collaboratori, hanno identificato una proteina che si trova solo sulla superficie dei TAM. Questo lavoro, che mira a individuare il target specifico delle terapie tumorali, è riportato nel numero di maggio del Journal of Controlled Release.
“Fornire farmaci ai tumori, evitando l’esposizione ai tessuti sani, è un obiettivo centrale nella cura del cancro”, afferma David Rampulla, Direttore del programma NIBIB “Sistemi di consegna e dispositivi per farmaci e prodotti biologici”.
“Identificare una proteina della superficie cellulare specifica solo per i macrofagi nei tumori e non nei tessuti sani è una scoperta entusiasmante con la reale possibilità di migliorare la specificità e la potenza delle terapie per una vasta gamma di tumori”.
Pang e i suoi colleghi avevano precedentemente usato una tecnica chiamata visualizzazione dei fagi per identificare un marker presente solo sulla superficie dei TAM. La visualizzazione dei fagi comporta l’inserimento di migliaia di pezzi casuali di DNA nei fagi, che sono virus che infettano e crescono nei batteri. Il pezzo di DNA in ciascun fago produce un peptide, un piccolo pezzo di una proteina che viene visualizzato sulla superficie del fagi. Il risultato è una vasta gamma di peptidi casuali sulla superficie dei fagi. I fagi individuati, sono stati esposti a una linea cellulare di macrofagi, che ha portato all’identificazione di un peptide legante i macrofagi chiamato CRV.
In questo studio, il Dr. Pang e il suo team hanno iniettato CRV nei topi che trasportavano una varietà di tipi di tumore. CRV si è legato con successo ai TAM nel tessuto tumorale evitando i tessuti sani circostanti. Per legare i TAM, CRV ha dovuto spostarsi dai vasi sanguigni del tumore al tessuto tumorale stesso, un processo chiamato stravaso. Il rapido stravaso di CRV per raggiungere i TAM è stato un segnale estremamente incoraggiante che questo peptide ha il potenziale per trasportare carichi terapeutici nei tumori solidi.
Il team ha convalidato che CRV si lega a un recettore sulla superficie di TAM chiamato RXRB. Ulteriori analisi hanno confermato che l’RXRB non si trova sulla superficie dei macrofagi negli organi normali ed è quindi un marcatore distinto trovato solo sui TAM.
Per testare l’idea di utilizzare il sistema per fornire farmaci antitumorali, il team ha collegato CRV a una nanoparticella, che potrebbe potenzialmente trasportare farmaci chemioterapici ai TAM. La nanoparticella di CRV è stata iniettata nei topi con tumori mammari. CRV ha migliorato la consegna della nanoparticella nei tumori solidi.
“I risultati dimostrano che abbiamo definito un obiettivo potenzialmente nuovo sui TAM per migliorare la terapia del cancro“, afferma Pang. “Questo apre la possibilità a una serie di terapie che colpiscono i TAM, che vanno dall’erogazione altamente specifica di chemioterapia ai tumori, allo sviluppo di molecole che si legano a TAM e che potrebbero potenzialmente invertire i TAM da promotori di tumori a potenti armi anti-tumorali”.
Fonte, NIH