Neuroinfiammazione-Immagine Credit Public Domain-
I ricercatori della Northwestern Medicine hanno scoperto che specifici canali del calcio aiutano a regolare le differenze di sesso nel funzionamento delle cellule immunitarie per la neuroinfiammazione e il dolore neuropatico generale, secondo i risultati pubblicati su Science Advances.
“Questo studio evidenzia l’importanza della segnalazione del calcio mediata da Orai1 della microglia che contribuisce al dolore neuropatico. Ci fornisce una base per continuare a indagare sul ruolo che Orai1 svolge nella reattività della microglia”, ha affermato Kaitlyn DeMeulenaere, una studentessa del Driskill Graduate Program in Life. Sciences (DGP) e co-primo autore dello studio.
Murali Prakriya, Ph.D., Professore Magerstadt di Farmacologia e Professore di Medicina presso la Divisione di Allergologia e Immunologia, è stato l’autore senior dello studio.
Le microglia sono le cellule immunitarie primarie del cervello e assomigliano ai macrofagi presenti nel sistema immunitario periferico. Le microglia rilevano ed eliminano i patogeni dannosi e le cellule morenti e stimolano altre cellule immunitarie che innescano risposte immunitarie efficaci nel cervello. Oltre alle loro funzioni di sorveglianza, nei cervelli sani, le microglia influenzano anche la formazione di sinapsi, o connessioni, tra i neuroni, che incidono sui circuiti neurali e regolano le funzioni cognitive complessive.
Tuttavia, la microglia può anche causare neuroinfiammazione persistente e dolore neuropatico, compreso il dolore cronico causato da lesioni nervose e produrre citochine pro-infiammatorie che causano neuroinfiammazione incontrollata. La microglia può anche guidare cambiamenti duraturi nei circuiti sinaptici nel sistema nervoso centrale per migliorare la sensazione di dolore, secondo Prakriya.
“I segnali nel midollo spinale che normalmente non attivano i circuiti del dolore sono alterati in modo tale che dopo una lesione del nervo, gli stessi segnali vengono trasmessi attraverso il midollo spinale alla struttura cerebrale somatosensoriale del cervello superiore. Questo cambiamento è mediato in parte da mediatori dell’infiammazione, citochine prodotte dalla microglia spinale“, ha affermato Prakriya, che è anche membro del Robert H. Lurie Comprehensive Cancer Center della Northwestern University.
Il laboratorio di Prakriya ha scoperto una classe di canali del calcio chiamati canali Orai1 più di un decennio fa e da allora ha continuato a studiare il loro ruolo fondamentale nell’attivazione delle cellule immunitarie.
Nel presente studio, il team di Prakriya mirava a determinare quale ruolo svolge Orai1 nell’attivazione della microglia e nel dolore neuropatico a seguito di lesioni ai nervi.
Utilizzando modelli murini knockout Orai1 della microglia, i ricercatori hanno scoperto che quando la funzione Orai1 veniva bloccata o eliminata, la segnalazione del calcio mediata da Orai1 veniva persa, riducendo in ultima analisi la produzione di citochine infiammatorie.
Vedi anche:Chiarito il ruolo del calcio nella malattia familiare di Alzheimer
“Questa è una scoperta importante perché implica Orai1 come punto di controllo, se vuoi, nella cascata di eventi che porta alla produzione di citochine infiammatorie che guidano l’ipersensibilità al dolore“, ha detto Prakriya.
Successivamente, i ricercatori hanno confrontato le misure di ipersensibilità al dolore in seguito a lesione del nervo sciatico nei modelli murini. Sorprendentemente, hanno identificato differenze distinte nell’ipersensibilità al dolore nei topi maschi rispetto ai topi femmine privi di Orai1.
Nello specifico, hanno scoperto che la perdita di Orai1 mitigava l’ipersensibilità al dolore nei topi maschi, ma non nelle femmine. Ciò ha spinto i ricdercatori a indagare ulteriormente sulle cause del dimorfismo sessuale della percezione del dolore.
Utilizzando tecniche di elettrofisiologia del midollo spinale, hanno scoperto che nei topi knockout Orai1 della microglia maschile, il potenziamento, o un aumento della forza, della trasmissione sinaptica che si verifica a seguito di una lesione del nervo era ridotto. I topi maschi hanno anche mostrato una ridotta induzione di citochine infiammatorie nel tessuto del midollo spinale in risposta alla lesione del nervo, tuttavia ciò non è stato osservato nei topi femmina.
“Non vi è alcun cambiamento nella percezione del dolore neuropatico nei topi femmina perché non vi è alcun cambiamento nel potenziamento sinaptico disadattivo che si verifica a valle delle citochine infiammatorie prodotte dalla microglia. Poiché il potenziamento sinaptico disadattivo è probabilmente il passaggio critico che guida il dolore neuropatico, spiega perché c’è una mitigazione nei topi maschi ma non nelle femmine“, ha detto Prakriya.
Utilizzando una tecnica di marcatura della microglia chiamata colorazione IBA1, i ricercatori hanno scoperto che sebbene l’attivazione della microglia fosse aumentata allo stesso modo sia nei topi maschi che in quelli femminili, la funzione Orai1 inibita riduceva l’estensione dell’attivazione della microglia nei topi maschi, ma non nelle femmine.
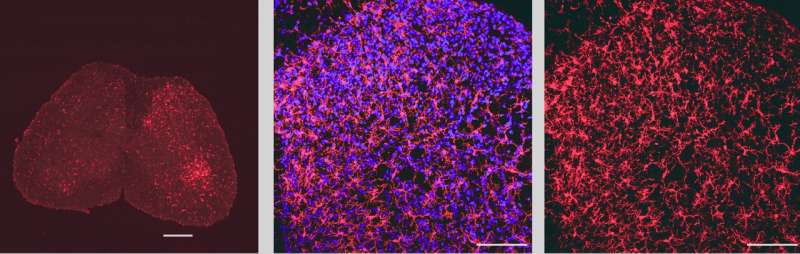
Immagine che mostra la microglia nel midollo spinale lombare etichettata con il marcatore microgliale IBA1 (in rosso). La macchia blu mostra nuclei di cellule marcate con un marcatore nucleare. Credito: laboratorio Prakirya
Hanno quindi somministrato a topi maschi e femmine un composto inibitore Orai1, una piccola molecola chiamato CM4620, che è attualmente in fase di test in studi clinici, e hanno scoperto che mentre il farmaco mitigava il dolore neuropatico nei topi maschi, non aveva alcun effetto nei topi femmina.
I risultati dimostrano che i canali Orai1 sono mediatori chiave della neuroinfiammazione indotta dalla microglia e del ruolo sessualmente dimorfico della microglia nel dolore neuropatico, sottolineando l’importanza di sviluppare terapie mirate specifiche per sesso in futuro.
“Questo studio indica notevoli differenze di sesso nei meccanismi sottostanti che mediano l’ipersensibilità al dolore tra maschi e femmine. Stiamo ora lavorando per identificare se la segnalazione Orai1 può essere manipolata in altre cellule immunitarie per fornire sollievo dal dolore nei topi femmina“, ha detto Prakriya.
Fonte: Science Advances