Nel 2008 i ricercatori della Scuola Perelman di Medicina presso l’Università della Pennsylvania hanno dimostrato che le mutazioni in due proteine associate alla malattia di familiare di Alzheimer (FAD), possono interrompere il flusso di ioni di calcio all’interno dei neuroni.
Le due proteine interagiscono con un canale di rilascio del calcio in un compartimento intracellulare. Forme mutanti di queste proteine che causano FAD, ma non le proteine normali, provocano segnalazione del calcio esagerato nella cellula.
Ora, lo stesso team, guidato da J. Kevin Foskett, PhD, presidente della Facoltà di Fisiologia e uno studente laureato, Dustin Shilling, hanno scoperto che sopprimere l’iperattività dei canali del calcio allevia i sintomi FAD-simili nei modelli murini della malattia.
I loro risultati compaiono questa settimana sulla rivista Journal of Neuroscience .
” Le attuali terapie per il morbo di Alzheimer sono farmaci che curano i sintomi di perdita cognitiva e demenza e molti farmaci che affrontano la patologia del morbo di Alzheimer, sono sperimentali. Queste nuove osservazioni suggeriscono che gli approcci basati sulla modulazione della segnalazione del calcio potrebbero essere esplorate “, dice il Prof.Foskett.
Le due proteine, chiamate PS1 e PS2 (presenilina 1 e 2), interagiscono con un canale di rilascio del calcio, il recettore inositolo trifosfato (IP3R), nel reticolo endoplasmatico. Mutante PS1 e PS2 aumentano l’attività di IP3R che a sua volta, aumenta i livelli di calcio nella cellula. “Abbiamo deciso di rispondere alla domanda: è aumentata la segnalazione del calcio, come risultato dell’interazione presenilin-IP3R, coinvolta nello sviluppo di sintomi familiari della malattia di Alzheimer, tra cui la demenza e deficit cognitivi ?” dice Foskett. “E guardando i risultati di questi esperimenti, la risposta è un sonoro ‘sì’ “.
La segnalazione del calcio intracellulare esagerata è un fenomeno robusto osservato in cellule esprimenti preseniline mutanti-FAD, sia nelle cellule umane in coltura che nelle cellule di topi. Il team ha utilizzato due modelli di mouse FAD per cercare queste connessioni. Specificamente, ha trovato che la riduzione dell’espressione di IP3R1, la forma dominante di questo recettore nel cervello, del 50 per cento, ha normalizzato la segnalazione del calcio esagerata osservata nei neuroni della corteccia e nell’ippocampo in entrambi i modelli murini.
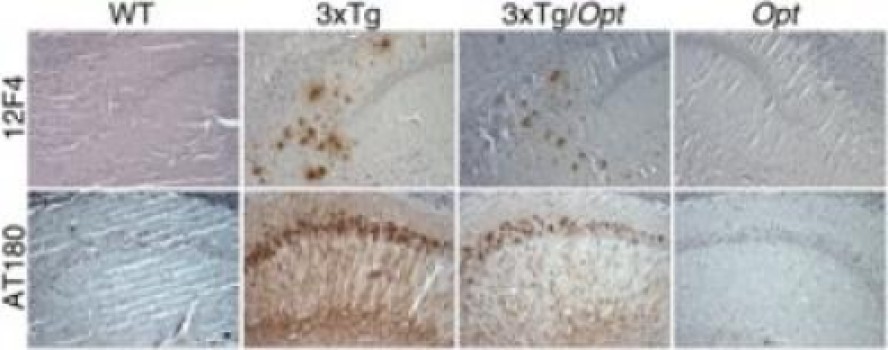
Inoltre, utilizzando topi 3xTg – animali contenenti presenilina 1 con una mutazione FAD, nonché mutante proteina tau umana espressa e geni APP – il team ha osservato che la ridotta espressione di IP3R1 ha diminuito profondamente l’ accumulo di placca amiloide nel tessuto cerebrale e la iperfosforilazione di proteina tau, una caratteristica biochimica della malattia di Alzheimer avanzata. Ridotta espressione di IP3R1 ha anche ridotto la difettosa segnalazione elettrica nell’ippocampo e deficit di memoria nei topi 3xTg, come misurato da test comportamentali.
“I nostri risultati indicano che la segnalazione del calcio esagerata, che è associata con mutazioni presenilin nella malattia di Alzheimer familiare, è mediata dal IP3R che contribuisce allo sviluppo dei sintomi della malattia negli animali”, dice Foskett. “Sappiamo ora che la via di segnalazione IP3 potrebbe essere considerata un potenziale bersaglio terapeutico per i pazienti con mutazioni in preseniline legati alla AD “.
L’ipotesi della ‘disregolazione del calcio’
“L’ipotesi della ‘disregolazione del calcio’ ereditaria, malattia ad esordio precoce di Alzheimer familiare è stata suggerita dai risultati di una ricerca precedente nel laboratorio di Foskett. Il morbo di Alzheimer colpisce ben 5 milioni di americani, il 5 per cento dei quali ha la forma familiare. La caratteristica della malattia è l’accumulo di grovigli e placche di amiloide beta proteina, nel cervello.
” I’ ipotesi’ che postula che il difetto principale è un accumulo di amiloide tossica nel cervello,m è stata a lungo utilizzata per spiegare la causa del morbo di Alzheimer”, dice Foskett. Nel 2008 lo studio Neuron del suo laboratorio, ha dimostrato che le cellule che portavano la forma mutata di PS1 che causa la malattia, presentavano una maggiore trasformazione di beta amiloide, che dipendeva l’interazione delle proteine PS con IP3R. Questa osservazione collega la disregolazione del calcio all’interno delle cellule, con la produzione di amiloide, una caratteristica nel cervello delle persone con malattia di Alzheimer.
Gli studi clinici di AD sono stati in gran parte diretti a ridurre l’onere dell’ amiloide nel cervello. Finora, dice Foskett, questi studi non sono riusciti a dimostrare i benefici terapeutici. Una idea è che gli interventi vengono avviati troppo tardi nel processo della malattia. Studi clinici anti-amiloide sono attualmente in corso con i pazienti asintomatici FAD perché è noto che essi finiranno per sviluppare la malattia, mentre predire chi svilupperà la forma comune di AD è molto meno certo.
Fonte University of Pennsylvania School of Medicine via Science Daily