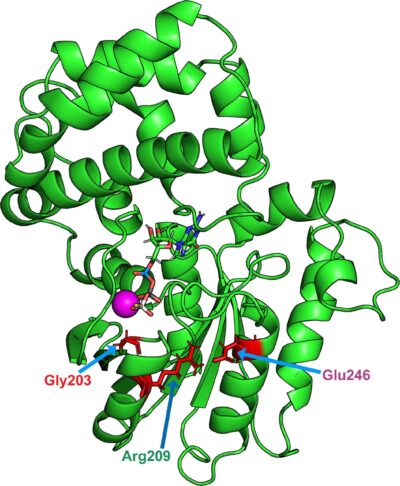
(Encefalopatie pediatriche-Immagine:Struttura del gene GNAO1 con la localizzazione delle tre mutazioni più frequenti. Credito: Larasati et al., Sci. avv. 8, eabn9350 (2022) 21 ottobre 2022).
L’encefalopatie pediatriche di origine genetica causano gravi disabilità motorie e intellettive sin dalla nascita. Una di queste malattie, identificata per la prima volta nel 2013, è causata da mutazioni nel gene GNAO1. Per comprendere i dettagli dei disturbi risultanti, gli scienziati dell’Università di Ginevra (UNIGE) hanno condotto analisi atomiche, molecolari e cellulari.
Hanno scoperto che una mutazione in GNAO1 porta alla sostituzione di un amminoacido con un altro nella sequenza proteica. Questo è sufficiente per interrompere il meccanismo di attivazione e disattivazione della proteina codificata, alterando così la capacità dei neuroni di comunicare correttamente con il loro ambiente.
Una semplice molecola di zinco, comunemente usata in altri contesti, potrebbe ripristinare, almeno in parte, il funzionamento della proteina interessata da queste mutazioni. Questi risultati, pubblicati sulla rivista Science Advances, fanno sperare in un trattamento che potrebbe cambiare la vita dei pazienti e delle loro famiglie.
I bambini con mutazioni del gene GNAO1 mostrano disturbi clinici significativi: ritardo dello sviluppo intellettivo e motorio, movimenti incontrollabili, nonché epilessia più o meno grave, talvolta accompagnata da danno cerebrale e atrofia. GNAO1 codifica per una proteina chiamata “Gαo” che è uno degli elementi costitutivi essenziali delle cellule neuronali.
“Questa mutazione è eterozigote dominante, il che significa che una delle due copie del gene è funzionale e l’altra è mutata”, spiega Vladimir Katanaev, Professore presso il Dipartimento di Fisiologia e Metabolismo Cellulare presso la Facoltà di Medicina dell’UNIGE, che ha guidato questa ricerca. “Anche se i neuroni hanno la metà delle proteine normali, i risultati sullo sviluppo neurologico sono devastanti“.
Un singolo amminoacido modificato
Le proteine Gαo funzionali vengono attivate quando sono legate al nucleotide chiamato GTP, quindi si disattivano attraverso l’idrolisi. Ciò consente alle proteine di seguire un ciclo di attivazione e disattivazione necessario per la funzione cellulare.
Le mutazioni nel gene GNAO1 portano alla sostituzione di un amminoacido in Gαo con un altro. Queste proteine mutate si attivano molto rapidamente, ma non sono in grado di effettuare l’idrolisi. Sono quindi intrappolate in uno stato di attivazione permanente.
“Si scopre che queste mutazioni influenzano indirettamente un aminoacido cruciale per l’idrolisi del GTP: la glutammina 205. Normalmente, questa glutammina è strutturalmente situata di fronte al GTP, che consente l’idrolisi. Tuttavia, questa glutammina viene spostata in caso di mutazione patologica: questa distanza strutturale impedisce che questo meccanismo abbia luogo“, spiega Vladimir Katanaev.
Interrompendo le interazioni con le proteine della membrana cellulare, queste mutazioni modificano la capacità dei neuroni di comunicare con il loro ambiente.
Una molecola nota da decenni
Gli scienziati hanno basato il resto del loro studio su questi primi risultati fondamentali. “In definitiva, il nostro obiettivo è cercare di trovare un trattamento che possa limitare i sintomi della malattia e migliorare la qualità della vita dei pazienti e delle loro famiglie”.
Per fare ciò, il team di ricerca ha eseguito uno screening ad alto rendimento di migliaia di farmaci approvati, con l’idea di identificare una molecola in grado di riattivare l’idrolisi. “In effetti, nelle malattie rare di solito non c’è modo di sviluppare una molecola completamente nuova. Il riutilizzo di molecole di farmaci già disponibili, approvate e sicure può invece essere una strategia di successo”, aggiunge Vladimir Katanaev.
Spicca una molecola, il piritione di zinco: corregge la perdita di interazioni intracellulari portando la glutammina 205 vicino alla sua normale posizione strutturale, consentendo l’idrolisi del GTP.
Vedi anche:Encefalite autoimmune: decifrato il funzionamento degli anticorpi
“Questo è un vecchio farmaco antimicotico e antibatterico utilizzato sotto forma di crema per alcune malattie della pelle. Abbiamo fatto un ulteriore passo avanti nell’analisi per vedere se tutta o parte di questa molecola fosse efficace. Si scopre che lo ione zinco è efficace e molto facile da trovare in qualsiasi farmacia, è già approvato per il trattamento della depressione lieve, dell’insonnia e persino di alcuni disturbi dello sviluppo nei bambini”, afferma Vladimir Katanaev.
Un modello di mosca per confermare questi risultati
Per confermare questo risultato, il team di ricerca ha utilizzato un modello animale innovativo: la mosca della Drosophila. “Abbiamo modificato il genoma delle mosche per replicare la mutazione del gene GNAO1, conservando una copia normale del gene come negli esseri umani”, spiega Mikhail Savitskiy, ricercatore nel laboratorio di Vladimir Katanaev e specialista nella modellazione delle malattie nella Drosophila.
“Le mosche avevano problemi di mobilità e una durata della vita ridotta“. Tuttavia, l’aggiunta di zinco alla loro dieta per tutta la vita, dalla fase larvale in poi, ha permesso loro di eliminare quasi completamente questi sintomi. “Questo risultato è davvero sorprendente, soprattutto perché lo zinco è una sostanza molto sicura, ben tollerata ed economica” dice Mikhail Savitskiy. I primi studi sui pazienti sembrano promettenti; verranno ora avviati studi clinici per valutare se un miglioramento può essere misurato a lungo termine.
Fonte:Science Advances