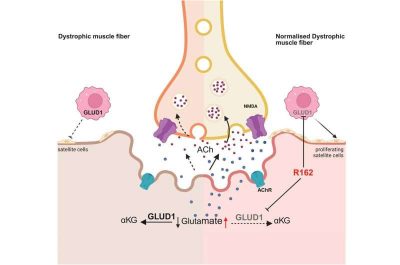
Distrofia muscolare di Duchenne- Immagine: un nuovo studio pubblicato sull’American Journal of Pathology identifica l’enzima glutammato deidrogenasi 1 (GLUD1) come potenziale bersaglio terapeutico per il ripristino muscolare nella distrofia muscolare di Duchenne. Di seguito è riportato uno schema degli effetti terapeutici del blocco farmacologico di GLUD1 nelle fibre muscolari distrofiche e nei macrofagi. Crediti: The American Journal of Pathology / Pereira-Nunes et al.
Una nuova ricerca ha identificato l’enzima glutammato deidrogenasi 1 (GLUD1) come nuovo bersaglio terapeutico per la distrofia muscolare di Duchenne (DMD). In modelli murini preclinici di DMD, i ricercatori hanno dimostrato che l’inibizione di GLUD1 migliora significativamente la forza e la coordinazione muscolare, segnalando un potenziale passaggio verso il ripristino della funzione muscolare piuttosto che la mera gestione dei sintomi. Lo studio innovativo pubblicato sull’American Journal of Pathology indica un percorso promettente e fattibile per il trattamento della DMD basato sullo sfruttamento del glutammato muscolare, rispondendo a un’esigenza clinicamente insoddisfatta.
La distrofia muscolare comprende un gruppo di malattie degenerative muscolari genetiche che portano alla progressiva atrofia muscolare. La DMD è la forma più comune e grave di distrofia muscolare e colpisce 1 maschio su 3.500-5.000 nati vivi a livello globale.
I difetti sottostanti nel gene della distrofina causano la distruzione delle fibre muscolari e ondate croniche di degenerazione e rigenerazione muscolare. Ciò si traduce nell’accumulo di cellule infiammatorie, fibrosi e disfunzione dei precursori muscolari, con conseguente perdita di massa e funzione muscolare. L’ approccio terapeutico per la DMD si concentra principalmente sul sollievo dei sintomi attraverso il trattamento con glucocorticoidi.
Il ricercatore principale, il Prof. Massimiliano Mazzone, Ph.D., del Laboratorio di infiammazione tumorale e angiogenesi del VIB-KU Leuven, Lovanio, Belgio, afferma: “Abbiamo precedentemente dimostrato che l’inibizione sia farmacologica che genetica di GLUD1, un enzima che converte l’L-glutammato in α-chetoglutarato e viceversa, nei macrofagi (un tipo di cellule immunitarie) ha migliorato significativamente la rigenerazione muscolare e il recupero funzionale in modelli di lesione acuta, ischemia e invecchiamento. Data la mancanza di una cura definitiva per la DMD e l’efficacia limitata delle attuali terapie, che mirano principalmente a rallentare la progressione della malattia e a migliorare la qualità della vita, eravamo ansiosi di verificare se colpire GLUD1 potesse offrire nuove prospettive terapeutiche specifiche per questa malattia”.
I ricercatori hanno studiato il potenziale terapeutico del target del metabolismo del glutammato nella DMD utilizzando l’inibitore di GLUD1 R162. In un modello murino preclinico di DMD (topi mdx), il trattamento sistemico con R162 ha migliorato significativamente la forza e la coordinazione muscolare.
Il co-ricercatore responsabile Emanuele Berardi, Ph.D., del Laboratorio di infiammazione tumorale e angiogenesi del VIB-KU Leuven e del Laboratorio di ingegneria tissutale della KU Leuven di Lovanio, Belgio, spiega: “Questo recupero funzionale è stato collegato alla riduzione del danno muscolare, al potenziamento del potenziale miogenico delle cellule satellite e al ripristino della struttura e della funzione della giunzione neuromuscolare (NMJ)”.
È interessante notare che, sebbene l’inibizione di GLUD1 nei macrofagi abbia da sola promosso l’attivazione delle cellule satellite, non è stata sufficiente a ripristinare la funzione muscolare, evidenziando il ruolo essenziale, ma non esclusivo, dei macrofagi nella rigenerazione muscolare. “Abbiamo inoltre dimostrato che i macrofagi sono necessari per mediare il pieno effetto terapeutico di R162, in particolare nel supportare il rimodellamento della giunzione neuromuscolare (NMJ)”, aggiungwe il ricercatore.
La co-ricercatrice Andreia Pereira-Nunes, Ph.D., del Laboratorio di Infiammazione Tumorale e Angiogenesi del VIB-KU Leuven, Lovanio, Belgio, e dell’Istituto di Ricerca sulle Scienze dell a Vita e della Salute (ICVS), Braga, Portogallo, spiega: “Meccanicisticamente, il trattamento con R162 ha riprogrammato il metabolismo del glutammato nei muscoli distrofici, aumentandone la disponibilità locale, che a sua volta ha migliorato la riorganizzazione morfologica delle giunzioni neuromuscolari (NMJ) e ripristinato i livelli di acetilcolina. È importante sottolineare che il trattamento è stato ben tollerato e non ha mostrato effetti avversi sul peso corporeo, sull’assunzione di cibo o sul comportamento“.
Questo studio introduce un nuovo approccio terapeutico non steroideo che non agisce direttamente sul difetto genetico della DMD, ma ne migliora la funzione neuromuscolare attraverso la riprogrammazione metabolica. La duplice azione terapeutica di R162 nel migliorare sia la funzione delle cellule precursori muscolari (cellule satellite) sia la neurotrasmissione offre un approccio promettente e potenzialmente traducibile per migliorare i risultati clinici dei pazienti, in particolare data la sua efficacia e sicurezza nei topi distrofici utilizzati per studiare la DMD.
Leggi anche:Distrofia muscolare di Duchenne: impatto sul cervello potrebbe essere reversibile
La co-ricercatrice Ummi Ammarah, dottoranda presso il Laboratorio di infiammazione tumorale e angiogenesi del VIB-KU Leuven, Lovanio, Belgio, e il Centro di biotecnologie molecolari dell’Università di Torino, Torino, Italia, conclude: “I nostri risultati forniscono la prima prova di concetto che i farmaci metabolici possono essere utilizzati efficacemente per trattare le distrofie muscolari, offrendo una nuova strategia bypassando il difetto genetico e modificando una funzione non correlata ai muscoli“.