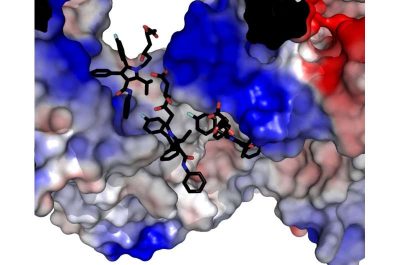
Statine-immagine: questa illustrazione, basata sulla microscopia crioelettronica macromolecolare ad alta risoluzione, mostra le molecole di statina in nero che si legano alla proteina RyR1. Crediti: The Bioelectricity Lab, UBC Life Sciences Institute
Le statine hanno trasformato la salute del cuore, salvando milioni di vite grazie alla riduzione del colesterolo e del rischio di infarti e ictus. Ma per molti pazienti, questi farmaci presentano un effetto collaterale preoccupante: dolori muscolari, debolezza e, in rari casi, grave disgregazione muscolare che può portare a insufficienza renale.
Come le statine influenzano le cellule muscolari
Il team ha utilizzato la criomicroscopia elettronica, una potente tecnica di imaging che rivela le proteine con dettagli quasi atomici, per catturare l’interazione delle statine con una proteina muscolare critica chiamata recettore della rianodina (RyR1). Questa proteina agisce come un gatekeeper per il calcio all’interno delle cellule muscolari, aprendosi solo quando i muscoli devono contrarsi. Quando le statine si legano a questo recettore, forzano l’apertura del gate, causando una continua perdita di calcio, un effetto tossico che può danneggiare il tessuto muscolare.
“Siamo stati in grado di osservare, quasi atomo per atomo, come le statine si agganciano a questo canale“, ha affermato l’autore principale dello studio, il Dott. Steven Molinarolo, ricercatore post-dottorato presso il Dipartimento di Biochimica e Biologia Molecolare dell’UBC. “Questa perdita di calcio spiega perché alcuni pazienti avvertono dolori muscolari o, in casi estremi, complicazioni potenzialmente letali”.
Implicazioni per lo sviluppo futuro delle statine
Lo studio si è concentrato sull’atorvastatina, una delle statine più prescritte, ma i risultati suggeriscono che l’effetto potrebbe essere comune a tutta la classe di farmaci. I ricercatori hanno scoperto che le statine si legano in un modo molto insolito: tre molecole si raggruppano all’interno di una tasca della proteina. La prima molecola si attacca quando il canale è chiuso, innescandone l’apertura. Altre due molecole si incuneano poi, forzando la completa apertura del canale.
“È la prima volta che abbiamo un quadro chiaro di come le statine attivano questo canale”, ha affermato il Dott. Filip Van Petegem, autore senior e Professore presso il Life Sciences Institute dell’UBC. “È un grande passo avanti perché ci fornisce una tabella di marcia per la progettazione di statine che non interagiscono con il tessuto muscolare”.
Modificando solo le parti della molecola della statina responsabili degli effetti negativi, gli scienziati potrebbero preservare la parte che abbassa il colesterolo, riducendo al contempo il rischio.
Potenziale impatto sui pazienti e sulla terapia
Sebbene il danno muscolare grave colpisca solo una piccola parte degli oltre 200 milioni di utilizzatori di statine in tutto il mondo, sintomi più lievi come dolori e affaticamento sono molto più comuni e spesso portano i pazienti a interrompere il trattamento. Le nuove scoperte potrebbero aiutare a prevenire questi problemi e a migliorare l’aderenza alla terapia salvavita.
Leggi anche:Statine collegate a un minor rischio di cancro del colon-retto nei pazienti con colite ulcerosa
La ricerca sottolinea l’importanza delle tecnologie di imaging avanzate nel promuovere le innovazioni mediche. Utilizzando la struttura di microscopia crioelettronica macromolecolare ad alta risoluzione della Facoltà di Medicina dell’UBC, il team è stato in grado di visualizzare l’interazione tra statina e proteina con un dettaglio straordinario, trasformando una questione fondamentale sulla sicurezza dei farmaci in spunti pratici che potrebbero plasmare la prossima generazione di terapie.
Astratto
“Le statine rappresentano la classe di farmaci più prescritta e inibiscono un enzima chiave nella biosintesi del colesterolo. Molti pazienti hanno riportato sintomi muscolari da lievi a gravi e un sottogruppo è a rischio di rabdomiolisi. Varianti di sequenza in RyR1, il recettore della rianodina del muscolo scheletrico, sono correlate all’intolleranza alle statine, ma non è ancora chiaro se RyR1 possa legare direttamente le statine. In questo articolo riportiamo le strutture crio-EM di RyR1 in assenza e presenza di atorvastatina, stabilendo con certezza che RyR1 è un bersaglio indesiderato. I nostri risultati mostrano una modalità di legame insolita, in cui tre molecole di atorvastatina si legano insieme in una fessura formata dal dominio di rilevamento pseudo-voltaggio, creando ampie interazioni tra loro e con RyR1. L’atorvastatina attiva RyR1 in modo sequenziale, per cui una statina per subunità può legarsi alla regione transmembrana di un RyR1 chiuso, con piccole perturbazioni strutturali che preparano il canale all’apertura. Il legame di due statine aggiuntive per subunità è associato a un ampliamento del dominio di rilevamento del pseudo-voltaggio che innesca l’apertura del poro. Il confronto con il legame dell’atorvastatina all’HMG-CoA reduttasi, il suo bersaglio previsto, offre indizi su come modificare la statina per ridurre il legame con RyR1, lasciando inalterato il legame con l’HMG-CoA reduttasi”.
“Le statine sono state un pilastro della cura cardiovascolare da decenni“, ha affermato il Dott. Van Petegem. “Il nostro obiettivo è renderle ancora più sicure, in modo che i pazienti possano trarne beneficio senza timore di gravi effetti collaterali”.
Per milioni di persone che fanno affidamento sulle statine, ciò potrebbe significare meno problemi muscolari e una migliore qualità della vita.