La sclerosi multipla (SM) è una malattia complessa e cronica, caratterizzata da demielinizzazione del sistema nervoso centrale (SNC) mediata da processi autoimmuni. Sebbene il numero e l’efficacia dei trattamenti modificanti la malattia disponibili siano aumentati nell’ultimo decennio, più recentemente con l’introduzione delle terapie anti-CD20 che inducono la deplezione delle cellule B, tutti questi trattamenti agiscono sui processi infiammatori periferici. Pertanto, vi è un’urgente necessità di trattamenti in grado di prevenire efficacemente la progressione della patologia neurologica e di migliorare la riparazione tissutale. Uno dei fattori chiave alla base della progressione della SM è la ridotta capacità del SNC di effettuare la rimielinizzazione, ovvero il processo di formazione di nuova mielina attorno agli assoni.
Due molecole farmacologiche sperimentali hanno promosso la riparazione della mielina in modelli di sclerosi multipla, indicando una possibile via futura per il trattamento dei danni ai nervi, anziché limitarsi a sopprimere l’infiammazione.
La sclerosi multipla (SM) è una delle principali cause di disabilità neurologica nei giovani adulti e colpisce quasi tre milioni di persone in tutto il mondo. Nonostante decenni di ricerca e importanti progressi nel rallentare la progressione della malattia, gli scienziati non sono ancora riusciti a sviluppare una terapia in grado di riparare il tessuto nervoso danneggiato.
Ora, una nuova tesi di dottorato suggerisce che la situazione potrebbe finalmente cambiare: i ricercatori hanno identificato due diverse molecole farmacologiche in grado di innescare con successo la rigenerazione della mielina, il rivestimento protettivo che permette alle cellule nervose di comunicare correttamente.
La sclerosi multipla è più comune nell’Europa settentrionale e in Canada, con tassi di incidenza che aumentano verso le latitudini più settentrionali. La malattia si manifesta quando il sistema immunitario attacca erroneamente la mielina, interrompendo gradualmente la trasmissione dei segnali nervosi nel cervello e nel midollo spinale. Con l’accumularsi del danno, i pazienti possono manifestare sintomi che vanno dalla vista offuscata e dalla stanchezza cronica a problemi di mobilità e disabilità neurologica a lungo termine.
Non esiste una cura per i danni neurologici
I farmaci attualmente utilizzati per la sclerosi multipla sono progettati per ridurre l’eccessiva attività del sistema immunitario, ma non riparano il danno nervoso già presente. Questa limitazione è particolarmente grave nella sclerosi multipla progressiva, dove il danno si accumula gradualmente nel corso di molti anni.
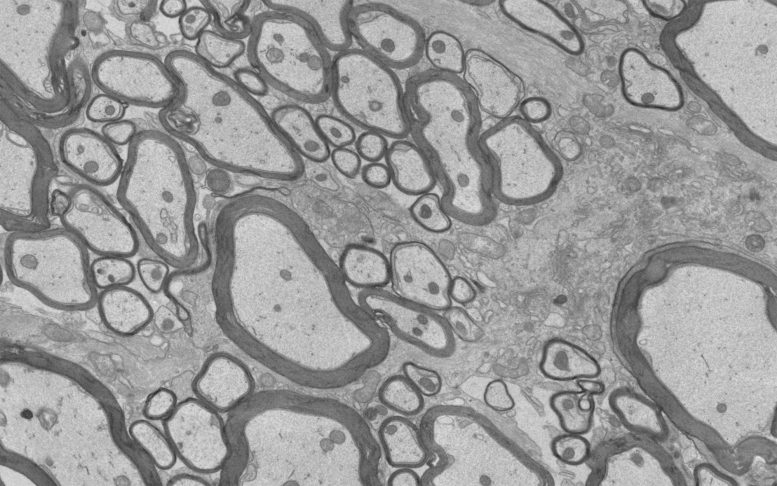
Per decenni, i ricercatori hanno cercato modi per riavviare la rimielinizzazione, il processo di riparazione mediante il quale la mielina danneggiata si rigenera e i neuroni riacquistano protezione. Finora, tutti i farmaci candidati testati a questo scopo si sono rivelati inefficaci. Un ostacolo importante è rappresentato dal fatto che, soprattutto negli stadi avanzati della sclerosi multipla, il sistema nervoso centrale sviluppa patologie tissutali locali che bloccano la riparazione della mielina.
Leggi anche:Sclerosi multipla: due strategie farmacologiche potenziano la riparazione della mielina
Due soluzioni con lo stesso risultato
Nella sua tesi di dottorato, Tapani Koppinen, del gruppo di ricerca della professoressa associata Merja Voutilainen, ha individuato due diverse modalità per migliorare la rimielinizzazione.
La prima strategia utilizza una molecola farmacologica per agire sulla risposta allo stress all’interno delle cellule cerebrali. Nelle aree danneggiate dalla sclerosi multipla, questa risposta rimane costantemente iperattiva, impedendo alle cellule che promuovono la riparazione di svolgere la loro funzione. Dopo aver bloccato questo meccanismo con la nuova molecola farmacologica, la rimielinizzazione è aumentata significativamente ed è avvenuta più rapidamente nel tessuto cerebrale che presentava danni simili a quelli della sclerosi multipla. Lo studio è stato pubblicato sulla rivista Molecular Therapy a febbraio.
La seconda strategia si concentra sul tessuto cicatriziale che si sviluppa intorno alle aree danneggiate e che crea un ostacolo fisico alla riparazione nervosa. Modificando la composizione di questo tessuto cicatriziale con un’altra molecola farmacologica, questo approccio ha contribuito a promuovere il recupero neuronale. Un articolo su questa strategia è stato pubblicato sulla rivista Neuropharmacology nel novembre 2025.
Sebbene i due farmaci agiscano attraverso meccanismi completamente diversi, hanno prodotto risultati sorprendentemente simili: una forte rimielinizzazione e una minore neuroinfiammazione nei modelli di malattia, ovvero nei test su animali e cellule che riproducono la patologia tissutale della sclerosi multipla.
Il primo farmaco che stimola la rimielinizzazione necessita di ulteriori ricerche.
In questa fase, i risultati provengono da studi su animali da laboratorio e modelli cellulari. Poiché la sclerosi multipla umana coinvolge condizioni tissutali più complesse, le molecole del farmaco devono ancora essere testate per verificarne l’efficacia sull’uomo. I farmaci mirati al cervello devono inoltre affrontare la barriera emato-encefalica, che impedisce a molte sostanze di penetrare nel cervello. Ciononostante, i ricercatori hanno dimostrato che entrambe le molecole hanno raggiunto con successo il sistema nervoso centrale negli animali da laboratorio.
“L’obiettivo è quello di permettere alle molecole che abbiamo sviluppato di raggiungere la fase di sperimentazione clinica, che un giorno potrebbe portare alla creazione dei primi farmaci in grado di favorire la rimielinizzazione nella sclerosi multipla. Nel frattempo, le nostre scoperte possono contribuire a indagare i meccanismi patogenetici della sclerosi multipla che inibiscono la rimielinizzazione“, afferma Koppinen.
Astratto
“L’infiammazione nella sclerosi multipla porta all’attivazione cronica di un meccanismo di stress cellulare, la risposta alle proteine mal ripiegate (UPR), che si ritiene esacerbi la neuroinfiammazione e impedisca le risposte rigenerative dei tessuti, come la rimielinizzazione. La proteina MANF, che modula le UPR, si è dimostrata molto promettente nell’attenuare l’attivazione cronica dell’UPR e nel migliorare la rigenerazione tissutale in vari modelli di malattia, ma non raggiunge il sistema nervoso centrale se somministrata perifericamente. Abbiamo utilizzato C-MANF, un frammento C-terminale di MANF e abbiamo dimostrato che la somministrazione sottocutanea di C-MANF promuove il recupero della funzione motoria e la rigenerazione tissutale in un modello murino di demielinizzazione autoimmune. Abbiamo dimostrato che C-MANF sopprime l’attivazione neuroinfiammatoria e facilita il recupero degli oligodendrociti dopo la demielinizzazione, riducendo al contempo l’attivazione a lungo termine delle UPR. Inoltre, abbiamo dimostrato che C-MANF potenzia la mielinizzazione degli OPC primari in coltura, che la promozione della rimielinizzazione nelle colture di fette organotipiche di cervelletto dipende dalla modulazione delle UPR e che l’applicazione esogena di C-MANF sopprime l’attivazione cronica di tutte e tre le vie delle UPR negli oligodendrociti. Infine, abbiamo dimostrato che la demielinizzazione nei cervelli con deficit di MANF porta a un’estesa neuroinfiammazione e degenerazione del SNC, indicando la modulazione delle UPR da parte di MANF come componente chiave nelle risposte tissutali alla demielinizzazione. Nel complesso, dimostriamo che la modulazione delle UPR con C-MANF rappresenta un nuovo e promettente approccio terapeutico per il trattamento della demielinizzazione neuroinfiammatoria.