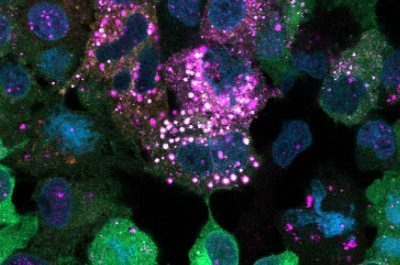
Metabolismo del glicogeno-immagine: cellule epatiche umane trattate con un farmaco che induce l’ubiquitinazione del glicogeno. Le brillanti macchiette bianche appaiono dove il glicogeno e l’ubiquitina si sovrappongono, indicando che il glicogeno è stato marcato con ubiquitina all’interno delle cellule. Fonte: WEHI
I ricercatori del WEHI hanno scoperto un meccanismo inedito che il nostro corpo utilizza per regolare gli zuccheri, una scoperta che riscrive le regole fondamentali della biologia e apre una nuova frontiera nella scienza. Pubblicato su Nature, lo studio è il primo a svelare un potenziale processo terapeutico che potrebbe essere utilizzato per ridurre direttamente la quantità di zucchero immagazzinata nell’organismo. L’articolo si intitola “Ubiquitinazione del glicogeno e dei metaboliti nelle cellule e nei tessuti”.
I risultati potrebbero avere implicazioni cliniche per le persone affette da patologie causate da livelli eccessivi di zucchero nel sangue, tra cui diabete, malattie cardiache e una serie di malattie rare per le quali attualmente non esistono trattamenti.
Quando consumiamo alimenti contenenti zucchero, il nostro corpo converte l’eccesso in glicogeno, che viene immagazzinato principalmente nel fegato e nei muscoli. Per secoli, gli scienziati hanno studiato il metabolismo del glicogeno: un percorso ben definito, insegnato a ogni studente di biologia e medicina di generazione in generazione.
Il Professor David Komander, coautore principale dello studio, ha affermato che la ricerca del team ha aggiunto un nuovo capitolo a un libro che in precedenza era considerato completo.
“È molto probabile che i libri di biologia dovranno essere modificati in seguito alle nostre scoperte”, ha affermato il Professor Komander, anche a capo della divisione di segnalazione dell’ubiquitina del WEHI. “Abbiamo scoperto una seconda via attraverso la quale il glicogeno può essere regolato direttamente, probabilmente a richiesta. Si tratta di una svolta entusiasmante per le persone affette da malattie causate da un eccesso di glicogeno“.
Le malattie da accumulo di glicogeno (GSD) sono un gruppo di rare patologie ereditarie che si manifestano quando l’organismo non è in grado di produrre o scomporre correttamente il glicogeno. Spesso non esistono trattamenti disponibili per queste malattie.
Un eccesso di glicogeno è inoltre collegato a patologie più comuni come diabete, obesità, malattie del fegato e del cuore. Queste condizioni sono scatenate da un accumulo di glicogeno. Ad oggi, non esistono terapie in grado di attaccare direttamente la molecola di glicogeno.
“Nuovi farmaci promettenti, come Ozempic, stanno trasformando il modo in cui gestiamo la glicemia, indirettamente attraverso la regolazione ormonale”, ha affermato il Professor Komander. “Senza la capacità di regolare il glicogeno stesso, è difficile contrastarne l’accumulo, causa principale di molte malattie. Ecco perché il nostro studio è entusiasmante. Abbiamo trovato un modo per andare direttamente alla fonte“.

L’eroe nascosto
L’ubiquitina è una proteina nota per legarsi ad altre proteine, stabilendo un potente sistema di controllo che aiuta l’organismo a identificare le proteine danneggiate che devono essere riciclate o eliminate.
Il glicogeno non è una proteina, bensì uno zucchero. Eppure, questo studio innovativo ha dimostrato che l’ubiquitina può legarsi anche agli zuccheri, sia in modelli animali che in cellule umane.
Il coautore principale, il Dottor Simon Cobbold, si è detto entusiasta che l’ubiquitina riceva finalmente il giusto riconoscimento. “L’ubiquitina è davvero un eroe sconosciuto che ha lavorato silenziosamente dietro le quinte per tutto questo tempo, mantenendoci in vita”, ha affermato il Dottor Cobbold.
Questa svolta è stata resa possibile dal NoPro-clipping, una tecnica all’avanguardia sviluppata negli ultimi quattro anni dal Dr. Cobbold, dal Prof. Komander e dal primo autore, Marco Jochem.
Questa tecnica pionieristica consente ai ricercatori di studiare l’ubiquitina con un livello di dettaglio senza precedenti e permette, per la prima volta, di rilevare eventi di ubiquitinazione non proteica tramite spettrometria di massa.
“Senza i nostri strumenti e il nostro metodo, questo straordinario processo sarebbe rimasto invisibile”, ha affermato il Dottor Cobbold. “Questa è la bellezza del NoPro-clipping: ci permette di studiare una serie di molecole che il campo dell’ubiquitina ha trascurato fino ad ora“.
Marco Jochem, dottorando, ha affermato che il vero punto di forza di questo strumento risiede nella sua versatilità. “Non solo possiamo usarlo per rilevare il glicogeno ubiquitinato, ma possiamo anche scoprire metaboliti ubiquitinati come il glicerolo e la spermina, che abbiamo scoperto per la prima volta in tutte le nostre cellule“, ha affermato. “La nostra scoperta sta riscrivendo le regole fondamentali della biologia e della segnalazione dell’ubiquitina. E sono sicuro che abbiamo solo scalfito la superficie“.
Leggi anche:Il glucosio aiuta le cellule T a costruire strutture che combattono il cancro
Risultati rapidi: come è stato condotto lo studio
Nella parte più eclatante dello studio, i ricercatori hanno utilizzato la tecnica NoPro-clipping per visualizzare come l’ubiquitina si legasse al glicogeno all’interno del fegato dei topi quando questi erano alimentati e a digiuno.
Hanno scoperto che quando i topi sono a digiuno e hanno bisogno di energia, i livelli di glicogeno si esauriscono.
Inoltre, la presenza di “tag” di ubiquitina è aumentata durante l’esaurimento del glicogeno, suggerendo che l‘ubiquitinazione degli zuccheri regoli la degradazione del glicogeno.
I risultati mostrano che l‘ubiquitina è una nuova e sorprendente componente del metabolismo del glicogeno, aggiungendo un nuovo livello a un processo biochimico ben noto e “da manuale”.
È importante sottolineare che le variazioni dinamiche nelle etichette di ubiquitina dello zucchero suggeriscono una funzione di controllo chiave che gestisce come e quando il glicogeno viene rilasciato.
I ricercatori sono stati anche in grado di aumentare l’ubiquitinazione del glicogeno, il che ha comportato una diminuzione del glicogeno nelle cellule.
Se questi risultati potranno essere estesi agli animali e all’uomo, si potranno sviluppare nuovi metodi per combattere le malattie. Sono in corso le prime discussioni con gli investitori.
Lo studio è frutto della collaborazione tra WEHI, l’Università di Melbourne, l’Università di Colonia (Germania) e Alfred Health.
Fonte: Nature