Neuroblastoma-immagine: modello schematico che illustra l’asse di segnalazione NO-mTOR nel neuroblastoma. In condizioni basali/patologiche (pannello di sinistra) e con inibizione di nNOS (pannello di destra). Crediti: Haitham Amal
Il neuroblastoma inizia prima della nascita. In qualche punto dello sviluppo fetale, le cellule della cresta neurale che avrebbero dovuto maturare in tessuto surrenale o gangli simpatici prendono una direzione errata e un bambino nasce portatore di una neoplasia che potrebbe non manifestarsi per mesi. Il neuroblastoma rappresenta circa il 28% di tutti i tumori diagnosticati nei neonati in Europa e negli Stati Uniti. Nella sua forma più lieve, regredisce spontaneamente, come un fuoco che si spegne da solo. Nella sua forma più aggressiva, metastatizza con una velocità tale da costringere gli oncologi a usare parole che preferirebbero non pronunciare di fronte ai genitori.
Il neuroblastoma ad alto rischio ha un tasso di sopravvivenza a cinque anni di circa il 40%. Questa percentuale è rimasta pressoché invariata per una generazione. Ora, uno studio pubblicato su Brain Medicine offre qualcosa che finora scarseggiava: una spiegazione meccanicistica di come questo tumore si autoalimenta e un modo per interrompere il circolo vizioso.
Il messaggero che si è trasformato in mercenario
L’ossido nitrico è tra le molecole di segnalazione più antiche in biologia. Dilata i vasi sanguigni. Trasporta messaggi tra i neuroni. A concentrazioni fisiologiche è indispensabile, un silenzioso servitore pubblico. Ma a concentrazioni elevate diventa reattivo, generando specie azotate che modificano chimicamente le proteine attraverso un processo chiamato S-nitrosilazione. Tale modifica è stata implicata in ogni fase della progressione del cancro.
La relazione tra ossido nitrico e tumori non è semplice. Concentrazioni molto elevate possono danneggiare il DNA e innescare l’apoptosi. Livelli più bassi e costanti sembrano invece avere l’effetto opposto, favorendo la sopravvivenza e la metastasi.
Il Professor Haitham Amal e i suoi colleghi dell’Università Ebraica di Gerusalemme avevano precedentemente dimostrato che l’ossido nitrico favorisce la progressione del glioblastoma. La questione ancora aperta era se lo stesso enzima, la sintasi dell’ossido nitrico neuronale, svolgesse una funzione simile anche nel neuroblastoma e, in tal caso, attraverso quale via metabolica a valle.
La risposta si è rivelata essere mTOR.
Due strade che conducono allo stesso silenzio
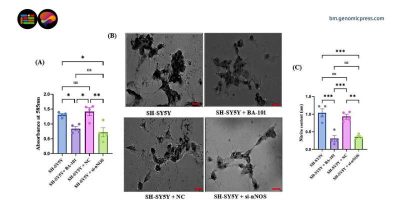
Il team ha attaccato la nNOS da due direzioni. Ha trattato cellule di neuroblastoma umano SH-SY5Y con BA-101, un inibitore farmacologico selettivo, a una concentrazione di 100 μM per 24 ore. Separatamente, i ricercatori hanno silenziato il gene nNOS con RNA interferente (siRNA). La logica era precisa: se un farmaco e uno strumento genetico producono lo stesso risultato, si tratta di un fenomeno biologico, non di un semplice rumore farmacologico.
Hanno ottenuto lo stesso risultato.
BA-101 ha ridotto l’attività della NADPH-diaforasi, il parametro standard per valutare la funzionalità della NOS, del 35-40%. Il silenziamento genetico l’ha ridotta del 45-50%. I livelli di nitriti, un indicatore stabile della produzione di ossido nitrico, sono diminuiti del 65-70% con BA-101 e del 55-60% con siRNA.
La formazione di colonie, la misura più diretta della capacità proliferativa, è diminuita significativamente dopo il trattamento con BA-101 (p < 0,001) e il silenziamento di nNOS (p < 0,01). Le cellule stavano perdendo la loro capacità di moltiplicarsi.
Una cascata di segnali collassa dall’alto
Ciò che seguì a valle fu sistematico. La nitrazione della tirosina proteica, misurata tramite l’immunoreattività della 3-nitrotirosina, diminuì drasticamente dopo il trattamento con BA-101 (p < 0,01) e il silenziamento di nNOS (p < 0,001). La firma chimica dello stress nitrosativo si stava affievolendo.
Poi è scattato l’effetto domino. La fosforilazione di AKT è diminuita (p < 0,01 con BA-101; p < 0,05 con siRNA), mentre l’AKT totale è rimasto invariato. La fosforilazione di mTOR stesso è diminuita in entrambe le condizioni (p < 0,01 in entrambi i casi).
La proteina ribosomiale S6, substrato a valle di mTORC1, è risultata aumentata (p < 0,05 con BA-101; p < 0,01 con siRNA). Ed ecco il dettaglio più significativo: TSC2, un regolatore negativo chiave della segnalazione di mTOR, è aumentato significativamente in entrambi i trattamenti (p < 0,05). La rimozione del segnale dell’ossido nitrico ha permesso al sistema frenante della cellula di riattivarsi, come rilasciare un piede da un acceleratore collegato al pavimento.
La sinaptofisina, un marcatore tumorale neuroendocrino utilizzato per valutare la natura maligna delle cellule del neuroblastoma, è diminuita significativamente con BA-101 (p < 0,01) e con il silenziamento di nNOS (p < 0,05). Le cellule tumorali non stavano semplicemente crescendo più lentamente. Stavano diventando, a livello molecolare, meno riconoscibilmente cancerose.
L’esperimento dello specchio
La buona scienza pone la domanda al contrario. Se il blocco dell’ossido nitrico sopprime la segnalazione di mTOR, allora inondare la cellula di ossido nitrico dovrebbe amplificarla. I ricercatori hanno esposto le cellule SH-SY5Y a SNAP, un donatore di ossido nitrico, a una concentrazione di 200 μM per 24 ore.
Ogni ago ha oscillato nella direzione opposta. La 3-nitrotirosina è aumentata (p < 0,05). TSC2 è diminuita (p < 0,01). La fosforilazione di AKT, mTOR e RPS6 è aumentata (p < 0,05 per ciascuno). L‘esperimento inverso ha prodotto il risultato inverso, che è il tipo di simmetria che separa una scoperta da una casualità.
Dalla piastra all’animale
La coltura cellulare può fornire molte informazioni, ma non può prevedere se un tumore all’interno di un organismo vivente reagirà allo stesso modo. Il team ha creato un modello di neuroblastoma xenogenico iniettando cellule SH-SY5Y per via sottocutanea nei fianchi di topi NOD-SCID di sei settimane, ha atteso la comparsa di tumori palpabili e ha quindi somministrato BA-101 per via intraperitoneale alla dose di 80 mg/kg/giorno per 22 giorni. Gli animali di controllo hanno ricevuto solo il veicolo. Sei topi per gruppo.
I tumori del gruppo di controllo hanno raggiunto una dimensione massima di circa 1,5 cm. I tumori trattati non hanno mostrato tale crescita. Il volume e il peso finali del tumore si sono ridotti drasticamente nel gruppo BA-101 (p < 0,001 per entrambi).
Il peso corporeo non ha mostrato differenze significative tra i gruppi, suggerendo che il composto è stato ben tollerato senza manifestare tossicità sistemica evidente. I dati in vivo hanno confermato quanto i dati in vivo devono fare: hanno dimostrato che il meccanismo osservato in vitro è attivo anche nell’organismo intero.
“L’entità della soppressione in vivo ha attirato la nostra attenzione”, ha affermato il Professor Haitham Amal, autore corrispondente dello studio, che ricopre incarichi presso l’Istituto per la ricerca sui farmaci, la Facoltà di Farmacia e Medicina dell’Università Ebraica di Gerusalemme e il Centro di Neuroscienze Traslazionali Rosamund Stone Zander e Hansjoerg Wyss del Boston Children’s Hospital, Harvard Medical School.
“Avevamo già dimostrato il ruolo dell’ossido nitrico nel glioblastoma, ma la coerenza dei risultati ottenuti nel neuroblastoma in ogni test, dalla fosforilazione proteica alla formazione di colonie fino alla crescita degli xenotrapianti, indica che la nNOS è più di un semplice fattore contribuente. Sembra essere un elemento centrale nella via di segnalazione che sostiene questo tumore“.“Ciò che mi ha convinto è stata la concordanza tra gli approcci farmacologici e genetici”, ha affermato il Dottor Shashank Kumar Ojha, primo autore dello studio e ricercatore presso l’Istituto per la ricerca sui farmaci dell’Università Ebraica di Gerusalemme.
“Quando BA-101 e siRNA producono indipendentemente lo stesso schema di effetti sull’attività della NADPH-diaforasi, sui marcatori di stress nitrosativo, sulla fosforilazione della via mTOR e sulla crescita clonogenica, si può essere certi che il processo biologico sia reale. Questa riproducibilità è ciò che fornisce un’ipotesi terapeutica degna di ulteriori verifiche“.
Leggi anche: Neuroblastoma: Dinutuximab beta più la chemioterapia riduce il tumore nei bambini
Ciò che resta sconosciuto
Gli autori sono espliciti riguardo ai limiti. Il lavoro in vitro si basa su una singola linea cellulare, SH-SY5Y, che non può riprodurre l’intera eterogeneità genetica del neuroblastoma né la complessità del microambiente tumorale. L’identità chimica di BA-101 non è attualmente divulgata in attesa del rilascio del brevetto, il che significa che la replicazione indipendente da parte di altri laboratori dovrà attendere.
Resta da chiarire se lo stress nitrosativo sia la causa diretta del suo deterioramento funzionale, o se sia coinvolto un meccanismo intermedio; gli autori lo segnalano esplicitamente come spunto per future ricerche.
Si tratta di precisazioni oneste e importanti. Ma non sminuiscono la scoperta principale. L’asse nNOS-mTOR è reale, è suscettibile di intervento farmacologico e nei topi risponde all’intervento con una forza che richiede ulteriori studi.
Gli inibitori di mTOR, come i rapaloghi e gli inibitori catalitici di mTOR, hanno mostrato un’efficacia limitata come monoterapie nel neuroblastoma, compromessa dall’attivazione a feedback e dai meccanismi di resistenza. Il presente studio suggerisce una diversa geometria d’attacco: anziché colpire mTOR alla serratura, intervenire a monte, sulla mano che gira la chiave.
Riducendo l’attivazione di mTOR dipendente dall’ossido nitrico, l’inibizione di nNOS potrebbe aggirare i meccanismi compensatori che hanno ostacolato il blocco diretto di mTOR.
C’è una grande distanza tra il fianco di un topo e il letto di un bambino. I ricercatori lo sanno meglio di chiunque altro. Ma una porta che prima era invisibile è stata ora localizzata, misurata e si è dimostrato che si apre. Ciò che la attraverserà in futuro dipenderà dagli studi che seguiranno.
Fonte:EurekAlert