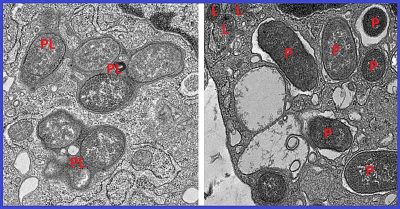
Malattia di Crohn-immagine: le micrografie elettroniche mostrano come i macrofagi che esprimono la girdina neutralizzino i patogeni fondendo i fagosomi (P) con i lisosomi cellulari (L) per formare i fagolisosomi (PL), compartimenti in cui i patogeni e i detriti cellulari vengono degradati (sinistra). Questo processo è cruciale per il mantenimento dell’omeostasi cellulare. In assenza di girdina, questa fusione fallisce, consentendo ai patogeni di eludere la degradazione e la neutralizzazione (destra). Credito: UC San Diego Health Sciences.
Studi su singole cellule hanno rivelato che i macrofagi intestinali mantengono l’omeostasi intestinale attraverso l’azione bilanciata di sottopopolazioni reattive (infiammatorie) e tolleranti (non infiammatorie). Il modo in cui tale equilibrio viene compromesso nelle malattie infiammatorie intestinali (IBD), tra cui il morbo di Crohn (MC) e la colite ulcerosa (CU), rimane irrisolto. In questo studio, i ricercatori definiscono gli stati macrofagici specifici del colon e rivelano il ruolo critico dei macrofagi non infiammatori associati al colon (niColAM) nella guarigione dalle IBD.
I ricercatori dell’Università della California a San Diego hanno risolto un dibattito decennale sul ruolo del primo gene della malattia di Crohn associato a un rischio maggiore di sviluppare questa malattia autoimmune.
L’intestino umano contiene due tipi di macrofagi, o globuli bianchi specializzati che svolgono ruoli molto diversi, ma ugualmente importanti nel mantenimento dell’equilibrio dell’apparato digerente. I macrofagi infiammatori combattono le infezioni microbiche, mentre i macrofagi non infiammatori riparano i tessuti danneggiati. Nel morbo di Crohn, una forma di malattia infiammatoria intestinale (MICI), uno squilibrio tra questi due tipi di macrofagi può causare un’infiammazione intestinale cronica, danneggiando la parete intestinale e causando dolore e altri sintomi.
I ricercatori della facoltà di medicina dell’Università della California a San Diego hanno sviluppato un nuovo approccio che integra l’intelligenza artificiale (IA) con tecniche avanzate di biologia molecolare per decodificare ciò che determina se un macrofago diventerà infiammatorio o non infiammatorio.
Lo studio risolve anche un mistero di lunga data che circonda il ruolo di un gene chiamato NOD2 in questo processo decisionale. NOD2 è stato scoperto nel 2001 ed è il primo gene associato a un rischio aumentato di morbo di Crohn.
Lo studio è pubblicato sul Journal of Clinical Investigation.
Utilizzando un potente strumento di apprendimento automatico, i ricercatori hanno analizzato migliaia di pattern di espressione genica dei macrofagi provenienti da tessuto del colon affetto da IBD e da tessuto del colon sano. Hanno identificato una firma genetica macrofagica composta da 53 geni che separa in modo affidabile i macrofagi reattivi e infiammatori dai macrofagi in fase di guarigione dei tessuti.
“NOD2 funziona come sistema di sorveglianza delle infezioni dell’organismo”, ha affermato l’autore senior Pradipta Ghosh, MD, Professore di medicina cellulare e molecolare presso la Facoltà di Medicina dell’UC San Diego. “Quando si lega alla girdina, rileva i patogeni invasori e mantiene l’equilibrio immunitario intestinale neutralizzandoli rapidamente. Senza questa interazione, il sistema di sorveglianza NOD2 collassa“.
I ricercatori hanno poi confermato l’importanza dell’interazione tra NOD2 e girdina confrontando modelli murini di morbo di Crohn privi della proteina girdina con quelli con girdina intatta. Hanno scoperto che i topi privi di girdina soffrivano di uno squilibrio nel microbioma intestinale e sviluppavano un’infiammazione dell’intestino tenue. Spesso morivano di sepsi, una condizione in cui il sistema immunitario innesca una risposta eccessiva a un’infezione, causando infiammazione in tutto il corpo e danni agli organi vitali.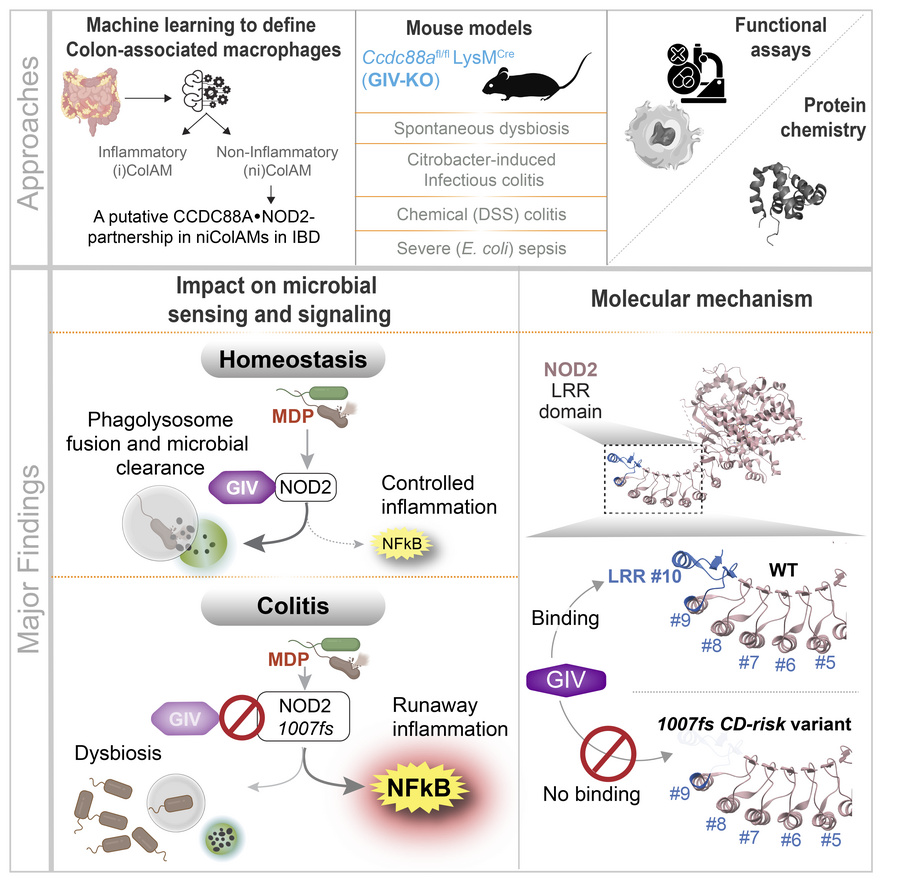
Astratto grafico credito Journal of Clinical Investigation.
Leggi anche: Malattia di Crohn: i lieviti fattori scatenanti
“L’intestino è un campo di battaglia e i macrofagi sono i pacificatori”, ha affermato il co-autore Gajanan D. Katkar, Ph.D., assistente ricercatore di progetto presso la Facoltà di Medicina dell’UC San Diego. “Per la prima volta, l’intelligenza artificiale ci ha permesso di definire e tracciare chiaramente i giocatori di due squadre avversarie”.
Unendo la classificazione basata sull’intelligenza artificiale, la biochimica meccanicistica e i modelli murini, lo studio risolve uno dei dibattiti più longevi sulla malattia di Crohn. I risultati non solo spiegano come una mutazione genetica chiave determini la malattia, ma potrebbero anche contribuire allo sviluppo di trattamenti volti a ripristinare la relazione tra girdina e NOD2.