Una famiglia di proteine soppressive del cancro, note come proteine TET, aiuta a regolare l’attività dei geni attraverso l’influenza sull’architettura cromosomica. Tuttavia, fino ad ora non era del tutto chiaro come i geni fossero attivati dalle proteine TET per assicurarsi che le cellule svolgessero le loro normali funzioni in modo efficiente.
Il team della ricercatrice dell’Istituto di Immunologia di La Jolla, Anjana Rao, ha pubblicato la ricerca nel numero del 26 aprile 2019 della rivista Science Immunology.
I ricercatori riferiscono che la delezione o la mutazione genetica di TET2 e TET3 nelle cellule B del topo smorza la generazione di anticorpi IgG funzionali, diminuendo l’efficacia delle risposte immunitarie.
Inoltre, identificano un gene delle cellule B che diventa silenziato in assenza di TET2 e TET3, evidenziando quanto sia critico il controllo “epigenetico” dell’espressione genica per una sana funzione delle cellule immunitarie e suggerisce perché la perdita di TET promuove l’oncogenesi.
Il DNA può essere strettamente avvolto da spirali dei geni sepolti all’interno di torsioni cromosomiche, mentre l’espressione genica procede intanto che le bobine si svolgono e il DNA diventa più accessibile. Questo processo è influenzato dalle proteine TET, che modificano la struttura chimica del DNA alterando un gruppo metilico collegato a C, una delle quattro basi del DNA A, C, T e G. Questa cosiddetta “regolazione epigenetica” alterando l’accessibilità del DNA o la struttura, è una strategia importante che le cellule usano per attivare e disattivare i geni.
“In precedenza le persone sapevano che le proteine TET erano coinvolte nella soppressione del cancro“, afferma il co-autore dello studio Chan-Wang Jerry Lio. “Ma era difficile capire quale fosse la normale funzione dei geni TET perché i topi hanno sviluppato il cancro rapidamente”.
Il nuovo studio aggira questo problema utilizzando una strategia alternativa di “knock out condizionale” in cui i ricercatori hanno eliminato TET2 e TET3 in cellule B mature in un momento a loro scelta in topi sperimentali. Cinque giorni dopo aver rimossero le cellule B del topo i ricercatori hanno eseguito una serie di test molecolari per confrontare la loro attività con quella delle cellule B derivate da topi normali in cui TET2 e TET3 sono rimasti intatti.
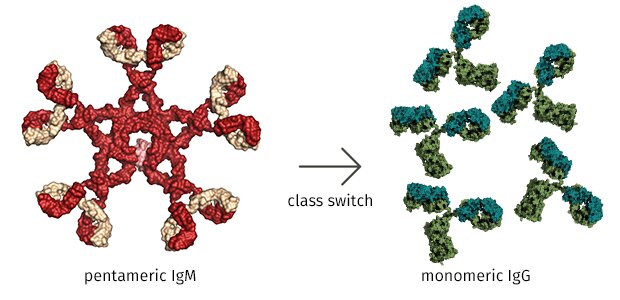
Una differenza fondamentale era che quando stimolati da un agente patogeno sperimentale, le cellule B mutanti che mancavano di TET2 e TET3 producevano una sovrabbondanza di una classe di anticorpi chiamata IgM, mentre le cellule B di controllo normali producevano anticorpi più efficaci classificati come IgG o “gamma globulina”.
“Gli anticorpi sono disponibili in diversi sapori“, spiega Vipul Shukla, altro coautore dello studio. “L’aroma standard (IgM) fa un cattivo lavoro di attivazione di altre cellule immunitarie, quindi una volta che una cellula B normale incontra un agente patogeno, cerca di convertire gli anticorpi IgM in un sapore più favorevole per innescare un’efficace risposta immunitaria”.
Quel sapore “benefico”, noto agli immunologi come IgG, costituisce circa il 75% di tutti gli anticorpi trovati nel siero umano normale.
Le cellule B sane non hanno problemi a convertire le IgM in IgG usando un trucco di modifica del gene innato chiamato “cambio di classe”, in cui gli strumenti proteici ritagliano regioni specifiche di IgM in un filamento di DNA e quindi incollano sequenze analoghe di DNA di IgG. Quella manovra crea geni ricombinati che esprimono gli anticorpi IgG, che a differenza delle IgM, sono in grado di neutralizzare i patogeni, aiutando altre cellule a riconoscere gli invasori (comprese le cellule cancerose) e mantenendo il benessere di un organismo.
Ed è qui che entra in gioco TET.
Il gruppo di Rao ha scoperto che le cellule B mutanti prive di TET2 e TET3 capovolgono questo interruttore solo in modo insufficiente e invece rimangono bloccate producendo anticorpi IgM perché mancano dello strumento necessario per lo splicing del DNA. Nello specifico, le cellule mutanti prive di TET2 e TET3 non producono una proteina chiamata AID, che esegue effettivamente lo splicing IgM-IgG, semplicemente perché TET2 e TET3 non erano disponibili per demetilare e quindi migliorare l’espressione del gene AID. Nelle cellule mutanti prive di TET2 e TET3, il gene AID rimane probabilmente metilato, inaccessibile e silente, consentendo agli anticorpi IgM di predominare.
L’incapacità di eseguire il cambio di classe ha conseguenze cliniche: i pazienti che ereditano mutazioni nel gene AID (che nell’uomo è chiamato AICDA) soffrono di una deficienza immunitaria chiamata sindrome iper IgM, in cui le loro cellule B non possono effettuare la normale conversione di IgM in anticorpi IgG . Questi individui sono più vulnerabili alle infezioni gravi e alle neoplasie.
I geni TET non sono ancora stati implicati nella sindrome da iper IgM. Ma la rivelazione che il gene AID è un bersaglio TET conferisce a Lio un senso immunologico indiscutibile in questo contesto. “TET2 è il gene più frequentemente mutato nei tumori del sangue tra cui linfomi diffusi a grandi cellule B, il che suggerisce che limita la progressione del cancro nelle cellule B normali“, afferma 5l ricerctore. “Ancora più importante, l’intera attività delle proteine TET richiede la vitamina C. Il nostro studio potrebbe spiegare come una dieta sana possa migliorare la nostra risposta immunitaria“.
Shukla concorda. “Le proteine TET sono spesso inibite nei tumori, compresi i tumori derivati da cellule B qui trattati”, dice Shukla. “Un importante fondamento logico di questo articolo è stato quello di identificare la normale funzione delle proteine TET in modo da comprendere meglio il motivo per cui i tumori si sviluppano quando i geni TET vengono trattenuti”.
Fonte, Science