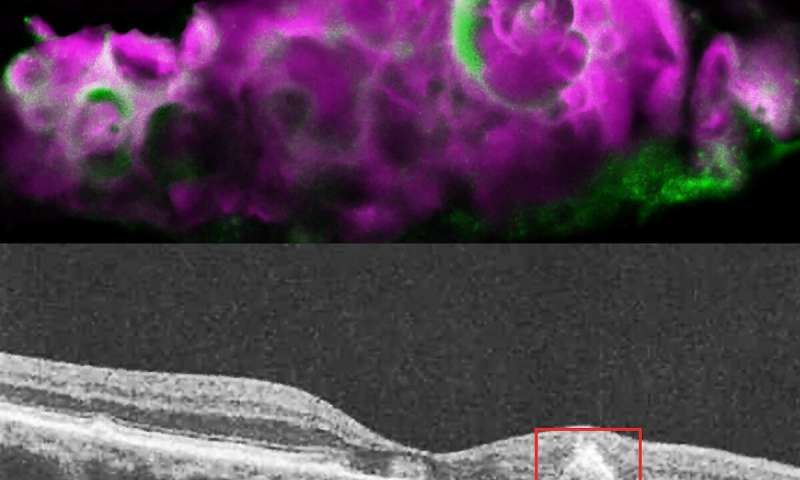
Immagine: sferule HAP (rosa) e proteina amelotina (verde) in drusen morbido dall’occhio con AMD secca. In basso: immagine OCT dell’occhio con AMD secca, che mostra un drusen morbido sotto l’epitelio pigmentato retinico. Credito: Dinusha Rajapakse, NEI.
Una proteina che normalmente deposita il calcio mineralizzato nello smalto dei denti può anche essere responsabile dei depositi di calcio nella parte posteriore dell’occhio nelle persone con degenerazione maculare legata all’età secca (AMD), secondo uno studio condotto da ricercatori del National Eye Institute (NEI).
Questa proteina, l’amelotina, può rivelarsi un bersaglio terapeutico per questa condizione. I risultati sono stati pubblicati sulla rivista Translational Research. Il NEI fa parte del National Institutes of Health.
“Usando un semplice modello di coltura cellulare di cellule epiteliali del pigmento retinico, siamo stati in grado di dimostrare che l’amelotina viene attivata da un certo tipo di stress e provoca la formazione di un particolare tipo di deposito di calcio osservato anche nelle ossa e nei denti. Quando abbiamo osservato gli occhi umani da donatore con AMD secca, abbiamo trovato la stessa proteina”, ha affermato Graeme Wistow, Ph.D., capo della Sezione NEI/Struttura molecolare e genomica funzionale e autore senior dello studio.
Esistono due forme di AMD: umida e secca. Mentre ci sono trattamenti che possono rallentare la progressione dell’AMD umida, attualmente non esistono trattamenti per l’AMD secca. Nell’AMD secca, depositi di colesterolo, lipidi, proteine e minerali si accumulano nella parte posteriore dell’occhio. Alcuni di questi depositi sono chiamati drusen morbidi e hanno una composizione specifica, diversa dai depositi trovati nella AMD umida. Forme di Drusen sono state trovate sotto l’epitelio pigmentato retinico (RPE), uno strato di cellule che trasporta sostanze nutritive dai vasi sanguigni sottostanti per supportare i fotorecettori sensibili alla luce della retina sopra di essi. Man mano che il drusen si sviluppa, l’RPE e infine i fotorecettori muoiono, portando alla cecità. I fotorecettori non possono ricrescere, quindi la cecità è permanente.
Recentemente, i ricercatori hanno scoperto un composto minerale contenente calcio chiamato idrossiapatite (HAP) in depositi di AMD secchi. HAP è un componente chiave dello smalto dei denti e delle ossa. Piccole palline di HAP piene di colesterolo, chiamate sferule, sono state trovate solo nei drusen di persone con AMD secca e non in quelle con AMD umida o senza AMD.
In questo studio, il team di Wistow ha scoperto che se avesse affamato le cellule RPE cresciute nei pozzetti, un tipo di sistema di coltura cellulare, per 9 giorni, le cellule avrebbero iniziato a depositare HAP. I ricercatori hanno determinato che la proteina amelotina, codificata dal gene AMTN, è fortemente sovraregolata dopo una fame prolungata ed è responsabile della mineralizzazione dell’HAP nel loro modello di coltura cellulare. Il blocco di questo percorso nella loro linea cellulare RPE ha anche bloccato la produzione di questi depositi simili a drusen.
Per verificare che il loro modello di coltura cellulare rappresentasse accuratamente AMD secca, i ricercatori hanno esaminato gli occhi da cadavere umano con AMD secca, AMD umida o senza AMD. Hanno trovato HAP e amelotina solo negli occhi con AMD secca e non negli altri occhi. Mentre l’amelotina è stata trovata a volte in aree di AMD secca senza drusen, era principalmente presente nelle aree di drusen morbide con grandi depositi di HAP.
“Prima di questo studio, nessuno sapeva davvero come si stava accumulando l’idrossiapatite nel drusen dell’ AMD secca”, ha detto Dinusha Rajapakse, Ph.D., il primo autore dello studio. “Trovare questa proteina specifica del dente nell’occhio, questa proteina legata alla deposizione di idrossiapatite, è stato davvero inaspettato”.
Perché le cellule RPE nell’AMD secca iniziano a depositare queste sferule HAP non è chiaro, ma Wistow pensa che potrebbe essere un meccanismo protettivo andato storto. “È possibile”, dice, “che questi depositi di proteine, lipidi e minerali possano aiutare le cellule RPE danneggiate a bloccare la crescita dei vasi sanguigni nella retina, un problema che è una delle caratteristiche chiave dell’AMD umida. Ma quando i depositi minerali diventano troppo estesi, possono anche bloccare il flusso di nutrienti verso l’RPE e i fotorecettori, portando alla morte delle cellule della retina”.
“Meccanicamente, l’amelotina sembra un giocatore chiave per la formazione di queste sferule idrossiapatite molto specifiche. Questo è ciò che fa nei denti, ed eccola nella parte posteriore dell’occhio. Concettualmente, si potrebbero utilizzare farmaci che bloccano specificamente la funzione dell’amelotina negli occhi e questo potrebbe ritardare la progressione della malattia. Ma non lo sapremo finché non lo proveremo”, ha detto Wistow.
Sono urgentemente necessari buoni modelli animali per testare le terapie AMD secca. Sulla base dei risultati di questo studio, Wistow e il suo team stanno creando un nuovo modello murino per la malattia. Inoltre, Wistow ritiene che il suo modello di coltura cellulare, che imita le caratteristiche dell’AMD secca, potrebbe essere potenzialmente utile per lo screening di farmaci ad alto rendimento per trovare molecole che rallentano o impediscono lo sviluppo di drusen molli.