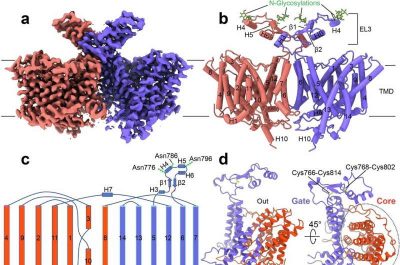
Cancro al seno-immagine: struttura crioEM di NBCn1. Crediti: Nature Communications
Gli scienziati dell’UCLA hanno caratterizzato la struttura e la funzione di una proteina chiave per la sopravvivenza nelle cellule del cancro al seno, aiutando a spiegare come questi tumori resistano allo stress ambientale e prosperino in ambienti acidi e poveri di ossigeno, che normalmente sarebbero tossici per le cellule sane.
L‘articolo è pubblicato sulla rivista Nature Communications.
Come NBCn1 aiuta le cellule cancerose a sopravvivere
Le cellule tumorali al seno si affidano a una proteina trasportatrice chiamata NBCn1 per trasportare ioni alcalini all’interno della cellula e mantenere un pH interno favorevole. Utilizzando la microscopia crioelettronica avanzata combinata con la modellazione computazionale, i ricercatori hanno dimostrato che NBCn1 trasporta due ioni sodio e uno ione carbonato attraverso un efficiente movimento “simile a quello di un ascensore” che riduce al minimo il consumo di energia. Ciò consente a NBCn1 di raggiungere un’elevata velocità di trasporto di circa 15.000 ioni al secondo, aiutando le cellule tumorali a mantenere un pH interno che ne promuove la sopravvivenza, la divisione e la resistenza allo stress acido.
I microambienti tumorali sono spesso acidi a causa dei bassi livelli di ossigeno e dell’elevata attività metabolica. Le cellule sane faticano a sopravvivere in queste condizioni, ma le cellule tumorali si adattano regolando la propria chimica interna. NBCn1 è un trasportatore della membrana plasmatica noto per contribuire al controllo del pH cellulare, ma fino ad ora si sapeva poco sulla sua struttura precisa o su come ottenga un trasporto ionico così efficiente.
Progressi nella ricerca sulla struttura delle proteine
Per comprendere il funzionamento di questa proteina, i ricercatori hanno utilizzato la microscopia crioelettronica per catturare la prima struttura atomica tridimensionale dell’NBCn1 umano. Hanno quindi applicato la modellazione computazionale per studiare la dinamica della proteina e il modo in cui interagisce con gli ioni. Questo approccio combinato ha permesso al team di visualizzare i cambiamenti strutturali dell’NBCn1 e di identificare i percorsi che gli ioni seguono durante il passaggio attraverso il trasportatore.
Grazie alla comprensione della struttura e della funzione di NBCn1, lo studio fornisce un modello per la progettazione di farmaci in grado di bloccare questo trasportatore e alterare l’equilibrio chimico interno da cui dipendono le cellule tumorali. Colpire specificamente questa proteina nelle cellule tumorali potrebbe offrire un modo preciso per indebolire i tumori riducendo al minimo i danni ai tessuti sani.
Leggi anche :Veleno dello scorpione amazzonico si rivela promettente contro il cancro al seno
“Questo lavoro fa progredire il campo del metabolismo delle cellule cancerose e della biologia del trasporto di membrana, fornendo il primo modello a livello atomico di NBCn1, un importante regolatore del pH cellulare”, ha affermato il dott. Ira Kurtz, illustre Professore di medicina, titolare della cattedra Factor in nefrologia molecolare e membro dell’UCLA Brain Research Institute.
Spiegano gli autori:
“In tutto il mondo, il cancro al seno è il tumore più comune nelle donne ed è anche la causa più comune di morte per cancro. Come altri tumori, i tumori al seno hanno sviluppato meccanismi adattativi per sopravvivere in presenza di un ambiente locale extracellulare acido. Le analisi di sistema nelle cellule del cancro al seno hanno mostrato un accoppiamento tra un aumento della produzione di acido lattico e una diminuzione dell’assorbimento di ossigeno, con la capacità di elevare il pH i e prevenirne il declino, prolungando così la sopravvivenza del tumore. Di conseguenza, l’abbassamento del pH i nelle cellule del cancro al seno è un potenziale approccio terapeutico che può migliorare la risposta agli inibitori della crescita delle cellule tumorali. Una delle principali proteine di trasporto ionico della membrana plasmatica nei tumori al seno, identificata tramite analisi di genomica funzionale, è NBCn1 (SLC4A7), che carica equivalenti di basi nelle cellule, aumentando così il pH 1 e acidificando l’ambiente extracellulare. NBCn1 appartiene alla famiglia proteica SLC4, i cui membri mediano in generale il trasporto di HCO 3 ‾ o CO 3 2 ‾ accoppiato a Na + e/o Cl‾ in una modalità di scambio o simporto. È importante notare che precedenti studi di associazione a livello del genoma hanno stabilito una connessione tra le variazioni negli SNP di SLC4A7 e il rischio di sviluppare un cancro al seno. Inoltre, i livelli di espressione dell’mRNA di SLC4A7, in particolare nei tumori al seno luminali A o basali/triplo negativi, sono stati identificati come correlati con la sopravvivenza delle pazienti. Nei modelli murini, la perdita di NBCn1 compromette la crescita delle cellule del cancro al seno, mentre un aumento dell’espressione di NBCn1 dovuto alla perdita di RPTPγ è associato alla trasformazione maligna del tessuto mammario normale, alla riduzione della sopravvivenza e a una recidiva più rapida. Nelle cellule del cancro al seno MCF-7, NBCn1 svolge un ruolo importante nella progressione del ciclo cellulare e nell’ingresso in mitosi. Uno studio recente ha confermato che il target di NBCn1 con anticorpi monoclonali provoca la morte delle cellule del cancro al seno in vitro.
In questo studio, abbiamo determinato la struttura a risoluzione quasi atomica mediante microscopia elettronica criogenica (cryoEM) di NBCn1 umano con densità corrispondenti agli ioni trasportati e abbiamo modellato computazionalmente i cambiamenti dello stato conformazionale durante il suo ciclo di trasporto. Piccole variazioni strutturali della proteina durante le sue transizioni elevatore OF ↔ IF sono associate a un tasso di turnover ionico (TOR) e a un flusso di basi misurati estremamente elevati. Utilizzando questo trasportatore di carico di basi altamente efficiente, le cellule del cancro al seno possono avere un vantaggio in termini di sopravvivenza”.
“Collegando la struttura della proteina, l’energetica degli ioni e la funzione, lo studio mostra come piccoli movimenti molecolari possano generare un’elevata efficienza di trasporto. Queste intuizioni colmano un divario critico tra la biofisica di base e la terapia del cancro e gettano le basi per nuove strategie che mirano alla regolazione del pH come fattore vulnerabile nelle cellule tumorali“.
Fonte: Nature Communications