Fibrosi polmonare idiopatica-immagine: illustrazione: Sara Gironi Carnevale
La fibrosi polmonare idiopatica, una malattia mortale, colpisce milioni di persone, ma non esiste una terapia efficace. Farmaci in fase di sviluppo potrebbero intervenire prima che si stabilizzi.
Anche una malattia mortale come la fibrosi polmonare idiopatica (IPF) può iniziare con una semplice tosse. Ma con il progredire della malattia, una persona può sperimentare fino a 500 spasmi respiratori al giorno. La respirazione diventa difficile, così come il sonno. Una carenza cronica di ossigeno aumenta la pressione sanguigna nei polmoni. Entro 3-5 anni dalla diagnosi, se non trattata, una persona svilupperà insufficienza respiratoria e morirà. Come suggerisce il termine “idiopatico”, la causa della malattia non è chiara, sebbene si ritenga che sia la genetica che l’ambiente abbiano un ruolo.
La fibrosi polmonare idiopatica si sviluppa più o meno in silenzio, quindi è difficile diagnosticarla precocemente. “C’è una diagnosi insufficiente. Spesso le persone si rivolgono a noi pneumologi quando è troppo tardi”, afferma Gisli Jenkins, pneumologo presso l’Imperial College di Londra.
I tentativi di curare la condizione, o almeno di alleviarne i sintomi, si sono concentrati principalmente sulla fibrosi, la formazione di tessuto cicatriziale attorno ai minuscoli alveoli polmonari. Finora, la situazione è stata difficile. Il trattamento con una combinazione di farmaci antinfiammatori, che è stato lo standard di cura da molti anni, ora non è raccomandato perché uno studio clinico del 2012 ha concluso che non solo non migliorava i risultati, ma aumentava anche la mortalità.
Nel 2014, due trattamenti sono stati approvati dalla Food and Drug Administration (FDA) statunitense e sono diventati l’attuale standard di cura. Il primo, Nintedanib, agisce sui miofibroblasti, le cellule che causano la fibrosi, nel tentativo di riparare i danni polmonari in aumento. Nintedanib inibisce tre tipi di recettori che promuovono l’attività di queste cellule per prevenire ulteriori danni.
Il farmaco rallenta la diminuzione della capacità vitale forzata (CVF), ovvero la quantità massima di aria che una persona può espirare forzatamente dopo aver inspirato il respiro più profondo possibile. Tuttavia, non ci sono prove che riduca la mortalità e causa effetti collaterali gravosi, come la diarrea.
Varianti generiche del Pirfenidone sono disponibili dal 2022. I principali brevetti per il Nintedanib sono scaduti in Europa e scadranno negli Stati Uniti nel 2026, aprendo la strada a opzioni generiche più accessibili. Tuttavia, i persistenti effetti collaterali di questi farmaci potrebbero limitare l’impatto di questa opportunità. Molte persone che assumono terapie per la fibrosi polmonare idiopatica devono modificare la propria dieta e preoccuparsi di trovare i servizi igienici quando sono fuori casa.
Secondo Toby Maher dell’Università della California del Sud a Los Angeles, meno della metà delle persone affette da IPF negli Stati Uniti assume uno dei due farmaci. “Gli pneumologi sono stati molto riluttanti a prescrivere farmaci che sapevano che i pazienti avrebbero avuto difficoltà a tollerare“, afferma Maher, pneumologo e ricercatore principale di diversi studi clinici per le terapie contro la IPF.
“I farmaci non migliorano la loro qualità di vita”, afferma lo pneumologo Moisés Selman dell’Istituto Nazionale per le Malattie Respiratorie di Città del Messico, pioniere della teoria, oggi ampiamente accettata, secondo cui la FPI deriva da una disfunzione delle cellule epiteliali. “I pazienti spesso hanno la sensazione che la loro malattia sia la stessa, o addirittura peggiore“.
Quindi la ricerca di trattamenti continua. Ci sono almeno una mezza dozzina di farmaci in fase di sviluppo. E uno, il Nerandomilast, è stato approvato dalla FDA nell’ottobre 2025. Questi trattamenti generalmente mirano agli stadi iniziali della malattia polmonare, perché la fibrosi conclamata è difficile da invertire. Ma finora nessuno di essi riduce la mortalità, per non parlare della cura della malattia.
Obiettivi sfuggenti
Nintedanib e Pirfenidone agiscono principalmente sulle fasi avanzate della fibrosi polmonare idiopatica (IPF), coinvolgendo i miofibroblasti che creano il tessuto cicatriziale e la via del TGF-β che stimola l’attività cellulare. Sono in fase di sviluppo composti per modulare questa via con maggiore precisione. Uno di questi composti, il GTX-11, riduce l’attivazione di due proteine a valle del recettore cellulare a cui si lega il TGF-β. Lo sviluppatore del composto, GAT Therapeutics di Barcellona, in Spagna, sta attualmente conducendo uno studio di fase I.
Tuttavia, i risultati deludenti di altri studi suggeriscono che sia difficile colpire questa via senza creare ulteriori problemi. Dopo essere stato secreto, il TGF-β è solitamente bloccato in uno stato inattivo da una proteina partner chiamata LAP. Un approccio promettente è stato quello di bloccare due proteine transmembrana, chiamate integrina αvβ1 e integrina αvβ6. Queste attivano LAP per rilasciare TGF-β in risposta a indicatori chimici e fisici di danno, come l’aumento della rigidità tissutale e spesso amplificano l’indicatore originale. Ma l’approccio ha incontrato ostacoli.
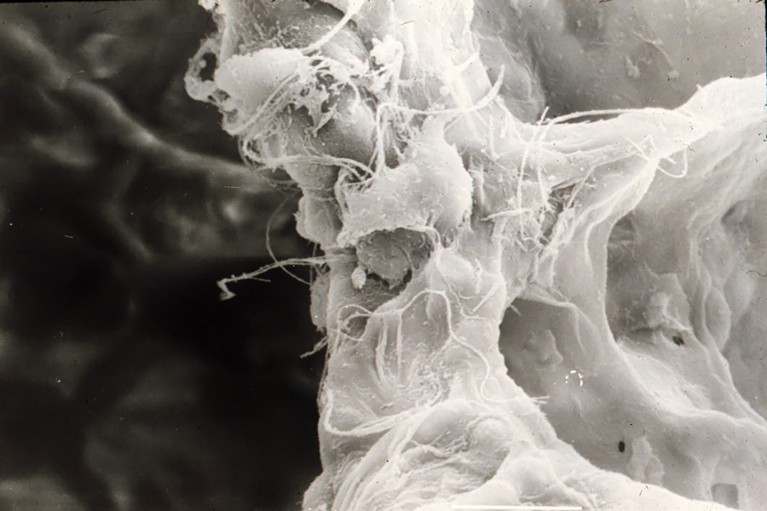
Immagine di microscopia elettronica a scansione (SEM) ad alta risoluzione che mostra l’ultrastruttura tridimensionale del setto alveolare nel polmone. La fitta rete fibrosa rappresenta la matrice extracellulare che forma la struttura settale, mentre le cellule arrotondate e dal contorno irregolare attaccate alla matrice corrispondono probabilmente a un macrofago alveolare e a un fibroblasto. Sulla superficie sono visibili sottili elementi fibrillari e filamentosi, coerenti con le fibre di collagene ed elastina che forniscono resistenza alla trazione ed elasticità alla parete settale. Le cavità circostanti indicano spazi aerei alveolari, che facilitano lo scambio gassoso. Crediti: Moises Selman
Nel marzo 2025, uno studio di fase II e III s un composto chiamato Bexotegrast, sviluppato da Pliant Therapeutics a South San Francisco, in California, è stato interrotto a causa di eventi avversi nei gruppi di trattamento. Tra questi, un peggioramento dei sintomi della fibrosi polmonare idiopatica (IPF) e un rischio maggiore di decesso e di ospedalizzazione per problemi respiratori. “Nonostante tutta la tecnologia e tutto sembrasse sensato, non ha funzionato“, afferma Jenkins, che è stato coinvolto in gran parte della ricerca che ha ispirato lo sviluppo di questo farmaco. “La biologia a supporto del bexotegrast era buona”, afferma lo pneumologo Paul Wolters dell’Università della California, San Francisco. “Ma è difficile trovare il giusto equilibrio tra efficacia e tossicità”.
Questa battuta d’arresto ha spinto a riconsiderare l’opportunità di colpire questa via. “Questi farmaci hanno un che di assurdo”, afferma Maher. “Probabilmente hanno un effetto antifibrotico, ma aumentano anche la suscettibilità al danno polmonare acuto”. “Di conseguenza”, conclude, “le integrine sono fuori discussione come bersaglio per il trattamento della fibrosi polmonare idiopatica“.
Jenkins concorda: “Per colpire le integrine, la finestra ‘giusta’ è molto piccola”, afferma.
Alcuni dei suoi colleghi, tuttavia, hanno scoperto altri percorsi coinvolti nell’attivazione del TGF-β che potrebbero rappresentare bersagli più efficaci. Nei polmoni danneggiati dalla fibrosi polmonare idiopatica (IPF), un programma di sviluppo dormiente chiamato segnalazione di Wnt viene spesso erroneamente riattivato. Questo innesca direttamente la fibrosi e amplifica il segnale del TGF-β. Un composto chiamato Rentosertib promette di agire su un enzima regolatore chiave nel percorso di Wnt, chiamato TNIK, che potrebbe contribuire a sopprimere la sua attivazione aberrante e quella del TGF-β.
I risultati di uno studio di fase 2 condotto da Insilico Medicine a Cambridge, Massachusetts, hanno dimostrato che il farmaco è generalmente sicuro e ben tollerato. Alla dose più elevata, i partecipanti hanno riscontrato un aumento statisticamente significativo della loro CVF nell’arco di 12 settimane, rispetto a un calo nel gruppo placebo. Delle 18 persone che hanno ricevuto la dose più elevata, 4 hanno dovuto interrompere anticipatamente il trattamento a causa di effetti collaterali avversi come tossicità epatica e diarrea.
Terapie più tollerabili
Nerandomilast agisce sul processo patologico in una fase ancora più precoce. Questo farmaco inibisce un enzima, la fosfodiesterasi 4B, che sopprime una molecola chiamata AMP ciclico. In circostanze normali, l’AMP ciclico rallenta i processi infiammatori alla base dell’attivazione del TGF-β. Uno studio di fase III su Nerandomilast condotto dall’azienda farmaceutica Boehringer Ingelheim si è concluso a settembre 2024. Lo studio ha raggiunto i suoi endpoint primari: ha rallentato il tasso di declino della funzionalità polmonare di oltre un terzo nel corso di un anno, rispetto sia al solo placebo che a placebo e nintedanib. “Ero molto scettico”, afferma Wolters. “Ma sono contento di ricredermi. Credo nei dati, che sono molto coerenti”.
Fondamentalmente, lo studio ha anche rilevato che il numero di persone che hanno abbandonato lo studio a causa di eventi avversi era lo stesso tra coloro che ricevevano nerandomilast e quelli nel gruppo placebo, un notevole miglioramento della tollerabilità rispetto ad altri trattamenti. La diarrea è un effetto collaterale del Nerandomilast, ma raramente è stata così grave da indurre i partecipanti allo studio ad abbandonare. “Dal punto di vista degli effetti collaterali, è sicuramente un vincitore”, afferma Jenkins.
I ricercatori hanno anche tentato di colpire un enzima presente nel tessuto polmonare danneggiato, chiamato autotaxina. Questo enzima coordina la produzione di un lipide chiamato acido lisofosfatidico (LPA), che si lega a un recettore sui fibroblasti per reclutarli nel sito della lesione. Due ampi studi di fase III che indagavano l’inibitore dell’autotaxina ziritaxestat sono stati interrotti nel febbraio 2021 dopo che il farmaco non è riuscito ad avere un effetto significativo sul declino della FVC. Anche la mortalità è stata più elevata nei pazienti che hanno assunto il farmaco rispetto a quelli che hanno ricevuto un placebo.
Una spiegazione per questo fallimento è che il blocco dell’autotassina o dell’LPA non risolve completamente il problema biologico; il recettore dell’LPA o il percorso potrebbero comunque essere attivati da una via diversa. “Ci sono molte possibilità di ridondanza nel sistema”, afferma Jenkins. I ricercatori sperano che un altro farmaco che ha come bersaglio l’LPA, attualmente in fase di studio, chiamato Admilparant, possa impedire che ciò accada.
L’Admilparant non limita la produzione di LPA, ma piuttosto blocca il suo recettore sulla superficie dei fibroblasti. “La speranza è che inibendo invece il recettore chiave, potremmo ottenere i benefici della specificità”, afferma Maher. Uno studio di fase II a cui Maher ha partecipato, ha concluso che l’Admilparant ha rallentato significativamente il declino della FVC nell’arco di 26 settimane, senza causare diarrea. Lo sviluppatore del composto, l’azienda farmaceutica statunitense Bristol Myers Squibb, sta ora pianificando uno studio di fase III.
Si ritiene che la fibrosi polmonare idiopatica (IPF) sia innescata da danni alle cellule epiteliali che rivestono gli alveoli. Un altro approccio terapeutico mira a fermare la fibrosi polmonare idiopatica (IPF) prima che si manifesti, promuovendo la riparazione di tali cellule. Un composto chiamato Buloxibutid, sviluppato da Vicore Pharma a Göteborg, in Svezia, attiva il recettore dell’angiotensina II di tipo 2, che sopprime l’infiammazione e promuove la riparazione cellulare. I partecipanti sono ora arruolati in uno studio di fase II. Qualsiasi tentativo di intervenire ancora più vicino all’insorgenza della malattia dipenderà da una migliore diagnosi della malattia.
Poiché il farmaco Nerandomilast ha effetti collaterali gastrointestinali meno gravi rispetto ai farmaci più vecchi per la IPF, il trattamento dovrebbe essere più tollerato per le persone che non presentano ancora sintomi gravi. Questo, a sua volta, potrebbe facilitare il reclutamento di partecipanti per studi su questa fase precoce della malattia.
Leggi anche:Fibrosi polmonare idiopatica: la FDA approva Jascayd
In definitiva, potrebbe essere necessario un approccio più olistico. “Il trattamento della fibrosi polmonare idiopatica (IPF) dovrebbe probabilmente essere una combinazione di trattamenti mirati a diverse fasi del processo“, afferma Selman. Man mano che i ricercatori continuano a svelare le origini della condizione, potrebbero passare dal tentativo di rallentare la progressione alla promozione attiva della riparazione. Questo potrebbe trasformare una malattia fatale in una cronica, o addirittura curarla del tutto, permettendo a milioni di persone di riprendere fiato.
Fontee: Natura