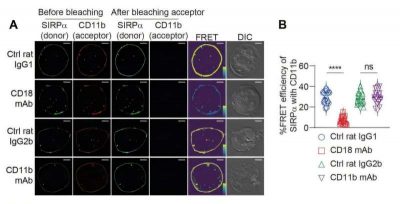
Immunoterapia- immagine: SIRPα interagisce con CD18, mentre SLAMF7 interagisce con CD11b. (A e B) Sono stati eseguiti test FRET utilizzando SIRPα marcata con donatore, CD11b marcata con accettore e CD18 non marcato. I dati mostrano (A) immagini rappresentative di microscopia confocale e (B) dati compilati. Crediti: Science Immunology.
Uno studio condotto da André Veillette, ricercatore presso il Montreal Clinical Research Institute (IRCM) e Professore presso la Facoltà di Medicina dell’Università di Montreal, getta nuova luce sulla complessità del sistema immunitario e sul suo ruolo nella cura del cancro.
Lo studio, pubblicato su Science Immunology, evidenzia come una comprensione più approfondita dei “freni” immunitari potrebbe portare a terapie più efficaci.
Il sistema immunitario utilizza meccanismi integrati, noti come checkpoint immunitari inibitori, per prevenire gli attacchi alle cellule sane. Sebbene siano essenziali per mantenere l’equilibrio, questi checkpoint possono anche impedire al sistema immunitario di attaccare le cellule tumorali. Per contrastare questo fenomeno, gli scienziati hanno sviluppato dei bloccanti dei checkpoint, una classe di farmaci che rilasciano questi freni e aiutano il sistema immunitario a combattere il cancro. Tuttavia, questi trattamenti non funzionano per tutti i pazienti o per tutti i tipi di cancro.
“I percorsi dei checkpoint sono molto più complessi di quanto pensassimo in passato”, spiega il Dott. Zhenghai Tang, autore principale dello studio ed ex ricercatore nel laboratorio del Dott. André Veillette presso l’IRCM, ora con sede presso l’Università di Macao. “Per migliorare i trattamenti, dobbiamo capire come funzionano questi freni a livello molecolare”.
Lo studio si è concentrato su due molecole chiave che controllano il sistema immunitario: SIRPα, presente sulle cellule immunitarie chiamate macrofagi e CD47, presente in molte cellule, comprese quelle tumorali. Quando queste due molecole interagiscono, inviano un segnale “non mangiarmi” che impedisce ai macrofagi di distruggere le cellule tumorali.
Bloccando l’interazione tra SIRPα e CD47, i ricercatori sono riusciti a ridurre il segnale inibitorio di circa il 50%. Sorprendentemente, la metà rimanente del segnale persisteva anche senza CD47, il che suggerisce che SIRPα può sopprimere le risposte immunitarie attraverso altri percorsi.
Questa scoperta aiuta a spiegare perché le terapie mirate esclusivamente al CD47 hanno avuto un successo limitato.
“Per rendere questi trattamenti più efficaci”, afferma il Dott. Tang, “potremmo dover bloccare tutti i modi in cui SIRPα sopprime il sistema immunitario, non solo il suo legame con CD47”.
Leggi anche: Sbloccare il sistema immunitario con l’immunoterapia
Astratto
Questa ricerca sottolinea quanto sia complesso il sistema immunitario e perché sia fondamentale comprendere come interagiscono le sue molecole. Per sviluppare trattamenti più efficaci, come gli anticorpi monoclonali progettati per colpire con precisione le molecole presenti sulle cellule tumorali, gli scienziati devono comprendere meglio questi meccanismi. Un’altra sfida consiste nel migliorare il modo in cui i risultati degli studi sugli animali possono essere tradotti in biologia umana, in modo che le scoperte in laboratorio portino in modo più affidabile a terapie concrete“.
Mentre i ricercatori continuano a svelare i meccanismi complessi della regolazione immunitaria, scoperte come questa aprono la strada a terapie contro il cancro più sicure, intelligenti e personalizzate.
Fonte: Science Immunology