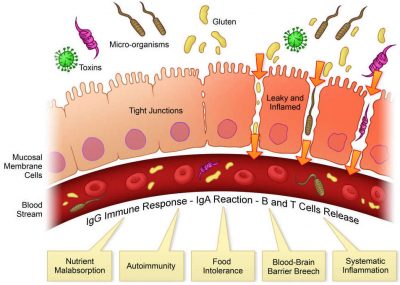
Permeabilità intestinale-immagine credit public domain.
Il tratto gastrointestinale presenta una delle barriere più lunghe tra l’ambiente e la circolazione sistemica, che si estende fino a 40 metri quadrati. Questa barriera è composta da uno strato di muco, microbiota commensale, epitelio intestinale e cellule immunitarie situate nella lamina propria. Lo strato di muco sopra l’epitelio intestinale lo protegge dal contenuto all’interno del lume intestinale. Il microbiota commensale supporta la funzione di barriera, modella le risposte immunitarie intestinali e sistemiche e inibisce i batteri patogeni stimolando direttamente le cellule epiteliali, producendo nutrienti e metaboliti essenziali per la salute degli enterociti e influenzando l’innesco del sistema immunitario. La barriera semipermeabile epiteliale contribuisce al mantenimento dell’omeostasi intestinale consentendo selettivamente ai nutrienti di attraversare il lume intestinale nell’ambiente interno, per raggiungere la circolazione sistemica, controllando al contempo il passaggio di agenti patogeni batterici, allergeni e tossine.
La permeabilità intestinale si riferisce alle proprietà funzionali della barriera intestinale ed è caratterizzata principalmente da meccanismi di trasporto paracellulare e transcellulare. La via paracellulare, regolata dalle giunzioni strette, consente il passaggio di ioni, acqua e grandi composti idrofili, mentre la via transcellulare facilita il passaggio di proteine, zuccheri, amminoacidi e batteri, tipicamente tramite trasporto mediato da trasportatori. L’interruzione di una delle due vie può influenzare l’omeostasi della barriera, alterare la permeabilità e potenzialmente portare a malattie.
Vari fattori, tra cui componenti dietetici, predisposizione genetica, farmaci (ad esempio, FANS e antibiotici), consumo di alcol, attività fisica intensa, stress psicologico o ambientale, gravidanza, agenti patogeni, malattie sistemiche, condizioni infiammatorie e citochine, disturbi metabolici tra cui l’obesità e tensioattivi (ad esempio, acidi biliari ed emulsionanti) possono alterare l’omeostasi della barriera e aumentare la permeabilità, portando a “intestino permeabile”.
Questa “permeabilità” consente il passaggio di microrganismi, allergeni e tossine che incitano l’infiammazione localmente nell’intestino e il passaggio nella circolazione sistemica. “L’intestino permeabile” è stato implicato in un’ampia gamma di malattie sistemiche (tra cui diabete mellito di tipo 2, obesità), malattie neuropsichiatriche (ad esempio, malattia di Alzheimer, morbo di Parkinson, disturbi dello spettro autistico, disturbo depressivo maggiore) e malattie autoimmuni (ad esempio, psoriasi, malattie reumatologiche e uveite), oltre a malattie intestinali (ad esempio, malattia infiammatoria intestinale (IBD), sindrome dell’intestino irritabile (IBS), celiachia).
Sono state suggerite numerose strategie per affrontare la disfunzione della barriera intestinale, come terapie immunitarie dirette, blocco dei fattori di segnalazione, introduzione di microbi specifici, trapianto di microbiota fecale, utilizzo di metaboliti microbici, probiotici, targetdi fattori regolatori indotti da malattie, trattamenti ormonali, trattamento di condizioni sottostanti, integrazione alimentare e mantenimento di una dieta sana e benessere generale. Questa sezione si concentra sui fattori dietetici e sui metaboliti microbici e nutrienti, sulla base di una revisione della letteratura recente e delle versioni aggiornate dei rapporti scritti da Khoshbin e Camilleri e Camilleri e Vella.
La fibra alimentare è un polimero di carboidrati composto da 10 o più monomeri che non vengono né assorbiti né digeriti nell’intestino tenue. I quattro sottogruppi di fibre alimentari su cui si concentra principalmente la ricerca sono gli oligosaccaridi resistenti, i polisaccaridi non amidacei, gli amidi resistenti e le sostanze associate. Le fonti alimentari di oligosaccaridi resistenti includono vari legumi, verdure, frutta e prodotti vegetali specifici come la radice di cicoria e la soia. I polisaccaridi non amidacei, come cellulosa, emicellulosa e pectine, si trovano in cereali, granaglie, frutta e verdura, mentre gli amidi resistenti provengono da alimenti come cereali, banane verdi e prodotti trasformati.
Inoltre, sostanze non carboidratiche associate come lignina, cere e chitine sono presenti negli strati esterni dei chicchi di cereali, nelle secrezioni degli insetti e negli esoscheletri dei crostacei. Questi tipi di fibre sono considerati prebiotici poiché stimolano i batteri benefici per la salute intestinale e aiutano ad aumentare le catene corte di acidi grassi (SCFA), il che migliora anche l’integrità della barriera intestinale.
Gli SCFA, prodotti dalla fermentazione delle fibre alimentari da parte del microbiota intestinale, svolgono un ruolo cruciale nella salute del colon e nella comunicazione microbiota-intestino-cervello, fornendo il 5-10% del fabbisogno energetico basale umano. La ricerca si è concentrata su tre SCFA: acetato, butirrato e propionato.
L’acetato, SCFA più abbondante, supporta la produzione di ATP, mentre gli altri SCFA abbassano complessivamente il pH del colon per inibire i batteri patogeni e modulare l’infiammazione attraverso vari meccanismi cellulari. Il butirrato, in particolare, ha significativi benefici per la salute, inclusa la prevenzione del cancro, mentre il propionato può ridurre il colesterolo nel sangue ed entrambi contribuiscono alla comunicazione lungo l’asse microbiota-intestino-cervello grazie alle loro proprietà neuroattive.
Gli oligosaccaridi resistenti includono i frutto-oligosaccaridi (inulina a catena corta), che sono fruttani lineari β-(2 → 1) derivati dall’idrolisi enzimatica dell’inulina a catena lunga o sintetizzati dal saccarosio. I galatto-oligosaccaridi sono costituiti da due a otto unità saccaridiche con glucosio e galattosio e possono essere presenti nel latte umano o sintetizzati dal lattosio. Altri oligosaccaridi resistenti includono tipi non digeribili come l‘oligosaccaride di konjac. Incorporare un’ampia gamma di frutta, verdura, vari legumi e soia (prodotti oligosaccaridici resistenti) nellsa dieta può contribuire notevolmente a migliorare la salute intestinale, soprattutto considerando le recenti diete occidentalizzate che sono diventate molto popolari.
Mistry et al. hanno dimostrato in uno studio in vivo su topi maschi alimentati con una dieta di tipo occidentale che l’integrazione di oligosaccaridi resistenti ha ridotto significativamente l’aumento di peso corporeo, l’accumulo di grasso, la resistenza all’insulina e i livelli di colesterolo plasmatico, alterando anche la composizione del microbiota intestinale in un modo che potrebbe favorire la salute metabolica. Questi risultati suggeriscono che gli oligosaccaridi resistenti potrebbero avere un potenziale terapeutico per migliorare i marcatori metabolici e ridurre il rischio di sindrome metabolica.
I polisaccaridi non amidacei includono la cellulosa, il principale componente strutturale delle pareti cellulari vegetali, e le emicellulose, che sono diversi polisaccaridi delle pareti cellulari presenti in frutta, verdura e cereali. Anche le pectine, presenti nelle pareti cellulari vegetali, e varie gomme e mucillagini di piante, microbi e alghe, sono polisaccaridi non amidacei chiave. Inoltre, i β-glucani e i β-fruttani, come l’inulina delle radici di cicoria, sono fibre non digeribili resistenti alla digestione enzimatica ma fermentabili nel colon. In uno studio in vivo con volontari maschi sani, è stato dimostrato che l’inulina riduce il rapporto lattulosio-mannitolo (L/M) e la zonulina sierica, aumentando al contempo il GLP-2 della mucosa dopo 8 settimane.
Tuttavia, i metodi dello studio non erano ottimali, tra cui l’uso di sonde per il glucosio inappropriate, tempi di raccolta delle urine limitati e livelli sierici che potrebbero non aver indicato accuratamente la permeabilità intestinale.