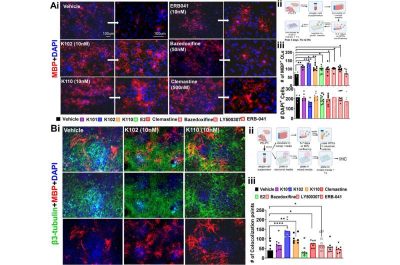
Sclerosi multipla-immagine crediti: Scientific Reports
La sclerosi multipla (SM) è una malattia autoimmune cronica che colpisce oltre 2,9 milioni di persone in tutto il mondo. Si verifica quando il sistema immunitario attacca erroneamente la guaina mielinica, l’isolamento protettivo che circonda le fibre nervose, causando l’interruzione dei segnali nervosi tra il cervello e il corpo. I sintomi possono includere intorpidimento, formicolio, perdita della vista e paralisi.
Sebbene i trattamenti attuali possano ridurre l’infiammazione, non esistono ancora terapie in grado di proteggere i neuroni o di ripristinare la guaina mielinica danneggiata. I ricercatori hanno ora compiuto un importante passo avanti nello sviluppo di una terapia di questo tipo. Hanno identificato due composti in grado di rimielinizzare gli assoni danneggiati.
Pubblicata sulla rivista Scientific Reports, la ricerca è stata guidata da Seema Tiwari-Woodruff, Professoressa di scienze biomediche presso la facoltà di medicina dell’Università della California, Riverside, e da John Katzenellenbogen, Professore di chimica presso l’Università dell’Illinois Urbana-Champaign.
“Il nostro lavoro rappresenta più di un decennio di collaborazione, con gli ultimi quattro anni concentrati sull’identificazione e l’ottimizzazione di nuovi farmaci candidati che mostrano un forte potenziale per il trattamento della SM e potenzialmente di altre malattie neurologiche che comportano demielinizzazione“, ha affermato Tiwari-Woodruff.
I ricercatori sono riusciti a lanciare un programma concesso in licenza da Cadenza Bio, Inc. L’azienda sta ora procedendo verso la valutazione clinica come potenziale terapia innovativa per le persone affette da SM.
Dalla scoperta allo sviluppo
Il progetto si basa su ricerche precedenti su un composto chiamato cloruro di indazolo, noto per promuovere la rimielinizzazione e modulare il sistema immunitario nei modelli murini di SM. “Pur essendo efficace, il cloruro di indazolo non aveva le proprietà farmacologiche e la brevettabilità necessarie per lo sviluppo clinico e gli investimenti commerciali”, ha affermato Tiwari-Woodruff.
In collaborazione con i chimici Katzenellenbogen e Sung Hoon Kim dell’UIUC, che hanno sintetizzato i composti, il gruppo di ricerca di Tiwari-Woodruff, guidato dal neolaureato dell’UCR Micah Feri, ha esaminato oltre 60 analoghi del cloruro di indazolo. Questa collaborazione ha identificato due candidati principali, K102 e K110, che hanno mostrato maggiore sicurezza, efficacia e proprietà farmacologiche sia nei modelli murini che nelle cellule umane.
Tra i due, K102 è emerso come il composto principale. I ricercatori hanno scoperto che non solo promuove la rimielinizzazione, ma modula anche la funzione immunitaria, un equilibrio importante per le terapie contro la SM. Ha anche mostrato risultati promettenti negli oligodendrociti umani, le cellule mielinizzanti del sistema nervoso centrale, derivati da cellule staminali pluripotenti indotte, suggerendo il potenziale di traslabilità tra i modelli animali e la malattia umana.
In condizioni normali, le cellule precursori degli oligodendrociti maturano in oligodendrociti produttori di mielina per riparare la mielina danneggiata. Nella SM, tuttavia, questo processo di riparazione naturale spesso fallisce, causando danni permanenti ai nervi. Una rimielinizzazione efficace attraverso un composto come il K102 potrebbe ripristinare una conduzione nervosa più rapida e contribuire a ridurre la disabilità a lungo termine associata alla malattia.
“Anche K110 è un candidato valido”, ha affermato Tiwari-Woodruff. “Ha effetti leggermente diversi sul sistema nervoso centrale e potrebbe essere più adatto per altre condizioni come lesioni del midollo spinale o traumi cranici, quindi lo stiamo tenendo in fase di sperimentazione“.
Leggi anche: Sclerosi multipla: danno mitocondriale precoce e perdita di mielina legati al danno cerebrale
Più di un decennio in lavorazione
Tiwari-Woodruff e Katzenellenbogen lavorano insieme da oltre 12 anni. Sebbene l’attenzione iniziale sia rivolta alla SM, il team ritiene che K102 e K110 possano in futuro essere applicati ad altre patologie che comportano danni neuronali, tra cui ictus e neurodegenerazione.
Cadenza Bio sta ora portando avanti K102 attraverso gli studi non clinici necessari a supportare i primi studi clinici sull’uomo.
“Speriamo che le sperimentazioni cliniche possano iniziare presto”, ha affermato Tiwari-Woodruff. “È stato un lungo viaggio, ma questo è lo scopo della scienza traslazionale: trasformare la scoperta in un impatto concreto nel mondo reale“.
Fonte:Scientific Reports