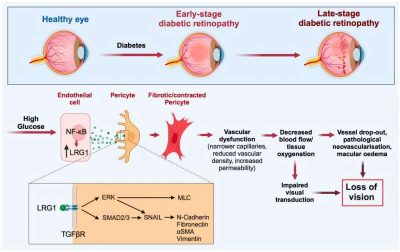
Retinopatia diabetica- modalità d’azione proposta di LRG1 nella retinopatia diabetica. Credit: Science Translational Medicine
Un team guidato da scienziati dell’UCL ha identificato una proteina chiave che scatena la retinopatia diabetica, una condizione causata da elevati livelli di zucchero nel sangue che danneggiano i vasi sanguigni della retina e una delle principali cause di perdita della vista tra gli adulti in età lavorativa.
La ricerca sui topi ha il potenziale di rivoluzionare il modo in cui viene trattata la malattia, spostando la terapia dalla gestione dei danni in fase avanzata alla prevenzione della perdita della vista prima che inizi.
I risultati, pubblicati su Science Translational Medicine, rivelano che una proteina chiamata LRG1 svolge un ruolo fondamentale nell’innescare la fase iniziale del danno retinico dopo lo sviluppo del diabete. LRG1 provoca una costrizione eccessiva delle cellule che avvolgono i vasi sanguigni più piccoli dell’occhio, “spremendoli”, riducendo l’apporto di ossigeno alla retina e ponendo le basi per un deterioramento visivo a lungo termine.
È importante notare che quando i ricercatori hanno bloccato l’attività di LRG1 nei modelli murini di diabete, sono riusciti a prevenire questo danno precoce e a preservare la sana funzionalità oculare.
L’autrice principale, la Dott.ssa Giulia De Rossi (UCL Institute of Ophthalmology), ha dichiarato: “La nostra scoperta dimostra che la patologia oculare diabetica inizia prima di quanto pensassimo e che LRG1 è un fattore chiave in questo danno precoce. Prendere di mira questa proteina potrebbe offrirci un modo per proteggere la vista prima che si verifichino danni gravi e prevenire, anziché curare, la cecità in milioni di persone affette da diabete”.
La retinopatia diabetica colpisce sia le persone con diabete di tipo 1 che di tipo 2. In genere, viene trattata solo quando compaiono i sintomi, come la vista offuscata o distorta, quando ormai il danno irreversibile è già in atto. Anche in quel caso, le terapie attuali, che hanno come bersaglio un’altra proteina, il VEGF, funzionano solo per circa il 50% dei pazienti e raramente invertono i danni esistenti in modo significativo.
Questa nuova ricerca dimostra che LRG1 inizia a causare danni oculari molto prima del VEGF, rendendolo un nuovo promettente bersaglio terapeutico. A differenza dei trattamenti attuali, un trattamento che blocca LRG1 potrebbe intervenire prima che la vista peggiori e prevenire del tutto la progressione della malattia.
La Dott.ssa Faye Riley, responsabile della comunicazione di ricerca presso Diabetes UK, ha commentato: “Quasi un terzo degli adulti con diabete presenta alcuni segni di retinopatia, una delle complicanze più temute della patologia. Identificando la causa principale del danno precoce e offrendo un nuovo percorso terapeutico, questa ricerca è estremamente promettente per la protezione della vista del crescente numero di persone con diabete in tutto il mondo“.
I ricercatori dell’UCL hanno già sviluppato un farmaco anti-LRG1 collaudato, attualmente in fase di ulteriori studi preclinici e che potrebbe essere pronto per la sperimentazione clinica sull’uomo nel prossimo futuro. I ricercatori ritengono che questa terapia non solo arresterà l’insorgenza della retinopatia diabetica, ma potrà anche essere efficace nelle fasi avanzate della malattia, in cui LRG1 continua a svolgere un ruolo.
Spiegano gli autori:
“La retinopatia diabetica (DR) è una complicanza comune del diabete mellito e una delle principali cause di deficit visivo e cecità nella popolazione in età lavorativa. La fase iniziale della malattia è caratterizzata da disfunzione capillare retinica, ma i meccanismi con cui l’iperglicemia altera l’omeostasi capillare in questa fase iniziale sono poco compresi, il che rappresenta un ostacolo allo sviluppo di trattamenti precoci efficaci. Abbiamo utilizzato due modelli murini di diabete di tipo I che replicano le caratteristiche precoci della patologia vascolare retinica umana. Sia nel modello con streptozotocina (STZ), in cui l’ipoinsulinemia è indotta chimicamente, sia nel modello Ins2Akita, che la sviluppa spontaneamente a causa di una mutazione nel gene dell’insulina, abbiamo osservato un’induzione precoce del gene della glicoproteina secreta α-2-glicoproteina 1 ricca di leucina ( Lrg1 ). Utilizzando i topi Ins2Akita, abbiamo dimostrato che l’induzione di Lrg1 precedeva quella del fattore di crescita endoteliale vascolare A ( Vegfa ). LRG1 ha innescato la disfunzione microvascolare retinica modificando la segnalazione del fattore di crescita trasformante-β (TGFβ) nei periciti, guidando la transdifferenziazione verso un fenotipo fibrotico più contrattile, con conseguente restringimento dei capillari e ispessimento della membrana basale. Utilizzando modelli computazionali, abbiamo dimostrato che questi cambiamenti vascolari precoci compromettevano il flusso sanguigno retinico e l’apporto di ossigeno, in linea con un difetto nella trasduzione visiva osservato in entrambi i modelli. Questo fenotipo retinico precoce potrebbe essere ripristinato mediante knockout di Lrg1 o mediante trattamento con un anticorpo bloccante la funzione di LRG1 sia nei topi STZ che Ins2Akita. Questi risultati dimostrano che LRG1 è un fattore determinante della disfunzione vascolare che contribuisce all’insorgenza della DR e si presenta come un potenziale bersaglio terapeutico preventivo“.
Il coautore, il Professor John Greenwood (UCL Institute of Ophthalmology), esperto mondiale nella biologia di LRG1, ha dichiarato: “Questo studio fornisce informazioni fondamentali sulla malattia e dimostra che il targeting terapeutico di LRG1 ha un reale potenziale clinico. La scoperta che LRG1 è un fattore scatenante precoce della retinopatia diabetica è estremamente entusiasmante”.
Leggi anche:Empagliflozin riduce la progressione della retinopatia diabetica
Il coautore, il Professor Emerito Stephen Moss (UCL Institute of Ophthalmology), ha aggiunto: “La buona notizia che accompagna questi risultati è che abbiamo già sviluppato una terapia LRG1 pronta per la sperimentazione clinica. Ciò potrebbe fornire una nuova ed efficace opzione per i pazienti, soprattutto per quelli nelle fasi iniziali della malattia che non rispondono ai trattamenti esistenti”.