I batteri che causano malattie gengivali possono raggiungere il cuore, causando danni che aumentano il rischio di fibrillazione atriale. Una buona igiene orale può contribuire a proteggere la salute del cuore.
Tentato di evitare l’uso del filo interdentale? Potrebbe non valerne la pena. Un nuovo studio dell’Università di Hiroshima (HU) ha scoperto che il batterio della malattia gengivale Porphyromonas gingivalis (P. gingivalis) può entrare nel flusso sanguigno e raggiungere il cuore. Una volta lì, contribuisce alla formazione di tessuto cicatriziale, noto come fibrosi, che distorce la struttura del cuore, interrompe i segnali elettrici e aumenta il rischio di fibrillazione atriale (FA).
I medici hanno osservato da tempo che le persone affette da parodontite, una forma diffusa di malattia gengivale, hanno maggiori probabilità di sviluppare problemi cardiovascolari. Una recente meta-analisi ha collegato la parodontite a un rischio del 30% maggiore di sviluppare fibrillazione atriale (FA), un grave disturbo del ritmo cardiaco associato a ictus, insufficienza cardiaca e altre condizioni potenzialmente letali. A livello globale, il numero di casi di FA è aumentato drasticamente, passando da 33,5 milioni nel 2010 a quasi 60 milioni nel 2019, spingendo i ricercatori a indagare su come la malattia gengivale possa essere alla base di questo aumento.
Studi precedenti hanno identificato l’infiammazione come un fattore chiave. Quando le cellule immunitarie gengivali rispondono a un’infezione, rilasciano segnali chimici che possono entrare nel flusso sanguigno. Questi segnali possono innescare un’infiammazione diffusa, potenzialmente dannosa per organi ben oltre la bocca.
Ma l’infiammazione non è l’unica minaccia che sfugge alle gengive infiammate. I ricercatori hanno scoperto DNA di batteri orali dannosi nel muscolo cardiaco, nelle valvole e persino nelle placche arteriose grasse. Tra questi, P. gingivalis ha attirato particolare attenzione per il suo presunto ruolo in una crescente lista di malattie sistemiche, tra cui l’Alzheimer , il diabete e alcuni tipi di cancro. È stato precedentemente rilevato nel cervello, nel fegato e nella placenta. Ma come riesca ad attecchire nel cuore non è chiaro.
Questo studio, pubblicato su Circulation, fornisce la prima chiara prova che P. gingivalis nelle gengive può insinuarsi nell’atrio sinistro sia nei modelli animali che negli esseri umani, indicando un potenziale percorso microbico che collega la parodontite alla fibrillazione atriale.
“La relazione causale tra parodontite e fibrillazione atriale è ancora sconosciuta, ma la diffusione dei batteri parodontali attraverso il flusso sanguigno potrebbe collegare queste condizioni”, ha affermato Shunsuke Miyauchi, primo autore dello studio e professore associato presso la Graduate School of Biomedical and Health Sciences dell’HU.
Tra i vari batteri parodontali, P. gingivalis è altamente patogeno per la parodontite e alcune malattie sistemiche extraorali. In questo studio, abbiamo affrontato queste due domande chiave: P. gingivalis si trasferisce all’atrio sinistro dalla lesione parodontale? E in tal caso, induce la progressione della fibrosi atriale e della fibrillazione atriale?
Esaminare il collegamento tra malattia gengivale e fibrillazione atriale
Per simulare come P. gingivalis potrebbe fuoriuscire dalla bocca e devastare altre zone, i ricercatori hanno creato un modello murino utilizzando il ceppo aggressivo W83 del batterio. Hanno diviso topi maschi di 13 settimane in due gruppi: a uno è stato introdotto il ceppo nella polpa dentale, mentre l’altro è rimasto infetto. Ciascuno è stato ulteriormente suddiviso in sottogruppi e osservato per 12 o 18 settimane per monitorare i rischi cardiovascolari di un’esposizione prolungata.
La stimolazione intracardiaca, una tecnica diagnostica per l’aritmia, non ha rivelato alcuna differenza nel rischio di fibrillazione atriale tra topi infetti e non infetti a 12 settimane. Tuttavia, alla settimana 18, i test hanno dimostrato che i topi esposti al batterio avevano una probabilità sei volte maggiore di sviluppare aritmie cardiache, con un tasso di inducibilità della fibrillazione atriale del 30% rispetto a solo il 5% nel gruppo di controllo.
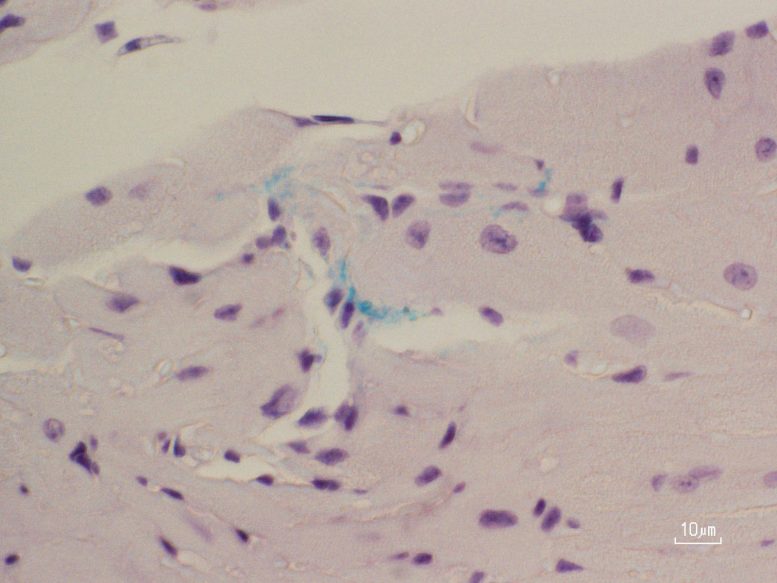
Per verificare se il loro modello replicasse accuratamente la parodontite, i ricercatori hanno esaminato le lesioni mascellari e ne hanno individuato i segni rivelatori. Hanno rilevato carie della polpa dentale e microascessi causati da P. gingivalis . Ma il danno non si è fermato lì. Hanno anche individuato il batterio nell’atrio sinistro del cuore, dove il tessuto infetto era diventato rigido e fibroso. Utilizzando l’amplificazione isotermica mediata da loop per rilevare firme genetiche specifiche, il team ha confermato che il ceppo di P. gingivalis che avevano introdotto era presente nel cuore. Al contrario, i topi non infetti avevano denti sani e nessuna traccia del batterio nei campioni di tessuto cardiaco.
Dodici settimane dopo l’infezione, i topi esposti a P. gingivalis mostravano già una maggiore cicatrizzazione cardiaca rispetto alle loro controparti non infette. A 18 settimane, la cicatrizzazione nei topi infetti era salita al 21,9%, rispetto al 16,3%, probabilmente correlato all’invecchiamento, del gruppo di controllo, suggerendo che P. gingivalis potrebbe non solo innescare danni cardiaci precoci, ma anche accelerarli nel tempo.
E questa preoccupante connessione non è stata osservata solo nei topi. In un altro studio sull’uomo, i ricercatori hanno analizzato il tessuto atriale sinistro di 68 pazienti con fibrillazione atriale sottoposti a intervento chirurgico al cuore. Anche lì è stato trovato P. gingivalis , in quantità maggiori nelle persone con grave malattia gengivale.
Maestro dell’assalto furtivo
Studi precedenti hanno dimostrato che P. gingivalis può invadere le cellule ospiti ed eludere la distruzione da parte degli autofagosomi, la squadra di smaltimento dei rifiuti cellulari. Questa capacità di nascondersi all’interno delle cellule suggerisce un modo con cui può superare le difese immunitarie e innescare un’infiammazione sufficiente a causare danni senza essere espulso. I topi infetti hanno mostrato un picco di galectina-3, un biomarcatore della fibrosi, e una maggiore espressione di Tgfb1 , un gene legato all’infiammazione e alla formazione di cicatrici.
I risultati suggeriscono che spazzolare i denti, usare il filo interdentale e sottoporsi a controlli dentistici regolari potrebbe non solo promuovere l’igiene orale,re. Mantenere le gengive sane potrebbe bloccare la porta d’ingresso per l’ invasione di P. gingivalis . ma anche contribuire a proteggere il cuo