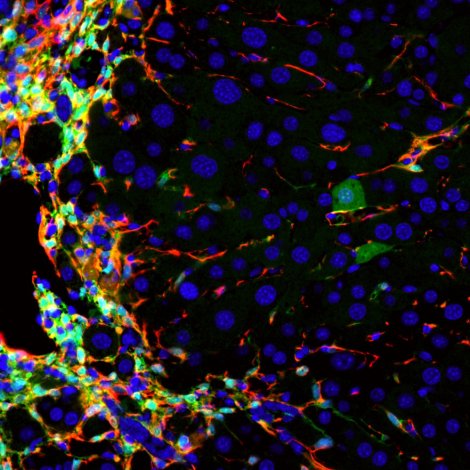
Immagine: una nuova tecnica testata sui topi è in grado di convertire le cellule che causano la malattia del fegato (rosso) in nuove cellule epatiche sane in grado di rigenerare il fegato danneggiato (verde scuro). Immagine dal Laboratorio Willenbring
Un recente studio offre una nuova speranza di trattamento per la cirrosi epatica e altre malattie del fegato.
I progressi nella ricerca sulle cellule staminali hanno permesso di convertire le cellule della pelle dei pazienti in cellule cardiache, cellule renali, cellule del fegato e molto altro, alimentando la speranza dei ricercatori che un giorno queste cellule potrebbero sostituire il trapianto di organi nei pazienti con insufficienza. Ma l’innesto con successo di queste cellule negli organi, resta una grande sfida clinica.
Ora un team di ricercatori guidato da scienziati UC San Francisco, ha dimostrato nei topi che è possibile generare nuove cellule epatiche sane all’interno dell’organo stesso. Ma c’è di più, i ricercatori hanno convertito le cellule che causano la malattia del fegato in cellule sane, riducendo in tal modo i danni al fegato e migliorando la funzione del fegato.
” La tecnica si avvale di una tecnologia di consegna virale del gene che potrebbe essere facilmente tradotta in una terapia per i pazienti con malattia epatica”, ha dichiarato Holger Willenbring, MD, PhD, Professore di chirurgia presso la UCSF e autore senior del nuovo studio pubblicato il 2 giugno 2016 sulla rivista Cell Stem Cell .
“Parte del motivo per cui questa tecnologia funziona è che il fegato è naturalmente un organo che si rigenera e per questo può affrontare bene le nuove cellule in esso introdotte. Quello che abbiamo ottenuto è che le cellule convertite non solo sono funzionalmente integrate nel tessuto epatico, ma si dividono e si espandono, portando a macchie di nuovo tessuto epatico “, ha spiegato Willenbring, che è anche Direttore associato del Liver Center at UCSF e membro del the Eli and Edythe Broad Center of Regeneration Medicine and Stem Cell Research.
Più di 600.000 pazienti soltanto negli Stati Uniti, soffrono di malattie del fegato in fase terminale o cirrosi. L’unica cura disponibile è il trapianto di fegato, ma a causa della carenza di donatori, solo 6.000 pazienti traggono beneficio da questa terapia ogni anno negli Stati Uniti, e più di 35.000 pazienti muoiono.
Il nuovo approccio si rivolge in particolare alla fibrosi epatica, la progressiva cicatrizzazione del fegato che è un driver primario della malattia epatica. La fibrosi si sviluppa quando le cellule del fegato chiamate epatociti non possono rigenerarsi abbastanza velocemente per tenere il passo ai danni causati da tossine come l’alcol o da malattie come l’epatite C o malattia del fegato grasso.
Cellule chiamate miofibroblasti cercano di riparare i danni causati dalla morte degli epatociti, con tessuto fibrotico cicatriziale. Ma questo processo è un po’ come l’applicazione di patch ad una gomma a terra: in un primo momento il patch aiuta a mantenere l’integrità strutturale del fegato, ma alla fine il fegato risulta costituito più da cerotti che da tessuto funzionale.
L’epatopatia fibrotica è una malattia a lenta progressione: una persona che contrae l’epatite C a 25 anni, può sentirsi bene per decenni, poi, improvvisamente all’età di 50 anni iniziare a sperimentare la fatica, debolezza, nausea, ecchimosi, diarrea e ittero che indicano l’insorgenza della malattia epatica allo stadio terminale.” La ragione è che il fegato può adattarsi bene ai danni causati da vari fattori purché almeno il 20 per cento del suo tessuto sia funzionale, ma una volta che il tessuto funzionale scende sotto la soglia critica, i pazienti spesso muoiono entro due anni”, spiega Willenbring.
“La fibrosi epatica non è rara”, ha aggiunto il ricercatore. “In realtà è lo stadio finale di molte malattie croniche del fegato. L’obesità, per esempio, può portare alla malattia del fegato grasso, che si prevede possa diventare la causa principale della fibrosi epatica, nei prossimi 10 anni”.
La nuova tecnica riduce i danni al fegato e aumenta la funzionalità epatica nei topi
Willenbring ha dedicato la sua carriera alla biologia delle cellule staminali per generare nuove epatociti che potrebbero essere utilizzati al posto di trapianti per il trattamento di insufficienza epatica.
Nonostante il successo degli esperimenti, Willenbring ha dovuto confrontarsi con la consapevolezza che questo approccio di terapia cellulare potrebbe non essere efficace nella maggior parte dei pazienti con insufficienza epatica a causa del groviglio di fibrosi nel fegato che compromette il successo di attecchimento delle cellule trapiantate.
Così nel corso degli ultimi cinque anni, Willenbring e il suo team, in stretta collaborazione con il laboratorio di Dirk Grimm, PhD della Heidelberg University Hospital in Germania, hanno intrapreso un approccio diverso: la conversione dei miofibroblasti fibrosi in nuovi epatociti sani nel fegato stesso .
La ricerca precedente aveva identificato un cocktail di geni che regolano le proteine in grado di convertire altri tipi di cellule in epatociti, ma il team aveva bisogno di un modo per consegnare queste istruzioni ai miofibroblasti. Dopo diversi anni di lavoro, il team ha identificato un sottotipo di virus adeno-associato (AAV) che potrebbero infettare specificamente i miofibroblasti. I ricercatori si sono focalizzati sull’ AAV che si è dimostrato sicuro ed efficace in studi di terapia genica umana, ad esempio, per la terapia della malattia da sanguinamento, emofilia B.
Il team ha dimostrato nei topi con malattia del fegato che i virus infettano i miofibroblasti ed effettivamente cambiano il destino di queste cellule e le trasformano in epatociti funzionali. Il numero di nuove cellule prodotte era relativamente basso – meno dell’uno per cento di tutti gli epatociti nei topi trattati – ma era sufficiente per ridurre la fibrosi e migliorare la funzione del fegato.
L’approccio virale è stato anche efficace nel convertire i miofibroblasti umani in una piastra di Petri, in epatociti, ma è necessaria ulteriore ricerca per preparare questo approccio per l’uso in pazienti umani.
In particolare, il laboratorio sta lavorando per confezionare il trattamento in un singolo virus, riducendo i potenziali effetti collaterali e per razionalizzarne lo sviluppo clinico. Il team sta anche lavorando per rendere i virus più specifici per i miofibroblasti.
” I nuovi risultati suggeriscono che nel fegato fibrotico questo approccio potrebbe produrre un miglioramento più efficiente e stabile della funzionalità epatica rispetto agli approcci di trapianto di cellule” , ha detto Willenbring che ha anche aggiunto che una volta che la confezione virale è ottimizzata, tale trattamento molto economico, può essere utilizzato da un’ampia gamma di strutture mediche e non solo negli ospedali di ricerca specializzati.
Willenbring è il primo a riconoscere che la nuova tecnica non sostituisce l’attuale standard di cura delle malattie del fegato.
“Un trapianto di fegato rimane la migliore opzione di trattamento”, ha detto Willenbring.” Ma aumentare la funzionalità epatica potrebbe tradursi in decenni di vita in più per questi pazienti”.