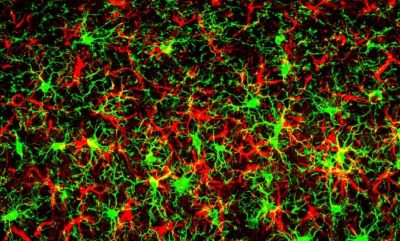
Un’immagine fluorescente mostra la gliosi reattiva – una condizione presente in molte malattie neurodegenerative – nella corteccia cerebrale indotta da GADD45G, il prodotto proteico del gene Gadd45g, espresso dagli astrociti. Gli astrociti reattivi sono mostrati in rosso e la microglia reattiva in verde, entrambi tipi comuni di cellule gliali. Credito: UT Southwestern.
“Prendere di mira la proteina GADD45g potrebbe migliorare i risultati per l’Alzheimer, il Parkinson e altre condizioni”, affermano i ricercatori dell’UTSW.
Gli scienziati dell’UT Southwestern Medical Center hanno identificato una proteina che sembra agire come un interruttore di controllo principale per la gliosi reattiva, una caratteristica importante di molte malattie neurodegenerative che si ritiene contribuisca alla loro patologia. I risultati dei ricercatori, pubblicati su Neuron, potrebbero portare a nuovi trattamenti per l’Alzheimer, il Parkinson, la malattia di Huntington e altre patologie neurodegenerative.
“La gliosi reattiva può aiutare il sistema nervoso ad adattarsi a condizioni di stress per continuare a funzionare correttamente, ma può anche essere disadattiva, causando persino la morte neuronale. Imparare a controllare questa condizione potrebbe aiutarci a proteggere le cellule dagli aspetti negativi della gliosi reattiva, modificando la traiettoria delle malattie neurodegenerative“, ha affermato Chun-Li Zhang, Ph.D., Professore di Biologia Molecolare, membro dell’Hamon Center for Regenerative Science and Medicine e Ricercatore presso il Peter O’Donnell Jr. Brain Institute dell’UT Southwestern. Il Dott. Zhang ha co-diretto lo studio con il primo autore Tianjin Shen, Ph.D., ricercatore scientifico presso lo Zhang Lab.
Più della metà del volume del sistema nervoso centrale è costituito da glia, cellule non neuronali che supportano i neuroni fornendo nutrienti, producendo isolamento e rimuovendo patogeni e cellule morte. Astrociti e microglia sono due tipi comuni di cellule gliali. Quando il sistema nervoso centrale è sottoposto a stress a causa di traumi o malattie, queste cellule proliferano e si ingrandiscono, secernendo proteine protettive, assorbendo fattori nocivi e rafforzando la barriera emato-encefalica, tutti tratti distintivi della gliosi reattiva.
“Tuttavia, questa condizione può anche avere effetti negativi”, ha spiegato il Dott. Zhang. La gliosi reattiva può danneggiare le connessioni tra i neuroni, chiamate sinapsi; limitare la rigenerazione degli assoni, le lunghe estensioni dei neuroni; aumentare la neuroinfiammazione e indurre l’apoptosi, ovvero la morte cellulare programmata. Si ritiene che questi aspetti negativi della gliosi reattiva svolgano un ruolo significativo nella patologia delle malattie neurodegenerative.
Sebbene i ricercatori abbiano identificato diverse proteine coinvolte nella gliosi reattiva, si ritiene che la loro produzione sia regolata da geni situati più a monte nella cascata di segnalazione molecolare responsabile di questa condizione. Per ricercare i principali controlli di questa condizione, il Dott. Zhang e i suoi colleghi hanno consultato un database di attività genica negli astrociti di topi dopo che queste cellule erano state esposte a una tossina batterica che causa infiammazione. Si sono subito concentrati su Gadd45g , un gene la cui attività è aumentata significativamente in risposta alla tossina.
Gadd45g fa parte di una più ampia famiglia di geni identificati come sensori dello stress nella ricerca sul cancro, ma il suo ruolo negli astrociti sani non era chiaro. Per cercare risposte, i ricercatori hanno lavorato con topi i cui astrociti erano stati alterati per sovrapprodurre GADD45G, il prodotto proteico del gene Gadd45g. Questa modifica non solo ha stimolato la gliosi reattiva negli astrociti, ma anche nelle cellule non modificate vicine. Ciò ha suggerito che gli astrociti secernessero segnali chimici per indurre la gliosi reattiva in altri tipi cellulari – una teoria che i ricercatori hanno confermato utilizzando astrociti geneticamente modificati coltivati in una capsula di Petri con neuroni. In entrambi gli esperimenti, la gliosi reattiva indotta dagli astrociti ha ridotto il numero di sinapsi neuronali e ha innescato l’infiammazione.
In un modello murino di Alzheimer grave, i ricercatori hanno riscontrato un aumento dell’attività di Gadd45g nel cervello, a supporto dell’ipotesi che il gene inneschi la gliosi reattiva che accompagna questa malattia. L’analisi dell’attività genica nelle persone affette da Alzheimer ha confermato che questo gene è sovraregolato anche nei pazienti umani. Quando i ricercatori hanno modificato geneticamente il modello per produrre più GADD45G, i sintomi della malattia sono risultati notevolmente peggiori rispetto ai modelli non modificati: i loro cervelli hanno accumulato il doppio della proteina beta-amiloide patologica e hanno mostrato un’infiammazione significativamente maggiore in età precoce.
Al contrario, l’eliminazione selettiva di Gadd45g negli astrociti ha ridotto significativamente la quantità di proteina beta-amiloide nel modello. Inoltre, la down-regulation del gene ha migliorato le capacità cognitive nel modello di Alzheimer, migliorando le prestazioni in diversi test di apprendimento e memoria.
“Nel complesso”, ha affermato il Dott. Zhang, “questi risultati suggeriscono che GADD45g funge da regolatore principale della gliosi reattiva. Trovare il modo di controllarne l’attività potrebbe in futuro migliorare la prognosi dell’Alzheimer e di altre malattie neurodegenerative”.
Leggi anche:Malattie neurodegenerative: editing del DNA mitocondriale offre nuove speranze
Altri ricercatori dell’UTSW che hanno contribuito a questo studio sono Wenjiao Tai, Ph.D., istruttore di biologia molecolare; Shuaipeng Ma, Ph.D., Xiaoling Zhong, Ph.D. e Yuhua Zou, M.Sc., ricercatori; e Dongfang Jiang, Ph.D., ricercatore post-dottorato.
Il Dott. Zhang è un borsista WW Caruth, Jr. in ricerca biomedica.
Lo studio è stato finanziato da sovvenzioni del Texas Alzheimer’s Research and Care Consortium, della Decherd Foundation e dei National Institutes of Health.
Fonte:Newsw