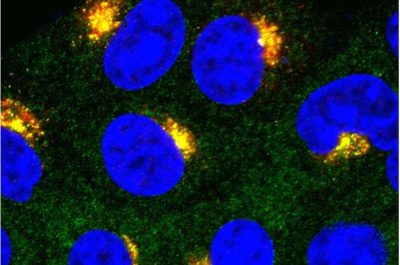
Malattie autoimmuni-immagine: questa immagine microscopica, frutto della ricerca degli scienziati dell’UT Southwestern, mostra gruppi di STING (stimolatori dei geni dell’interferone) – aree gialle vicino al nucleo cellulare in blu – sull’apparato di Golgi e sulle vescicole post-Golgi all’interno delle cellule. Crediti: UT Southwestern Medical Center.
Ricercatori dell’UT Southwestern Medical Center hanno identificato due lipidi che interagiscono con una proteina essenziale nota come stimolatore dei geni dell’interferone (STING) per innescare una risposta immunitaria nel corpo umano. Le loro scoperte, descritte in dettaglio in due articoli pubblicati contemporaneamente su Nature, potrebbero aprire la strada a nuovi modi per manipolare il sistema immunitario e combattere infezioni, cancro, malattie autoimmuni e malattie neurodegenerative.
Questi studi rivelano ulteriori livelli di regolazione del pathway cGAS-STING, sottolineando l’importanza di controllare l’attività di questo pathway affinché l’organismo possa innescare una risposta immunitaria efficace contro le infezioni, evitando al contempo reazioni autoimmuni ai propri tessuti. “È stato dimostrato che la disregolazione di questo pathway causa una varietà di malattie autoimmuni e infiammatorie“, ha affermato Zhijian “James” Chen, Ph.D., Professore di Biologia Molecolare e Direttore del Center for Inflammation Research presso l’UT Southwestern.
Il Dott. Chen, uno dei principali ricercatori al mondo sull’immunità innata, è coautore di uno studio e autore senior dell’altro. La sua scoperta del cGAS, un enzima che produce una molecola chiamata cGAMP per attivare STING, è stata riconosciuta con numerosi riconoscimenti, tra cui il Japan Prize in Life Sciences del 2026, l’Albert Lasker Basic Medical Research Award del 2024 e il Breakthrough Prize in Life Sciences del 2019.
STING è una parte fondamentale del sistema immunitario innato, che fornisce una protezione ampia e precoce contro gli invasori esterni, come virus, batteri, funghi e parassiti, nonché contro il cancro. Un fattore scatenante dell’attività immunitaria innata è il DNA presente nel citoplasma delle cellule. cGAS rileva questo DNA e produce cGAMP che si lega a STING, che risiede in un organello cellulare chiamato reticolo endoplasmatico (ER) quando è inattivo.

Dopo il legame con cGAMP, le molecole di STING vengono attivate, legandosi in una catena (un processo chiamato oligomerizzazione) e migrando verso un organello diverso chiamato Golgi. Lì, attivano ulteriori molecole in una cascata di segnalazione che stimola l’attività immunitaria. L’oligomerizzazione di STING è necessaria affinché ciò avvenga.
Non è ancora chiaro come STING si oligomerizzi e perché debba spostarsi dal RE all’apparato di Golgi. Per trovare ulteriori molecole che svolgano un ruolo nella regolazione di STING, un team guidato dal Dott. Chen e da Jay Xiaojun Tan, Ph.D., ex borsista post-dottorato presso il Chen Lab e ora professore associato di Biologia Cellulare presso la Facoltà di Medicina dell’Università di Pittsburgh, ha analizzato quali molecole interagiscono con STING. Tra queste, una si è distinta: un enzima noto come PIKfyve, che produce un lipide chiamato PtdIns(3,5)P 2.
Quando i ricercatori hanno utilizzato una tecnica genetica per eliminare PIKfyve dalle cellule, STING non si è più spostato dal RE al Golgi né ha attivato molecole nella sua cascata di segnalazione immunitaria. Esperimenti successivi hanno dimostrato che la miscelazione di PtdIns(3,5)P 2 con STING ha migliorato l’attivazione di STING da parte di cGAMP. Ulteriori studi hanno dimostrato che PtdIns(3,5)P 2 si lega direttamente a STING. Insieme, questi risultati suggeriscono che PtdIns(3,5)P 2 interagisca con cGAMP per attivare STING.
Contemporaneamente, Jie Li, Ph.D., Istruttore di Biofisica presso l’UTSW, sotto la supervisione di Xiaochen Bai, Ph.D., Professore Associato di Biofisica e Biologia Cellulare, e Xuewu Zhang, Ph.D., Professore di Farmacologia e Biofisica, stavano anche cercando le molecole necessarie per attivare STING. Studi precedenti avevano dimostrato che i fosfatidilinositolo fosfati (PIP), la famiglia chimica che include PtdIns(3,5)P2 , potevano svolgere un ruolo importante in questo processo. Di conseguenza, i ricercatori hanno testato l’effetto di diversi PIP su STING stimolato da cGAMP. I loro esperimenti hanno dimostrato che PtdIns(3,5)P2 era necessario affinché le molecole di STING si legassero in una catena.
Per comprendere meglio il ruolo di PtdIns(3,5)P 2, i ricercatori hanno utilizzato la microscopia crioelettronica, che può visualizzare le molecole a livello atomico. I loro risultati hanno mostrato che PtdIns(3,5)P 2 si lega a una scanalatura tra coppie di molecole STING, fungendo da ponte che collega queste coppie in una stringa. I ricercatori sono rimasti sorpresi nel trovare anche molecole di colesterolo in un punto vicino al legame di PtdIns(3,5)P 2. Il colesterolo sembra stabilizzare la disposizione lineare di STING.
Oltre a dimostrare il ruolo chiave di PtdIns(3,5)P 2 nell’attivazione di STING, questi risultati spiegano anche perché STING deve migrare dal RE al Golgi per avviare la sua cascata di segnalazione. Mentre PtdIns(3,5)P 2 e colesterolo sono presenti in quantità limitate nel RE, le concentrazioni di queste molecole sono molto più elevate nel Golgi e nelle vescicole derivate dal Golgi, un fattore necessario affinché STING si assembli in lunghe catene.
Collaborando come gruppo, i due team hanno testato gli effetti di porzioni mutanti di STING che si legano a PtdIns(3,5)P2 e colesterolo. Queste molecole di STING mutanti non formavano più una catena né avviavano la cascata di segnalazione, confermando che PtdIns(3,5)P2 e colesterolo sono necessari per questi eventi.
Leggi anche:Malattie autoimmuni: proteina mitocondriale bersaglio promettente per il trattamento
“Questi risultati non rispondono solo a domande scientifiche di base”, ha spiegato il Dott. Zhang. Piuttosto, conoscere le molecole coinvolte nell’attivazione di STING e il modo in cui si legano a STING può guidare i ricercatori nella progettazione di farmaci che possano favorire o ostacolare questi processi. Incoraggiare l’attivazione di STING potrebbe aiutare i pazienti a combattere infezioni o tumori, mentre soffocarla potrebbe curare malattie autoimmuni e neurodegenerative. I ricercatori intendono continuare a studiare il funzionamento del pathway cGAS-STING per raggiungere questi obiettivi.
Fonte:Nature