La ricerca della Duke University ribalta le precedenti convinzioni sui retrotrasposoni, dimostrando che queste sequenze di DNA utilizzano attivamente meccanismi cellulari per formare forme circolari e replicarsi. Questa scoperta, che ha implicazioni per la comprensione dell’evoluzione genetica e delle malattie, mette in discussione la visione di lunga data secondo cui il DNA circolare è semplicemente un sottoprodotto accidentale. Credito: SciTechDaily.com
Il DNA circolare , ritenuto un sottoprodotto accidentale, sta prendendo in prestito i meccanismi di riparazione del DNA della cellula per copiare se stesso.
Come i suoi cugini virali, è stato scoperto che una sequenza di DNA in qualche modo parassitaria chiamata retrotrasposone prende in prestito il meccanismo della cellula per raggiungere i suoi obiettivi.
In una ricerca pubblicata sulla rivista Nature, un team della Duke University ha determinato che i retrotrasposoni dirottano una parte poco conosciuta della funzione di riparazione del DNA della cellula per chiudersi in una forma ad anello e quindi creare un doppio filamento corrispondente.
La scoperta sconvolge 40 anni di saggezza convenzionale secondo cui questi anelli erano solo un inutile sottoprodotto di una cattiva copiatura genetica. Potrebbe anche offrire nuove informazioni sul cancro, sulle infezioni virali e sulle risposte immunitarie.
I retrotrasposoni sono segmenti di DNA lunghi circa 7.000 lettere che si copiano e incollano in diverse parti del genoma sia delle piante che degli animali. In questo modo, svolgono un ruolo nella riscrittura del DNA e nella regolazione del modo in cui la cellula utilizza i suoi geni. Si ritiene che i retrotrasposoni siano alla base di gran parte della variazione e dell’innovazione nei geni che guidano l’evoluzione e sono ereditati da entrambi i genitori.
Implicazioni dei retrotrsposono nell’evoluzione e nella malattia
Molti studi hanno suggerito che questi anelli di DNA esterni ai cromosomi siano in qualche modo coinvolti nello sviluppo e nella progressione del cancro, in parte perché è noto che ospitano oncogeni che guidano il cancro all’interno delle loro sequenze di DNA. È noto anche che il retrovirus HIV, che causa l’AIDS, forma un DNA circolare.
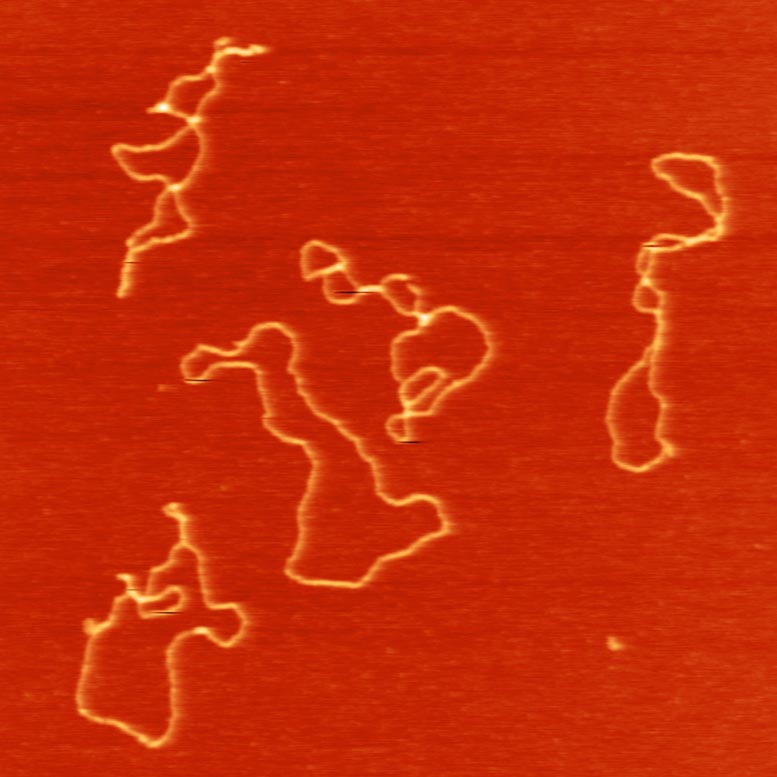
È stato osservato che il DNA circolare a forma di anello copia se stesso prendendo in prestito alcuni dei meccanismi della cellula, proprio come fa un virus. Credito: Fu Yang, ZZ Lab della Duke University
“Penso che questi elementi siano la fonte della dinamica del genoma, dell’evoluzione degli animali e influenzano persino la nostra vita quotidiana“, ha affermato Zhao Zhang (ZZ), assistente Professore di farmacologia e biologia del cancro e studioso della Duke Science & Technology. “Ma stiamo ancora apprezzando la loro funzione”.
Svelare il mistero dei retrotrasposoni
I retrotrasposoni sono abbastanza comuni – costituiscono circa il 40% del genoma umano e oltre il 75% del genoma del mais – ma come e dove si copiano è sempre stato un po’ oscuro.
Zhang mostra un grosso libro di testo sui retrovirus che ha consultato per questo studio. “I libri dicono che le sequenze ad anello si sono create ricombinando le due estremità del DNA lineare e sono solo un vicolo cieco, un sottoprodotto di una replicazione fallita”, ha spiegato.
In precedenti lavori con le uova del moscerino della frutta, il team di Zhang aveva stabilito che i retrotrasposoni ereditati utilizzano le “cellule nutrici” che supportano l’uovo, come fabbriche per produrre molte copie di se stessi che vengono poi distribuite in tutto il genoma nell’uovo in via di sviluppo della mosca. Questo sistema modello ha permesso ai ricercatori di saperne di più sui retrotrasposoni.
Nell’ultimo lavoro, i ricercatori hanno scoperto inaspettatamente che la maggior parte dei retrotrasposoni appena aggiunti avevano questa forma circolare anziché essere integrati nel genoma dell’ospite. Quindi hanno eseguito una serie di esperimenti mettendo fuori uso i meccanismi di riparazione del DNA della cellula uno alla volta per capire come e dove si formano i cerchi.
La risposta: un meccanismo di riparazione del DNA poco studiato chiamato riparazione alternativa del DNA con giunzione finale o alt-EJ in breve, che ripara le rotture del doppio filamento. Le sequenze di retrotrasposone utilizzavano questa parte del meccanismo di riparazione dell’ospite per cucire insieme le estremità del loro DNA a filamento singolo e quindi utilizzavano la sua DNA sintasi per creare un doppio filamento corrispondente. Per buona misura, i ricercatori hanno confermato che questo è anche il processo all’interno delle cellule umane.
Ripensare il DNA circolare
Quindi i retrotrasposoni non sono un incidente sciatto; in realtà stanno dirottando una piccola parte dei macchinari della cellula per produrre più di se stessi, proprio come fanno i virus.
“La nostra scoperta in realtà ribalta il modello dei libri di testo“, ha detto Zhang. “Abbiamo dimostrato che l’evento di ricombinazione proposto dal libro di testo non è importante per la formazione degli anelli“, ha detto Zhang. “Invece, è il percorso alt-EJ che guida la produzione dell’anello“.
“Il mio laboratorio attualmente sta cercando di verificare se il DNA circolare può essere un intermedio per realizzare nuovi inserimenti nel genoma“, ha detto Zhang. “Stiamo anche testando se il DNA circolare può essere percepito dal nostro sistema immunitario per innescare una risposta immunitaria“.
Leggi anche:Come un antico invasore genetico abita il nostro DNA
“Nel campo dei retrovirali e dei retrotrasposoni, si pensa che il DNA circolare sia solo un evento minore, ma il nostro studio sta portando il DNA circolare al centro della scena“, ha detto Zhang. “I ricercatori dovrebbero prestare maggiore attenzione al DNA circolare”.
Immagine Credit Public Domain.
Fonte: Nature

