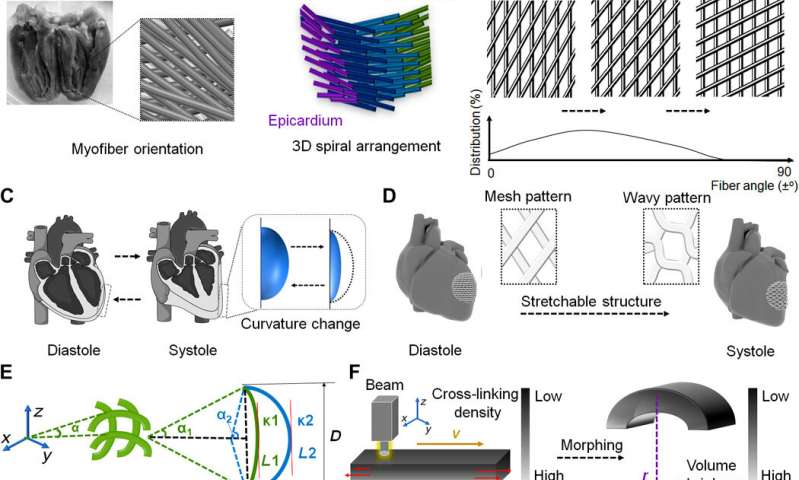
Immagine:progettazione di un cerotto cardiaco fisiologicamente adattabile. Credito:Science Advances , doi: 10.1126 / sciadv.abb5067.
I bioingegneri hanno tecniche ingegneristiche di impalcatura cardiaca notevolmente avanzate per il trattamento dell’infarto miocardico, una forma di malattia cardiovascolare e la principale causa di morbilità e mortalità in tutto il mondo.
Tuttavia, è ancora difficile replicare la specificità strutturale e la variabilità dei tessuti cardiaci con i tradizionali processi di bioingegneria. In un nuovo rapporto su Science Advances, Haitao Cui e un team di ricerca interdisciplinare presso il National Institute of Health, Università del Maryland e George Washington University, negli Stati Uniti, hanno sviluppato un cerotto cardiaco quadridimensionale (4-D) con adattabilità fisiologica. Hanno usato la stereolitografia, una tecnologia laser che impiega una resina liquida sensibile ai raggi UV, per stampare il costrutto e combinare l’auto-morphing 4-D con microstrutture espandibili per migliorare le loro proprietà biomeccaniche da integrare nel cuore pulsante.
I risultati hanno mostrato una migliore vascolarizzazione e maturazione dei cardiomiociti sotto stimolazione meccanica fisiologicamente rilevante. I costrutti erano adatti per l’uso in un modello murino di infarto miocardico cronico (MI) con attecchimento cellulare migliorato e fornitura vascolare.
Il lavoro fornisce un’efficace strategia di trattamento per l’MI e un metodo di bioingegneria all’avanguardia per migliorare la progettazione strutturale di tessuti complessi per la rigenerazione degli organi.
Bioingegneria del cuore umano
Il cuore è un organo dinamico e multicellulare legato al tessuto con caratteristiche strutturali e funzionali altamente specifiche. I muscoli cardiaci adulti non hanno la capacità di autoripararsi e rigenerarsi dopo un infarto miocardico, quindi i cerotti cardiaci tradizionali servono come sistemi di supporto meccanici temporanei per prevenire il rimodellamento ventricolare sinistro post-infarto. Il campo dell’ingegneria cardiaca sta emergendo per generare tessuti cardiaci funzionali come alternativa promettente a lungo termine alla riparazione dei tessuti danneggiati. L’impalcatura può fornire supporto meccanico con cerotti cellulari e ripristinare la funzionalità del miocardio danneggiato. I materiali a base di idrogel derivati da fonti naturali sono adatti per imitare il microambiente dei tessutie supportare l’adesione e la crescita cellulare. Forniscono matrici favorevoli per la crescita e la differenziazione dei cardiomiociti, ma il loro design strutturale e i limiti di fabbricazione hanno reso difficili le applicazioni cliniche . La maggior parte dei team di ricerca incorpora cardiomiociti derivati da cellule staminali pluripotenti indotte dall’uomo (hiPSC-CMs) come fonte continua di cellule per la differenziazione cellulare (crescita e maturazione), grazie alle loro promettenti applicazioni nell’ingegneria cardiaca.

Cui et al. hanno sviluppato un cerotto cardiaco a base di idrogel 4-D con un design intelligente specifico per l’adattabilità fisiologica usando la stereolitografia per ottenere molti micro-modelli e microarchitettura specifici. Il processo di automorfizzazione ha raggiunto conformazioni identiche alla curvatura superficiale del cuore. Gli scienziati hanno tenuto conto delle caratteristiche fisiologiche del tessuto cardiaco per creare una microarchitettura altamente estensibile, usando l’idrogel per facilitare la trasformazione da un modello ondulato a un reticolo, rispetto alle funzioni diastole e sistole del ciclo cardiaco. Il team ha quindi tri-coltivato cardiomiociti, cellule stromali mesenchimali e cellule endoteliali sui cerotti cardiaci ingegnerizzati per riprodurre le reti vascolari per supportare e guidare le cellule contraenti.
Progettare un cerotto cardiaco fisiologicamente adattabile
Usando l’imaging del tensore della diffrazione (DTI), gli scienziati hanno notato una rete elicoidale di miofibre nel ventricolo sinistro (LV) disposte per formare una struttura a foglio, mentre la progettazione assistita da computer (CAD) li ha aiutati a trasformare i dettagli anatomici di complesse strutture in fibra in un tessuto cardiaco ingegnerizzato. Le funzioni di diastole e sistole sono specifiche del tessuto cardiaco e indotte dalle contrazioni del muscolo cardiaco, per generare la forza per la circolazione sanguigna. Il cambiamento di volume nel cuore ha rappresentato la disposizione allungata dinamicamente delle fibre in una regione selezionata. Per tenere conto della curvatura ventricolare, il modello di mesh derivato dal CAD potrebbe quindi cambiare in un esagono o modello ondulato nel piano 2D. Le fibre muscolari cardiache contengono miofibrille raggruppate longitudinalmente con cardiomiociti e guaine di collagene, circondate da capillari ad alta densità. Questa architettura muscolare anisotropa può produrre attività elettromeccaniche coordinate dei ventricoli come la contrazione e la propagazione dell’onda di eccitazione.

Al fine di integrare la relazione tra la struttura estensibile e la curvatura ventricolare, il team ha matematicamente caratterizzato il design utilizzando un modello geometrico solido e semplificato con un prototipo di curva piana. I ricercatori avevano precedentemente utilizzato il morphing 4-D indotto dalla luce con stereolitografia personalizzata per sviluppare lo stress interno classificato indotto dal laser come una delle principali forze di immersione per il morphing dinamico 4-D nell’ingegneria neurale. Sulla base di questi principi, il cerotto cardiaco stampato in 3D sviluppato da Cui et al. potrebbe trasformarsi da un modello piatto all’architettura curva 4-D, a seconda della selezione dei parametri di stampa appropriati.
Vedi anche: Cerotto cardiaco artificiale pronto all’uso ripara i danni da infarto in ratti e maiali
Stampa e ottimizzazione del patch cardiaco
Gli scienziati hanno utilizzato un inchiostro stampabile a base di gelatina metacrilato (GelMA) e polietilenglicole diacrilato (PEGDA) per progettare il cerotto cardiaco anisotropico con orientamento della fibra miocardica. GelMA è un biomateriale fotocurabile contenente molte sequenze di peptidi per promuovere l’attaccamento e la crescita delle cellule. La velocità di stampa ha influenzato le prestazioni di fotopolimerizzazione e l’accuratezza strutturale provocando l’automorfizzazione 4-D. Il team ha determinato l’accuratezza di stampa della disposizione delle fibre e ha variato il rapporto in peso di GelMA e PEGDA per i risultanti moduli meccanici di idrogel per raggiungere il modulo del miocardio nativo, mentre i modelli stampati rappresentavano la microarchitettura del tessuto miocardico nativo.

Il team ha coltivato gli hiPSC-CM sugli scaffold a causa della loro nota capacità di ripristinare le funzioni cardiache e, dopo tre giorni, gli hiPSC-CM associati hanno mostrato contrazioni spontanee. Sette giorni dopo, gli hiPSC-CM formavano aggregati sopra le fibre stampate per la contrazione sincrona per l’accoppiamento elettrofisiologico delle cellule. Al settimo giorno, i cardiomiociti hanno mostrato una crescita aumentata sui cerotti cardiaci, mentre i transitori di calcio sono aumentati a uno stato stabile per stabilire eccellenti comportamenti fisiologici di contrazione-rilassamento funzionale.
Test di maturazione funzionale e impianto in vivo
Per gli studi di stimolazione biomeccanica e di maturazione funzionale, il team ha eseguito immunocolorazione e determinato l’espressione di geni correlati al cuore su costrutti di materiale cellulare. Al giorno 14, hanno notato la maggiore espressione di geni associati all’accoppiamento eccitazione-contrazione, struttura sarcomerica e angiogenesi (formazione di nuovi vasi sanguigni), mentre gli iPSC-CM nei cerotti stampati sono maturati nel tempo. Il team ha impiantato i cerotti cardiaci in modelli murini di danno da riperfusione ischemica per la simulazione di patologie cardiache clinicamente acute o croniche nella ricerca cardiovascolare.

I ricercatori hanno valutato i cerotti cardiaci in uno studio a lungo termine (quattro mesi) dopo l’impianto per evidenziare il recupero di modelli animali in un breve periodo di tempo con meno infiammazione e alti tassi di sopravvivenza, rispetto al classico modello di infarto miocardico. Il team ha condotto test immunofluorescenti per mostrare le cellule vascolari che attraversano l’interfaccia del miocardio e si espandono all’interno del cerotto miocardico, fornendo così supporto meccanico e prevenendo efficacemente il rimodellamento del ventricolo sinistro. Entro quattro mesi, il cerotto impiantato ha mostrato un’eccellente connettività con il cuore del topo, gli scienziati hanno notato una maggiore densità cellulare e una più piccola area di infrazione nel cerotto cellulare rispetto ai cerotti acellulari impiantati nel gruppo MI.
In questo modo, Haitao Cui e colleghi hanno sviluppato un cerotto cardiaco 4-D fisiologicamente adattabile per ricapitolare le caratteristiche architettoniche e biologiche del tessuto miocardico nativo. Hanno usato la stampa SL a scansione di fascio per progettare patch intelligenti per fornire supporto meccanico e una struttura e una matrice fisiologicamente sintonizzabili per l’impianto cellulare. I cerotti cardiaci hanno mostrato alti livelli di attecchimento cellulare e vascolarizzazione dopo l’impianto in un modello MI di topo. Il team intende estendere gli studi futuri a un modello di grande animale fisiologicamente rilevante come il modello suino o primati non umani per risultati più realistici nelle terapie cliniche di ingegneria cardiaca.
Fonte: Science Advances