
Cancro- immagine: meccanismi epigenetici influenzano il modo in cui il DNA viene impacchettato nei cromosomi e, di conseguenza, l’accessibilità dei geni per la trascrizione. Crediti: Ella Maru Studios.
Le analisi epigenomiche suggeriscono nuovi approcci promettenti per il monitoraggio e il trattamento del cancro. Cosa rivelano queste analisi e quanto sono vicine a migliorare gli esiti per i pazienti?
Quando si parla di cancro, i meccanismi che influenzano l’espressione genica senza modificarne la sequenza codificante sono importanti quanto le mutazioni genetiche. Tuttavia, la ricerca su questi processi epigenetici è rimasta indietro perché in passato erano difficili da studiare. “Le nuove tecnologie ci stanno permettendo di recuperare il terreno perduto in ambito genetico”, afferma Céline Vallot, epigenetista specializzata in oncologia presso l’Institut Curie di Parigi.
I processi epigenetici agiscono tipicamente modificando la struttura della cromatina: il DNA e le proteine istoniche che compongono i cromosomi. Se la cromatina è aperta e accessibile, può avvenire la trascrizione genica; dove è più compatta, i geni vengono silenziati. La conformazione della cromatina può essere alterata da enzimi che marcano chimicamente il DNA o gli istoni attorno a cui si avvolge. La maggior parte della ricerca epigenetica si è concentrata sui processi che influenzano questi enzimi e su come potrebbero attivare gli oncogeni o disattivare i geni oncosoppressori.
Anche la struttura della cromatina, e quindi l’espressione genica, è influenzata dal DNA non codificante, che costituisce il 98% del genoma. In particolare, esistono brevi regioni che regolano l’espressione dei geni vicini e l’attenzione si sta concentrando sulle mutazioni che interessano questi cosiddetti enhancer e isolatori. “Le alterazioni epigenetiche che modificano i confini tra le regioni geniche vicine causano una stimolazione inappropriata dei geni”, afferma Howard Chang, Direttore del Center for Personal Dynamic Regulomes presso la Stanford University, in California. Il gruppo di Chang sta sviluppando metodi innovativi per studiare l’epigenoma e identificare i meccanismi chiave che regolano la trascrizione nei campi del cancro, dello sviluppo e dell’invecchiamento.
I profili trascrizionali aberranti derivanti da alterazioni epigenetiche possono essere utilizzati non solo per distinguere diversi sottotipi di cancro, ma anche come metodo per individuare tumori in campioni di sangue. Farmaci che agiscono sui regolatori epigenetici sono già approvati per il trattamento della sindrome mielodisplastica, dei linfomi a cellule T e del mieloma multiplo.
Tuttavia, le terapie epigenetiche non hanno ancora espresso appieno il loro potenziale. Le terapie attuali sono limitate dalla tossicità e dagli effetti indesiderati. I progressi nelle tecnologie di sequenziamento di nuova generazione stanno consentendo ai ricercatori di mappare le informazioni epigenomiche e i loro effetti sulla struttura della cromatina con una precisione senza precedenti. Studiando il panorama epigenetico delle cellule tumorali e delle cellule immunitarie con cui combattono, i ricercatori stanno identificando nuovi bersagli epigenetici e approcci terapeutici. Questa conoscenza sta contribuendo sia a migliorare la selettività delle terapie epigenetiche sia a personalizzare i trattamenti in base alle caratteristiche di ciascun paziente.
Epigenetica e immuno-oncologia
L’oncologa pediatrica Crystal Mackall e il suo team presso l’Università di Stanford stanno utilizzando l’ATAC-seq (Assay for Transposase-Accessible Chromatin using sequencing ) per svelare i meccanismi epigenetici che regolano l’esaurimento delle cellule T, uno stato di disfunzione progressiva che si sviluppa quando le cellule vengono continuamente stimolate da antigeni e fattori infiammatori. Superare l’esaurimento delle cellule T è fondamentale per migliorare la durata delle terapie con cellule T con recettore chimerico per l’antigene (CAR-T).
“L’ATAC-seq offre una visualizzazione senza precedenti delle regioni del genoma più attive a livello trascrizionale”, afferma. Il team di Mackall ha utilizzato l’ATAC-seq per identificare i fattori di trascrizione che vengono sovraregolati durante l’esaurimento delle cellule CAR T.
L’obiettivo del team dell’Università di Stanford è quello di interrompere i programmi trascrizionali che guidano l’espressione genica associata all’esaurimento. Hanno individuato una possibile via: la sovraespressione del fattore di trascrizione c-Jun sembra prevenire l’esaurimento e migliorare il controllo del tumore, aprendo la strada a terapie CAR-T di nuova generazione resistenti all’esaurimento.
Combinando le conoscenze epigenetiche con le tecnologie di editing genetico come CRISPR, Mackall prevede un aumento “dell’ingegneria epigenetica”, che si concentrerà sulle regioni regolatorie non codificanti del genoma. “Anziché eliminare completamente l’espressione dei geni associati all’esaurimento, attraverso l’ingegneria epigenetica possiamo regolarne finemente l’espressione e impedire alle cellule di reagire in un certo modo in un contesto specifico“, spiega. “Abbiamo visto che funziona, dobbiamo ancora scoprire se è utile”.
Vallot concorda sul fatto che siano necessari ulteriori miglioramenti nelle tecnologie epigenetiche prima che le scoperte attuali possano essere applicate ai pazienti. “La tecnologia sta iniziando ad essere applicata ai campioni dei pazienti”, afferma. “Spero che, tra cinque anni, possa essere utilizzata per caratterizzare ampie coorti di pazienti ai fini di terapie personalizzate”.
Tecnologie epigenetiche emergenti a singola cellula
Fino a poco tempo fa, la maggior parte degli studi si basava su tecniche che misuravano gli stati epigenetici medi di popolazioni cellulari e tessuti nel loro complesso. Sebbene abbiano fornito informazioni preziose sui meccanismi generalizzati, non consentono di esaminare gli eventi epigenetici che si verificano in popolazioni cellulari poco caratterizzate e in tipi cellulari rari all’interno di tessuti normali o tumorali.
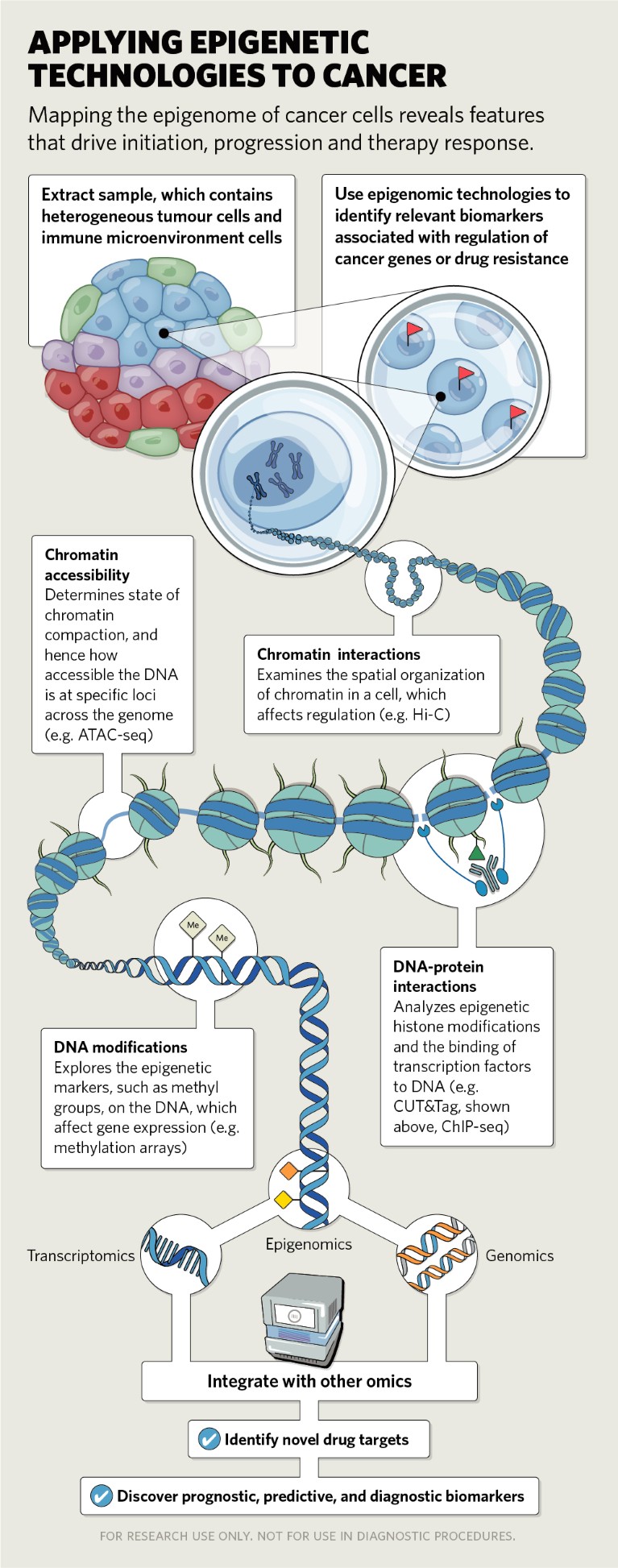
Comprendere l’eterogeneità delle cellule tumorali, sia all’interno che tra i tumori, può far luce sulle caratteristiche che determinano il potenziale metastatico delle cellule e la loro sensibilità al trattamento. Sono stati riportati più di 30 metodi epigenomici a singola cellula, che possono essere utilizzati per valutare la struttura della cromatina o l’accessibilità del DNA (come scATAC-seq), l’organizzazione tridimensionale dei cromosomi (scHI-c) e le modificazioni degli istoni e del DNA a livello dell’intero genoma (scChIP-seq, scCUT&Tag) [vedi ‘Applicazione delle tecnologie epigenetiche al cancro’].
Leggi anche: Il paradosso mortale del cancro: come i tumori alterano il proprio DNA per continuare a crescere
Melanie Eckersley-Maslin, epigenetista dello sviluppo, ha utilizzato tecnologie a singola cellula per studiare il rimodellamento epigenetico e la determinazione del destino cellulare durante le prime fasi dello sviluppo embrionale. Ora è entrata a far parte del Peter MacCallum Cancer Centre di Melbourne, in Australia, dove il suo team applicherà questi metodi per esaminare le traiettorie del destino delle cellule tumorali.
È ormai noto che le cellule tumorali possono sviluppare modelli di espressione genica simili a quelli osservati nelle cellule embrionali, ma i ricercatori sanno ancora poco su come e perché ciò accada. “È come se le cellule attraversassero una crisi di mezza età”, afferma Eckersley-Maslin, “perdono la loro identità e diventano più simili alle cellule embrionali, capaci di acquisire diversi destini cellulari e di adattarsi a nuovi ambienti”. Gli scienziati sospettano che comprendere il significato funzionale di questi cambiamenti possa portare alla scoperta di nuovi biomarcatori tumorali e bersagli farmacologici.
I ricercatori dell’Institut Curie hanno sviluppato un approccio che prevede l‘immunoprecipitazione della cromatina a singola cellula seguita dal sequenziamento (scChIP-seq) per esplorare la plasticità delle cellule del cancro al seno e le sue implicazioni per il trattamento. Utilizzando modelli di xenotrapianto derivati da pazienti affetti da cancro al seno, hanno individuato un sottogruppo di cellule sensibili ai farmaci non trattate che condividono una firma cromatinica comune con le cellule resistenti al tamoxifene.<sup> 3 </sup> Il loro lavoro evidenzia la perdita di un particolare marcatore della cromatina, associato a una repressione trascrizionale stabile (H3K27me3), come meccanismo chiave alla base della resistenza ai farmaci.
“Gli approcci a singola cellula stanno aprendo la strada alla valutazione dell’eterogeneità epigenetica all’interno dei tumori, fondamentale per comprendere la plasticità delle cellule tumorali e il processo evolutivo verso la resistenza”, afferma Vallot, autrice principale dello studio. Si sta concentrando su come le cellule modificano la loro predisposizione epigenetica a diventare resistenti al trattamento nel tempo e se la chemioterapia può essere combinata con modulatori epigenetici per prevenire la chemioresistenza. “La tempistica è cruciale“, afferma. “I modulatori epigenetici devono essere somministrati all’inizio della chemioterapia per limitare la plasticità delle cellule tumorali e arrestare l’evoluzione della resistenza”.
Mettere tutto insieme
La combinazione di tecniche epigenomiche per analizzare molteplici marcatori epigenetici all’interno della stessa singola cellula e la loro integrazione con informazioni trascrizionali e genetiche saranno fondamentali per generare profili cellulari completi e terapie oncologiche personalizzate. “Combinando diverse tecnologie, i ricercatori stanno realizzando progetti davvero innovativi e acquisendo una migliore comprensione di ciò che accade nel cancro”, afferma Eckersley-Maslin. Sono in fase di sviluppo numerosi approcci multi-omici per far progredire la ricerca sul cancro.
“Il futuro si prospetta roseo per le tecnologie di sequenziamento avanzate nella ricerca sul cancro”, afferma Chang. “La multiomica e i metodi di genomica spaziale sono due importanti progressi che ci stanno aiutando a imparare a leggere e riscrivere il genoma del cancro“.
Fonte: Nature
.

