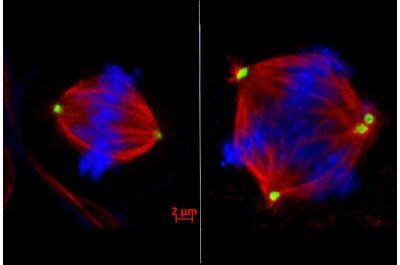
Cancro al seno triplo negativo-immaginne: a sinistra: Divisione cellulare normale con i cromosomi (blu) allineati e pronti per essere estratti in due cellule figlie separate dai due centrosomi (verde). A destra: Nella divisione cellulare difettosa, sono presenti troppi centrosomi, con conseguente instabilità cromosomica in più cellule. Crediti: Dott.ssa Shelly Yang Bai
Ripristinare l’ordine nelle cellule tumorali in divisione potrebbe arrestare la diffusione del cancro al seno triplo negativo.
Il carcinoma mammario triplo negativo (TNBC) è una delle forme di cancro al seno più aggressive e difficili da trattare, ma un nuovo studio condotto dalla Weill Cornell Medicine suggerisce un modo sorprendente per impedirne la diffusione. I ricercatori hanno scoperto che un enzima chiamato EZH2 induce le cellule TNBC a dividersi in modo anomalo, consentendo loro di trasferirsi in organi distanti. Lo studio preclinico ha anche scoperto che i farmaci che bloccano EZH2 potrebbero ripristinare l’ordine nelle cellule in divisione e ostacolare la diffusione delle cellule TNBC.
“Le metastasi sono la causa principale delle scarse probabilità di sopravvivenza per i pazienti con carcinoma mammario triplo negativo”, ha affermato l’autore senior, il Dott. Vivek Mittal, Professore di Ricerca Ford-Isom di Chirurgia Cardiotoracica e membro del Sandra and Edward Meyer Cancer Center presso la Weill Cornell Medicine. “Il nostro studio suggerisce un nuovo approccio terapeutico per bloccare le metastasi prima che si formino e aiutare le pazienti a sconfiggere questo tumore mortale”.
I risultati, pubblicati il 2 ottobre su Cancer Discovery, mettono in discussione l’idea diffusa che i trattamenti contro il cancro debbano amplificare gli errori di divisione cellulare già presenti nelle cellule tumorali oltre il punto di rottura per indurre la morte cellulare. Quando le cellule normali si dividono, i cromosomi – “pacchetti” di DNA contenenti geni – vengono duplicati e divisi equamente in due cellule figlie. Questo processo va in tilt in molte cellule tumorali, portando a instabilità cromosomica: troppi, troppo pochi o cromosomi confusi in più cellule figlie.
“Trovo un po’ preoccupante il tentativo di spingere le cellule tumorali oltre il limite con una maggiore instabilità cromosomica, perché se non si raggiunge il livello giusto, si potrebbe paradossalmente sviluppare una malattia aggressiva”, ha affermato il Dott. Mittal. “Invece, i nostri risultati suggeriscono che ripristinare l’ordine nella divisione cellulare prendendo di mira EZH2 può impedirne la diffusione”.
La prima autrice, la Dott.ssa Shelley Yang Bai, ha iniziato questo lavoro come studentessa laureata ed è ora ricercatrice post-dottorato con il Dott. Mittal in chirurgia cardiotoracica presso la Weill Cornell Medicine. Il Dott. Samuel Bakhoum, che all’epoca lavorava presso il Memorial Sloan Kettering Cancer Center, ha co-diretto questo studio.
Collegare epigenetica e metastasi
Circa il 5% delle cellule di un tumore primario TNBC ha un’alta probabilità di metastatizzare e queste cellule presentano caratteristiche uniche, come un metabolismo diverso, una maggiore instabilità cromosomica e un’epigenetica alterata, ovvero modifiche al DNA o alle proteine associate che non alterano direttamente il codice genetico.
Il team del Dott. Mittal ha individuato un fattore sospetto che potrebbe innescare la metastasi in queste particolari cellule tumorali: EZH2. Questa proteina normalmente “modifica il modo in cui il DNA viene impacchettato nelle cellule”. Ma i tumori spesso dirottano EZH2 aumentandone la produzione. Nel TNBC, questa sovrapproduzione porta al silenziamento di geni chiave necessari alla corretta segregazione dei cromosomi durante la divisione cellulare e a errori dilagati.
Analizzando i dati di pazienti affette da tumore al seno, il Dott. Bai ha scoperto che le pazienti con livelli più elevati di EZH2 presentavano anche cellule tumorali con maggiori alterazioni cromosomiche. Ciò ha fornito indizi per ulteriori esperimenti di laboratorio. Mentre l’inibizione di EZH2 con Tazemetostat, un farmaco approvato dalla FDA per il trattamento di alcuni tumori, riduceva l’instabilità cromosomica nelle linee cellulari, l’aumento dei livelli di EZH2 aumentava geneticamente gli errori nella divisione cellulare.
Inoltre, i modelli murini con livelli elevati di EZH2 e instabilità cromosomica nei tumori primari hanno mostrato un aumento delle metastasi polmonari rispetto ai tumori privi di EZH2, confermando un legame diretto tra livelli di EZH2, instabilità cromosomica e metastasi. Ma in che modo EZH2 determina l’instabilità?
Caos cromosomico
Il team ha scoperto che EZH2 silenzia il gene tankyrase 1, che normalmente garantisce il corretto funzionamento del meccanismo di separazione dei cromosomi durante la divisione cellulare. Questo innesca una reazione a catena : la diminuzione di tankyrase 1 provoca l’accumulo eccessivo di un’altra proteina, la CPAP. Questo induce i centrosomi della cellula – strutture che separano i cromosomi – a moltiplicarsi in modo incontrollato, portando a divisioni difettose in tre o più cellule figlie.
Il team ha dimostrato che l’inibizione di EZH2 ripristina l’equilibrio, riducendo significativamente le metastasi nei modelli preclinici. “Per la prima volta, abbiamo collegato EZH2, che è un regolatore epigenetico, con l’instabilità cromosomica in modo meccanicistico”, ha affermato il Dott. Bai.
Leggi anche:RNA raramente studiato collegato al cancro al seno triplo negativo
Gli inibitori di EZH2 potrebbero essere i primi farmaci in grado di sopprimere direttamente l’instabilità cromosomica. “Questo studio fornisce un nuovo approccio promettente al trattamento del carcinoma mammario triplo negativo, prendendo di mira la causa principale delle metastasi”, ha affermato la Dott.ssa Magdalena Plasilova, professoressa associata di chirurgia clinica (in attesa di assegnazione del titolo), oncologa chirurgica presso il NewYork-Presbyterian/Weill Cornell Medical Center e autrice dello studio. “Vedo in prima persona l’impatto devastante delle metastasi sui pazienti e questo offre la speranza di migliorare i risultati e i tassi di sopravvivenza”.
Sebbene il Tazemetostat possa essere riproposto come trattamento per il TNBC, altri farmaci potrebbero avere effetti simili o migliori. “La nostra scoperta apre le porte a sperimentazioni cliniche per testare gli inibitori di EZH2 nel carcinoma mammario ad alto rischio e potenzialmente in altri tumori caratterizzati da instabilità cromosomica, come l’adenocarcinoma polmonare”, ha affermato il Dott. Mittal, che è anche membro dell’Englander Institute of Precision Medicine presso il Weill Cornell. Attualmente, sta pianificando collaborazioni per condurre test di sicurezza in una sperimentazione clinica.
Fonte:Cancer Discovery