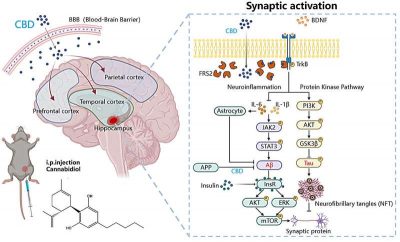
Alzheimer-immagine: schema riassuntivo dello studio. Il diagramma illustra il meccanismo neuroprotettivo del CBD scoperto in questo lavoro. Il CBD si lega direttamente alla proteina adattatrice FRS2, agendo come una colla molecolare per stabilizzare il complesso di segnalazione TrkB-FRS2. Ciò sostiene l’attivazione a valle della via PI3K/AKT in modo indipendente dal BDNF. Attraverso questo meccanismo, un singolo intervento con CBD sopprime simultaneamente l’iperfosforilazione della proteina Tau, riduce la deposizione di Aβ, allevia la neuroinfiammazione, ripristina la sensibilità all’insulina e, in definitiva, salvaguarda l’architettura sinaptica e la funzione cognitiva. Fonte: Liu et al. ( Molecular Psychiatry , 2026).
La malattia di Alzheimer (AD) è una patologia neurodegenerativa caratterizzata da progressiva perdita di memoria, declino cognitivo e alterazioni comportamentali. È noto che i deficit associati all’AD derivano dall’accumulo anomalo di proteine, in particolare tau e β-amiloide (Aβ), nel cervello e tra le cellule nervose, che causa neuroinfiammazione e può provocare la degenerazione delle cellule cerebrali.
E’ stato recentemente scoperto che il cannabidiolo (CBD), un composto non psicoattivo derivato dalla pianta di Cannabis sativa, si sta dimostrando promettente nella protezione delle cellule cerebrali dai danni.
Rispetto al Δ9-tetraidrocannabinolo (THC), il composto della cannabis che provoca sensazioni di euforia e altera lo stato mentale dell’utilizzatore, il CBD è più sicuro e potrebbe quindi essere più facile da introdurre in ambito clinico.
Ricercatori dell’Università di Shenzhen, dell’Accademia cinese delle scienze e di altri Istituti hanno condotto uno studio per esplorare gli effetti del CBD su un modello murino di malattia di Alzheimer.
I loro risultati, pubblicati su Molecular Psychiatry, offrono nuove prospettive su come l’assunzione ripetuta di CBD potrebbe ridurre l’accumulo dannoso di proteine, ripristinare le connessioni cerebrali e migliorare la memoria nei topi che presentavano sintomi simili a quelli dell’Alzheimer.
“Studi precedenti hanno dimostrato che il CBD può ridurre la patologia della proteina Tau, attenuare la neuroinfiammazione e migliorare la funzione sinaptica e cognitiva nei modelli di malattia di Alzheimer“, ha dichiarato Xiubo Du, autore senior dell’articolo, a Medical Xpress.
“Tuttavia, rimane una lacuna fondamentale: non comprendiamo appieno come il CBD agisca a livello molecolare, in particolare quali proteine bersaglio interagisca con esso nel cervello. Senza questa conoscenza, è difficile spiegarne l’efficacia, per non parlare di ottimizzarla“.
Ripristino della funzione cerebrale nei topi con il CBD
Il primo obiettivo di questo recente studio era quello di verificare ulteriormente se il CBD potesse migliorare le funzioni cognitive e attenuare i deficit cognitivi in un modello murino di malattia di Alzheimer. Contemporaneamente, i ricercatori speravano anche di identificare i processi molecolari che potrebbero essere alla base dei benefici neuroprotettivi del CBD e che potrebbero essere bersaglio di interventi terapeutici.
Du e i suoi colleghi hanno studiato un modello murino di malattia di Alzheimer noto come topi triplo-transgenici con AD. Si tratta di topi geneticamente modificati le cui sinapsi subiscono un danno progressivo, in seguito alla formazione di grovigli di proteina Tau e all’accumulo di Aβ. Questi topi mostrano caratteristiche simili a quelle osservate nei pazienti affetti da AD, come perdita di memoria e comportamenti ansiosi.
Innanzitutto, i ricercatori hanno trattato i topi con CBD sei giorni alla settimana per un periodo totale di 45 giorni. Al termine di questo periodo di trattamento, hanno osservato il comportamento dei topi ed esaminato i loro cervelli.
È interessante notare che, dopo il trattamento, la memoria dei topi è migliorata e i loro livelli di ansia sono risultati inferiori. Inoltre, le spine dendritiche nel loro cervello e la struttura complessiva delle sinapsi (ovvero le giunzioni tra i neuroni) sembrano essersi ripristinate.
“Abbiamo quindi analizzato come il CBD produce gli effetti osservati“, ha affermato Du. “Abbiamo scoperto che attiva la via di segnalazione TrkB-PI3K-AKT, una via fondamentale per la sopravvivenza e la plasticità neuronale. È interessante notare che il fattore neurotrofico derivato dal cervello (BDNF), l’attivatore canonico di TrkB, non ha subito variazioni dopo il trattamento con CBD. Ciò suggerisce che il CBD agisca attraverso un meccanismo diverso.“
Il ruolo chiave della proteina FRS2
Du e i suoi colleghi hanno anche cercato di identificare la proteina a cui il CBD si lega nel cervello del topo utilizzando una tecnica chiamata profilazione termica del proteoma. Si tratta di un approccio di laboratorio che prevede il trattamento di tessuti o cellule con un composto specifico, il riscaldamento a diverse temperature, la rimozione delle proteine che si denaturano e l’analisi delle proteine rimanenti.
“L’idea è semplice: quando una piccola molecola si lega a una proteina, quest’ultima diventa più stabile, un po’ come quando due persone che si tengono per mano sono più difficili da separare”, ha spiegato Du. “Attraverso questo screening, FRS2 è emerso come candidato, mostrando una maggiore stabilità termica dopo il trattamento con CBD“.
Successivamente, Du e i suoi colleghi hanno cercato di convalidare i loro risultati utilizzando varie tecniche comunemente impiegate dai neurobiologi, tra cui l’estinzione della fluorescenza, la risonanza plasmonica di superficie (SPR), l’interferometria a strato biologico (BLI) e i test di spostamento termico cellulare (CETSA). Tutti questi ulteriori test hanno confermato che il CBD si lega in modo specifico e diretto a una proteina chiamata FRS2.
“Quando abbiamo eseguito simulazioni di dinamica molecolare, abbiamo scoperto che, a differenza dei farmaci convenzionali che si legano a un singolo sito di legame, il CBD si distribuisce dinamicamente sulla superficie di FRS2, concentrandosi infine all’interfaccia proteina-proteina TrkB-FRS2“, ha affermato Du.
“In questo caso, il gruppo ossidrilico del CBD forma legami idrogeno con specifici residui di tirosina su TrkB, mentre la sua regione idrofobica interagisce con FRS2, fungendo da ‘colla molecolare’ che rinforza la loro associazione, stabilizzando così il complesso di segnalazione e sostenendo l’attivazione della via di segnalazione a valle“.
Per approfondire il ruolo di FRS2, i ricercatori ne hanno bloccato la produzione nei topi utilizzando l’shRNA, un piccolo frammento di RNA che può essere introdotto nelle cellule per silenziare geni specifici o impedire la produzione di proteine specifiche.
Hanno scoperto che, quando la produzione di questa proteina veniva ridotta, il CBD si dimostrava significativamente meno efficace nel prevenire l’accumulo dannoso di proteine, nel proteggere le sinapsi e nel migliorare le funzioni cognitive dei topi.
“Questo ha confermato che FRS2 è essenziale per gli effetti neuroprotettivi del CBD”, ha affermato Du. “Ciò che trovo più sorprendente nei nostri risultati è che il CBD non sostituisce il BDNF, bensì rinforza il ponte di segnalazione che il BDNF crea. Invece di inserirsi in una rigida tasca ‘chiave-serratura’, agisce come una colla molecolare all’interfaccia TrkB-FRS2. Questa osservazione potrebbe avere importanti implicazioni per la ricerca scientifica e l’intervento terapeutico“.
Un promettente bersaglio terapeutico
I risultati ottenuti da Du e dai suoi colleghi hanno fatto nuova luce sui processi biologici attraverso i quali il CBD potrebbe ridurre l’accumulo di proteine nel cervello, diminuire l’infiammazione e promuovere una sana funzionalità cerebrale. Inoltre, il team ha dimostrato che le interazioni tra proteine, come FRS2 e TrkB, potrebbero essere bersaglio di terapie mirate utilizzando molecole che si legano a queste proteine, come il CBD.
“Questo approccio terapeutico aggira le problematiche delle terapie basate sul BDNF: scarsa stabilità, penetrazione limitata nel cervello e rischio di convulsioni“, ha affermato Du.
“Abbiamo scoperto che il CBD fornisce una neuroprotezione delicata e duratura e, cosa notevole, un singolo intervento può migliorare diverse patologie: Tau, Aβ, neuroinfiammazione e perdita sinaptica“.
Se validati sugli esseri umani, i risultati del team potrebbero aprire la strada allo sviluppo di nuove terapie per l’Alzheimer che prendono di mira l’interfaccia tra le proteine FRS2 e TrkB. Nello specifico, potrebbero fornire indicazioni per la progettazione di nuovi farmaci che si legano a queste proteine in modo più efficace e selettivo rispetto al CBD.
“Ciò che mi entusiasma di più è il concetto di ‘ attivazione indipendente dal ligando‘ “, ha affermato Du. “Nelle fasi avanzate dell’Alzheimer, i neuroni perdono la capacità di produrre BDNF. Poiché il CBD attiva il TrkB senza richiedere il BDNF, questa via rimane accessibile anche negli stadi più avanzati, un aspetto cruciale dato che la maggior parte dei pazienti riceve la diagnosi dopo una significativa progressione della malattia“.
In futuro, questo recente studio potrebbe aprire nuove prospettive per il trattamento della malattia di Alzheimer e di altre patologie neurodegenerative. Nel frattempo, Du e i suoi colleghi intendono approfondire le loro osservazioni e sviluppare nuovi farmaci che agiscano sulle proteine FRS2 e TrkB.
“Il CBD presenta dei limiti: efficacia modesta e potenziali effetti indesiderati”, ha affermato Du. “Ora stiamo utilizzando la progettazione guidata dalla struttura per rimodellare l’impalcatura del CBD, introducendo un ingombro sterico per ridurre le interazioni indesiderate e al contempo rafforzare il legame all’interfaccia FRS2-TrkB. Il nostro obiettivo è sviluppare colle molecolari di nuova generazione con maggiore potenza e selettività“.
Legg ache: Alzheimer: esosomi arricchiti con miR-124-3p mostrano un potenziale terapeutico
Nell’ambito delle loro future ricerche, gli studiosi intendono testare le nuove molecole ottimizzate che stanno progettando su modelli murini che riproducono la forma più comune di malattia di Alzheimer, nota come Alzheimer sporadico. Si tratta di un tipo di Alzheimer che non può essere ricondotto a mutazioni genetiche ereditarie e si stima che rappresenti oltre il 95% dei casi di Alzheimer nell’uomo.
“Stiamo anche valutando se questa strategia di ‘colla molecolare’ sia applicabile ad altre malattie neurodegenerative”, ha aggiunto Du. “In definitiva, il nostro obiettivo è quello di affermare la ‘riprogrammazione dell’omeostasi dei complessi proteici’ come un nuovo paradigma farmacologico, andando oltre la semplice eliminazione della patologia per puntare al ripristino funzionale, con candidati farmaci meccanicisticamente definiti pronti per l’ulteriore sviluppo“.
Fonte: Molecular Psychiatry