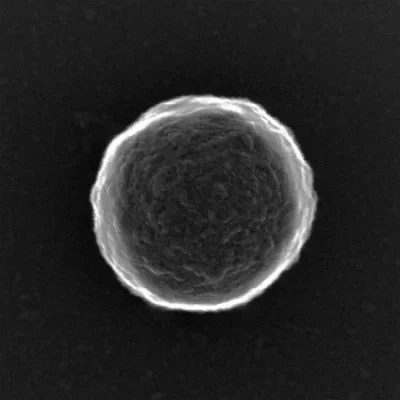
Microrobot: una singola microbolla ripresa con microscopia elettronica a scansione e trasmissione (STEM). Crediti immagine: Gao Lab/Caltech
Il potenziale dei microbot è enorme. Questi oggetti in miniatura possono essere progettati per svolgere azioni all’interno del corpo, come rilevare biomarcatori, manipolare oggetti come i coaguli di sangue o somministrare farmaci ai siti tumorali. Ma capire come rendere questi minuscoli robot efficaci, biocompatibili ed economici è una sfida.
Ora un team guidato dal Caltech ha compiuto un enorme passo avanti verso la realizzazione della prossima generazione di microrobot per la somministrazione di farmaci. Hanno semplificato sia la struttura dei microrobot sia il loro metodo di produzione, rendendoli altamente efficaci e sufficientemente “intelligenti” da dirigersi autonomamente verso un tumore.
Il team di scienziati del Caltech e dell’USC descrive i bubble bot e la loro applicazione di successo nel trattamento dei tumori della vescica nei topi in un articolo apparso nel numero della rivista Nature Nanotechnology.
Il team, guidato da Wei Gao, Professore di ingegneria medica al Caltech e ricercatore dell’Heritage Medical Research Institute, ha precedentemente utilizzato l’imaging ecografico e la guida magnetica su un modello animale per consegnare mini robot stampati in 3D a un tumore, dove potevano biodegradarsi e rilasciare il loro carico: farmaci antitumorali. Questi microrobot sono stati fabbricati in una camera bianca con attrezzature specializzate e presentavano un guscio di idrogel, costituito da un polimero gelatinoso che circondava una microbolla. Questo guscio ha contribuito a far muovere i robot e ha fornito un eccellente contrasto di imaging per consentire ai ricercatori di monitorarli all’interno del corpo.
“Abbiamo pensato: e se rendessimo tutto ancora più semplice, trasformando la bolla stessa in un robot?”, racconta Gao. “Possiamo creare bolle facilmente e sappiamo già che sono altamente biocompatibili. E se vogliamo farle scoppiare, possiamo farlo immediatamente”.

Gli scienziati hanno creato due diversi tipi di bubble bot. Quelli illustrati nella parte superiore di questa immagine sono modificati con nanoparticelle magnetiche e indirizzati verso un bersaglio tumorale tramite magneti esterni. I bot illustrati nella parte inferiore hanno enzimi diversi legati alla superficie e seguono un gradiente chimico per localizzare il bersaglio tumorale in modo indipendente. Crediti immagine: Gao Lab/Caltech
Il team ha sviluppato un metodo per creare questi semplici robot a bolle. Utilizzando una sonda a ultrasuoni, hanno agitato una soluzione a base di BSA (albumina sierica bovina, una proteina animale standard spesso utilizzata negli esperimenti di laboratorio) per creare migliaia di microbolle con involucri proteici.
Successivamente, gli scienziati hanno sfruttato un’altra caratteristica del guscio proteico: gli abbondanti gruppi amminici disponibili sulla superficie. I gruppi amminici sono un insieme di atomi caratterizzati da un legame carbonio-azoto, facilmente modificabili chimicamente. Legandosi a questi gruppi amminici, i ricercatori hanno creato due tipi di microrobot con diversi modi di controllare i propri movimenti. E farmaci antitumorali come la Doxorubicina possono legarsi con successo alla superficie di entrambe le versioni.
Gli scienziati hanno applicato l‘enzima ureasi sulla superficie di entrambe le versioni dei robot a bolle. L’ureasi agisce come un piccolo motore per far muovere i robot. L’enzima catalizza una reazione con l’urea, un prodotto di scarto abbondantemente presente in tutto il corpo che funge da biocarburante per i robot, producendo ammoniaca e anidride carbonica. Poiché l’ureasi non è distribuita uniformemente sulla superficie delle bolle, col tempo, una maggiore quantità di questi prodotti si accumulerà su un lato rispetto all’altro. Questo squilibrio crea un ambiente chimico asimmetrico attorno alla bolla, generando una “spinta” netta che spinge in avanti i microrobot.
Nella prima versione, il team ha applicato nanoparticelle magnetiche alla superficie dei bubble bot, rendendoli magneticamente sensibili. Con l’aiuto dell’imaging ecografico delle microbolle interne dei bubble bot, è stato possibile orientarli con magneti esterni per dirigerli verso un bersaglio all’interno del corpo.
Ma i ricercatori volevano fare un ulteriore passo avanti. “Volevamo rendere i robot più intelligenti”, afferma Gao. Sapendo che tumori e infiammazioni producono elevate concentrazioni di perossido di idrogeno rispetto alle cellule normali, il team ha deciso di legare un ulteriore enzima, la catalasi, alla superficie di una seconda versione dei microrobot. La catalasi innesca una reazione con il perossido di idrogeno, creando acqua e ossigeno. Attraverso il cosiddetto comportamento chemiotattico, le bolle legate alla catalasi si muovono automaticamente verso concentrazioni più elevate di perossido di idrogeno, dirigendole verso i tumori.
Leggi anche:Trattare il cancro al fegato con i microrobot
“In questo caso, non è necessaria alcuna diagnostica per immagini; non è necessario alcun controllo esterno. Il robot è abbastanza intelligente da individuare il tumore“, spiega Gao. “Il movimento autonomo del robot a bolle, insieme alla sua capacità di percepire il gradiente di perossido di idrogeno, porta a questo target, che chiamiamo target tumorale chemiotattico”.
Una volta che i robot raggiungono il bersaglio, gli scienziati possono applicare ultrasuoni focalizzati per far scoppiare le bolle, rilasciando il loro carico terapeutico. Questa potente azione di scoppio migliora la penetrazione del farmaco nel tumore rispetto ai robot idrogel a lenta degradazione utilizzati in precedenza dal team.
Quando gli scienziati hanno iniettato dei bubble bot nei topi per somministrare terapie antitumorali, hanno osservato una riduzione di circa il 60 percento del peso dei tumori alla vescica nell’arco di 21 giorni, rispetto ai topi a cui era stato somministrato solo il farmaco.
“Questa piattaforma robotica a bolle è semplice, ma integra tutto ciò che serve per la terapia: biocompatibilità, movimento controllabile, guida per immagini e un trigger on-demand che aiuta il farmaco a penetrare più in profondità nel tumore. Il nostro obiettivo è sempre stato quello di avvicinare i microrobot all’uso clinico reale, e questo progetto robotico rappresenta un grande passo in questa direzione”, afferma l’autore principale dell’articolo, Songsong Tang, che ha completato il lavoro durante il suo periodo come ricercatore post-dottorato nel laboratorio di Gao al Caltech; Tang entrerà a far parte dell’Università di Scienza e Tecnologia della Cina come Professore.
Scritto da Kimm Fesenmaier
Fonte: Caltech