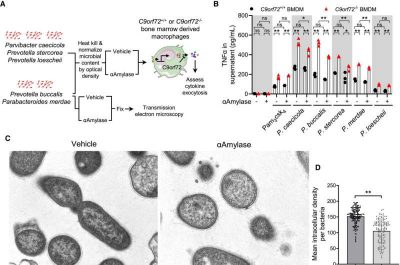
SLA e demenza frontotemporale-immagine:C9orf72 nei macrofagi limita la risposta infiammatoria al glicogeno batterico. Crediti: Cell Reports (2026).
Una scoperta significativa dei ricercatori della Case Western Reserve University potrebbe cambiare il modo in cui i medici trattano due delle malattie neurodegenerative più devastanti. Il team ha identificato un legame tra la flora batterica intestinale e il deterioramento cerebrale nella sclerosi laterale amiotrofica (SLA) e nella demenza frontotemporale (FTD). I ricercatori hanno scoperto che alcuni zuccheri batterici causano risposte immunitarie che uccidono le cellule e come prevenirle.
La FTD colpisce principalmente i lobi frontali e temporali del cervello, causando cambiamenti nella personalità, nel comportamento e nel linguaggio. La SLA colpisce principalmente i motoneuroni, causando una graduale debolezza muscolare e paralisi.
La maggior parte delle cause dei casi di SLA e FTD sono sconosciute, sebbene i ricercatori abbiano esaminato diverse possibili cause, tra cui la genetica, problemi ambientali, lesioni cerebrali e dieta.
Uno studio individua un collegamento molecolare mancante
Lo studio, recentemente pubblicato su Cell Reports, risolve un interrogativo di lunga data sulle malattie neurodegenerative. Il team ha scoperto una connessione molecolare che spiega perché alcune persone con specifiche mutazioni genetiche sviluppano la DFT e la SLA, mentre altre no.
“Abbiamo scoperto che i batteri intestinali nocivi producono forme infiammatorie di glicogeno (un tipo di zucchero) e che questi zuccheri batterici innescano risposte immunitarie che danneggiano il cervello“, ha affermato Aaron Burberry, Professore associato presso il Dipartimento di Patologia della Case Western Reserve School of Medicine.
Burberry, il ricercatore senior dello studio, ha riferito che il 70% dei 23 pazienti affetti da SLA/FTD esaminati presentava livelli di glicogeno pericolosi. Tra coloro che non soffrivano di patologie cerebrali, solo un terzo presentava livelli elevati di glicogeno.
Lo studio ha implicazioni immediate per l’assistenza ai pazienti, poiché identifica nuovi obiettivi per il trattamento della SLA e della FTD, fornendo al contempo biomarcatori per identificare i pazienti che potrebbero trarre beneficio da terapie mirate all’intestino.
Potenziale per nuovi trattamenti incentrati sull’intestino
Questa scoperta apre la strada alla sperimentazione di nuovi trattamenti che scompongono gli zuccheri nocivi nell’intestino e apre le porte allo sviluppo di farmaci che agiscono sulla connessione tra l’apparato digerente e il cervello, offrendo potenzialmente nuove speranze ai pazienti affetti da queste devastanti malattie cerebrali.
Alex Rodriguez-Palacios, Professore associato presso il Digestive Health Research Institute presso la Facoltà di Medicina, ha affermato che il team ha utilizzato i risultati delle sue ricerche per ridurre gli zuccheri nocivi, il che “ha migliorato la salute del cervello e prolungato la durata della vita”.
La loro scoperta è particolarmente significativa per i cosiddetti portatori della mutazione C90RF72, la causa genetica più comune di SLA e FTD. La ricerca spiega perché alcune persone con la mutazione sviluppano le malattie mentre altre no, identificando i batteri intestinali come un fattore scatenante ambientale chiave.
Modelli murini all’avanguardia consentono approfondimenti
Il Dipartimento di Patologia e l’Istituto di Ricerca sulla Salute Digestiva dell’Università sono all’avanguardia nella ricerca sulle malattie neurovegetative grazie alla loro capacità unica di condurre studi utilizzando modelli murini privi di germi, ovvero topi cresciuti in ambienti completamente sterili e privi di batteri, consentendo ai ricercatori di studiare esattamente in che modo specifici batteri intestinali influenzano le malattie cerebrali.
Leggi anche:SLA e demenza frontotemporale: trovate proteine anomale nel liquido cerebrospinale
Fabio Cominelli, illustre Professore universitario e Direttore del Digestive Health Research Institute, supervisiona questo programma, che si basa su un innovativo sistema di allevamento sterile “gabbia nella gabbia” sviluppato da Rodriguez-Palacios, una capacità tecnica che poche Istituzioni al mondo possiedono e che ha reso possibile questa scoperta.
Questo progetto rende possibili gli studi microbiologici su larga scala necessari per comprendere la complessa comunicazione tra intestino e cervello, una ricerca che sarebbe impossibile condurre con i metodi tradizionali, che possono coinvolgere solo pochi topi alla volta.
“Per capire quando e perché viene prodotto glicogeno microbico dannoso, il team condurrà studi più ampi che esamineranno le comunità del microbioma intestinale nei pazienti con SLA/FTD prima e dopo l’insorgenza della malattia”, ha affermato Burberry. “I nostri risultati supportano anche gli studi clinici per determinare se la degradazione del glicogeno nei pazienti con SLA/FTD possa rallentare la progressione della malattia e potrebbero iniziare tra un anno”.
Fonte: Cell Reports