SLA-immagine: astratto grafico Credit Cell.
I ricercatori dell’Università dello Utah presso il Pulst-Scoles Laboratory hanno scoperto che la riduzione dei livelli della proteina STAUFEN-1 può prevenire la morte dei neuroni causata dal danno al DNA e dall’attivazione di p53 nelle malattie neurodegenerative come la SLA.
Quando le cellule cerebrali muoiono in malattie come la SLA (sclerosi laterale amiotrofica) e la demenza frontotemporale, spesso attivano un programma di “autodistruzione” chiamato apoptosi. Ora, i ricercatori del Laboratorio Pulst-Scoles del Dipartimento di Neurologia dell’Università dello Utah hanno scoperto un nuovo modo promettente per proteggere i neuroni da questo processo dannoso, prendendo di mira una proteina chiamata STAUFEN-1.
I risultati, pubblicati sulla rivista Cell Death & Disease, potrebbero portare a nuovi trattamenti per numerose malattie neurodegenerative, tra cui la SLA, il morbo di Parkinson e il morbo di Alzheimer.
Come muoiono i neuroni nella SLA e nelle malattie neurodegenerative: il ruolo di p53 e del danno al DNA
Mandi Gandelman, MSci, Ph.D., prima autrice dello studio, ha dedicato la sua carriera alla comprensione della morte neuronale nelle malattie neurodegenerative. “Studio come e perché i neuroni muoiono durante queste malattie, cosa ne determina la morte e come possiamo prevenirla”, ha spiegato Gandelman.
La sfida è particolarmente urgente perché oltre il 90% delle malattie neurodegenerative non è ereditario. “Dobbiamo scoprire come i neuroni dicono: ‘Ricevo segnali che devo morire’ e intervenire in quel momento“, ha affermato Gandelman.
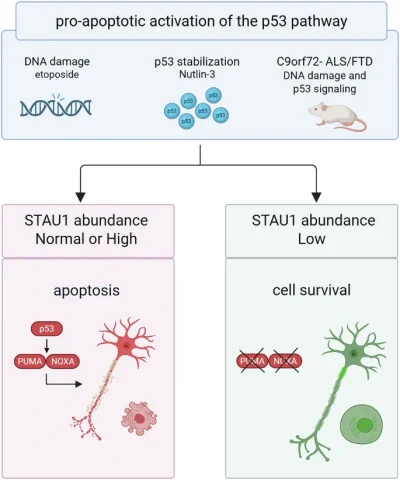
Uno dei principali fattori scatenanti della morte neuronale è un percorso cellulare controllato da una proteina chiamata p53. Quando attivata da stress o danni, p53 può segnalare ai neuroni di morire quando non dovrebbero, accelerando la progressione della malattia. Gandelman e i suoi colleghi hanno scoperto che una proteina chiamata STAUFEN-1, i cui livelli aumentano in modo anomalo in diverse malattie neurodegenerative, svolge un ruolo cruciale in questo processo mortale.
Test della riduzione di STAUFEN-1 nei neuroni e nelle cellule cerebrali umane
Il team di ricerca ha utilizzato molteplici approcci sperimentali, a partire dai neuroni umani creati da cellule staminali pluripotenti indotte. “Li chiamiamo neuroni derivati da iPSC”, ha spiegato Gandelman. “Possiamo differenziarli in neuroni e poi studiarli in vitro”. L’utilizzo dei neuroni umani è stato fondamentale. “Quando otteniamo una scoperta, vogliamo essere certi di poterla trasmettere ai pazienti“, ha osservato Gandelman.
I ricercatori hanno analizzato per la prima volta l’espressione genica quando i livelli di STAUFEN-1 erano ridotti e hanno scoperto che oltre 3.000 geni modificavano la loro attività, con molti geni responsabili della morte cellulare. Poi sono arrivati gli esperimenti critici: l’esposizione dei neuroni a composti che attivano p53 e normalmente causano una morte cellulare estesa. Un composto, l’etoposide, provoca rotture del DNA.
“Le cellule cercano di riparare queste rotture e, di solito, quando aggiungiamo una quantità sufficiente di questo composto, non riescono a ripararle e muoiono tutte in modo massiccio“, ha spiegato Gandelman.
Ma quando i livelli di STAUFEN-1 sono stati ridotti, è successo qualcosa di straordinario: “Se abbassiamo i livelli di STAUFEN-1, si prevengono i danni al DNA e le cellule sopravvivono”, ha affermato Gandelman. La protezione era spettacolare.
“Questi composti causano danni molto estesi al DNA e morte cellulare nei neuroni, a meno che non interveniamo su STAUFEN-1. Questo è importante perché tali rotture sono molto comuni in tutte le malattie neurodegenerative“, ha osservato Gandelman.
Cosa sono i neuroni derivati dalle cellule iPSC e perché sono importanti per la ricerca sulla SLA
I neuroni derivati da iPSC sono cellule cerebrali umane coltivate in laboratorio a partire da cellule adulte riprogrammate. Gli scienziati le usano come “cervello in vitro” per studiare malattie cerebrali come la SLA e il morbo di Parkinson, testare nuovi farmaci e comprendere il funzionamento del cervello umano. Questi neuroni coltivati in laboratorio possono comportarsi come vere cellule nervose, formando connessioni e inviando segnali. I ricercatori stanno ora lavorando per rendere questi modelli più realistici coltivando reti di diversi tipi di cellule cerebrali, come cellule di supporto e immunitarie, per imitare meglio ciò che accade nel cervello umano.
I modelli murini di SLA confermano la riduzione di STAUFEN-1 come una promettente strategia terapeutica
Per garantire che i loro risultati non si limitassero alle condizioni di laboratorio, i ricercatori hanno testato topi portatori della mutazione C9orf72, una delle cause genetiche più comuni di SLA. Questi topi accumulano danni al DNA nel corso della loro vita.
Il team ha incrociato questi topi con topi affetti dalla malattia con topi che presentavano livelli più bassi di STAUFEN-1. I risultati rispecchiavano gli esperimenti sui neuroni umani: la via di morte p53 era meno attivata.
“Abbiamo dimostrato che questo funziona nei neuroni umani e che funziona anche con i fattori scatenanti della morte neuronale nel topo”, ha affermato Gandelman. “Questo ci fornisce una buona risposta su come questo potrebbe essere utile per la terapia”.
Leggi anche:SLA-SOD1: nuovo farmaco stabilizza il declino
Dalla scoperta alla terapia: avanzare i trattamenti STAUFEN-1 verso le sperimentazioni cliniche sulla SLA
“In molte malattie neurologiche, l’abbondanza di STAUFEN-1 aumenta”, ha spiegato Gandelman. “E inoltre, osserviamo che molte di queste malattie presentano livelli elevati di danno al DNA. In questo articolo, abbiamo descritto come la riduzione di questi livelli elevati di STAUFEN-1 prevenga il danno al DNA”.
Il laboratorio sta ora sviluppando molecole terapeutiche per studi clinici. Daniel Scoles, Ph.D., sta analizzando oligonucleotidi antisenso, molecole in grado di degradare l’RNA di STAUFEN-1 e ridurne i livelli nel sistema nervoso.
Poiché i livelli di STAUFEN-1 sono elevati in numerose malattie neurodegenerative, questo approccio potrebbe potenzialmente aiutare i pazienti affetti da SLA, Parkinson, Alzheimer e altre patologie in cui il danno al DNA provoca la neurodegenerazione.
Ulteriori informazioni: Cell Death & Disease