Tumori aggressivi-immagine: Ifetroban, un farmaco antipiastrinico già dimostratosi sicuro per l’uso umano, potrebbe rallentare efficacemente la diffusione del cancro aggressivo, secondo un nuovo studio pubblicato su Experimental Hematology and Oncology. Crediti: Srijita Chattopadhyay/Ole Miss Digital Imaging Services
I tumori aggressivi possono utilizzare i vasi sanguigni come fossero strade, accelerando attraverso il corpo e trovando nuovi spazi in cui crescere. Ma una nuova ricerca dimostra che un farmaco in fase di sperimentazione clinica potrebbe aiutare a fermare la diffusione del cancro prima che raggiunga la sua destinazione.
Come l’ifetroban interrompe la diffusione del cancro
Una ricerca dell’Università del Mississippi dimostra che l’Ifetroban, un farmaco antiaggregante piastrinico, può aiutare il sistema immunitario a identificare e rimuovere meglio le cellule tumorali entrate nel flusso sanguigno. Bloccare le metastasi, il processo attraverso il quale i tumori si diffondono, toglierebbe “i denti” a malattie aggressive come il cancro al seno, ai polmoni e al pancreas.
“La diffusione del cancro è ciò che uccide le persone“, ha affermato Thomas Werfel, Professore associato di ingegneria biomedica. “Possiamo curare il cancro localizzato: è il cancro metastatico a essere davvero devastante, ed è quello che stiamo prendendo di mira. Quando le cellule tumorali entrano nel flusso sanguigno, formano legami con le piastrine, creando di fatto uno “scudo” attorno alla cellula tumorale che la nasconde ai globuli bianchi e ad altri agenti del sistema immunitario”.
Leggi anche: Tumori aggressivi: nuovi obiettivi per diagnosi e trattamento
Ifetroban impedisce la formazione di questi legami piastrinici, consentendo al sistema immunitario di colpire e rimuovere le cellule tumorali prima che si diffondano in una nuova sede.
“Una volta che il cancro entra nella fase metastatica, la sopravvivenza diminuisce notevolmente”, ha affermato Veeresh Toragall, ricercatore post-dottorato presso il Dipartimento di Ingegneria Biomedica. “Ciò che stiamo pensando è di colpire le metastasi, la diffusione del cancro. In questo caso, ciò che abbiamo fatto è molto semplice: abbiamo ridotto l’interazione tra le piastrine e le cellule tumorali. Una volta eliminata l’interazione tra questi due, le piastrine non proteggono più le cellule tumorali circolanti nell’organismo. Quindi, il sistema immunitario è libero di attaccare queste cellule tumorali e rimuoverle”.
Risultati dello studio e potenziale futuro
Lo studio, pubblicato su Experimental Hematology and Oncology, ha testato la capacità di Ifetroban di interrompere la schermatura piastrinica nel carcinoma mammario triplo negativo, una patologia particolarmente aggressiva che rappresenta 1 diagnosi di tumore al seno su 10. Studi precedenti hanno dimostrato che il carcinoma mammario triplo negativo è associato a una maggiore attività del recettore TPr, che aiuta le piastrine ad aderire alle cellule tumorali.
“Quindi, la domanda era: quanto sarebbe stato efficace colpire il TPr e bloccarlo?”, ha detto Werfel. “Sappiamo che il TNBC è una malattia fortemente metastatica, e per noi aveva senso cercare di ridurre le metastasi per ridurre la mortalità”.
Lo studio ha dimostrato che l’Ifetroban ha ridotto le metastasi polmonari del 67%, le metastasi epatiche del 60% nei modelli animali e ha ridotto le cellule tumorali circolanti complessive di oltre il 50%.
“Al momento, ci sono pochissimi farmaci, se non nessuno, approvati per colpire specificamente le metastasi”, ha detto Werfel. “Questo non sostituirà altri farmaci antitumorali. Sarà comunque necessaria la terapia citotossica per uccidere le cellule tumorali. Ma mentre li uccidi, sai che non andranno altrove e non creeranno nuovi tumori”.
Astratto
“Oltre al loro ruolo centrale nell’emostasi del sangue, è sempre più chiaro che le piastrine contribuiscono a molteplici fasi della cascata metastatica. Le piastrine sono una delle cellule più abbondanti con cui le cellule tumorali interagiscono una volta entrate in circolo e l’interazione delle piastrine con le cellule tumorali può migliorare la sopravvivenza delle cellule tumorali, l’arresto e l’adesione nei siti secondari, nonché l’extravasazione. Pertanto, mirare all’interazione tra piastrine e cellule tumorali circolanti potrebbe essere un approccio efficace per ridurre le metastasi. In questo studio, riproponiamo l’Ifetroban, un inibitore del recettore del trombossano A2 – prostanoide (TPr), per bloccare le interazioni piastrine-cellule tumorali e ridurre le metastasi in modelli di carcinoma mammario triplo negativo (TNBC). Utilizziamo modelli di co-coltura in vitro di piastrine e linee cellulari tumorali per valutare l’impatto del trattamento con fetroban sull’adesione delle piastrine alle cellule tumorali. In ciascun caso, l’adesione piastrine-cellule tumorali è aumentata significativamente con l’introduzione dell’agonista del TPr U46619, mentre il pretrattamento con Ifetroban (antagonista del TPr) ha ridotto significativamente l’adesione piastrine-cellule tumorali. Inoltre, abbiamo utilizzato un sistema modello di pesce zebra per valutare rapidamente le interazioni tra metastasi e piastrine in vivo, dimostrando che Ifetroban riduce le metastasi degli xenotrapianti di MDA-MB-231 senza ridurre il numero di piastrine negli embrioni di pesce zebra transgenici CD41. Infine, confermiamo che Ifetroban riduce significativamente le metastasi sia polmonari che epatiche in diversi modelli murini di TNBC (4T1 e MDA-MB-231). In questi modelli, abbiamo osservato che Ifetroban riduce le metastasi in assenza di un tumore primario e quando il TPr viene eliminato dalle cellule tumorali, supportando ulteriormente l’idea che Ifetroban attenua il ruolo di supporto del TPr piastrinico nella cascata metastatica. Sulla base dei risultati di questo studio, l’Ifetroban potrebbe essere utilizzato come agente clinico per ridurre le metastasi nei pazienti con tumore al seno triplo negativo“.
Abstract grafico
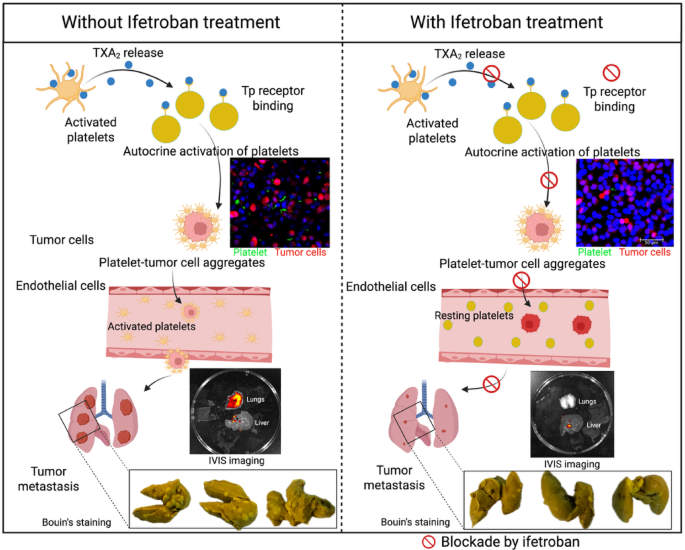
Poiché la sicurezza dell’Ifetroban è già stata testata su oltre 1.400 pazienti in precedenti studi clinici, potrebbe diventare una terapia contro il cancro molto più rapidamente rispetto ai tempi tradizionali di scoperta dei farmaci.
“Questo farmaco è già stato studiato per altri usi ed è attualmente in fase di sperimentazione clinica“, ha affermato Toragall. “Questo accorcia i tempi di approvazione per il trattamento delle metastasi del cancro. Non dovremo aspettare 15 anni per metterlo sul mercato se si dimostrerà sicuro ed efficace negli studi clinici sul cancro”.
Fonte: Experimental Hematology & Oncology